Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 242
A hepatocellularis carcinoma célzott és immunkezelése: előrejelzés 2019-re és azon túl
A hepatocellularis carcinoma (HCC) szisztémás kezelésének hatásossága lényegesen javult, miután a SHARP vizsgálatban és az Asia Pacifi c vizsgálatban 2007-ben kimutatták, hogy egy molekulárisan célzott kezelés, a szorafenib használatával meghosszabbodik a túlélés. A szorafenib tágította az előrehaladott hepatocellularis carcinomában szenvedők kezelési lehetőségeit, és némileg meghosszabbította az előrehaladott HCC-s betegek túlélését. Ugyanakkor szükség volt egy, a szorafenibnél még hatásosabb első vonalban használható molekulárisan célzott gyógyszerre, valamint egy progresszió után – vagy szorafenibintolerancia esetén – alkalmazható második vonalú gyógyszerre, mivel a szorafenib nem csökkenti a tumor méretét, illetve nem okoz nekrózist a tumorban, ráadásul relatíve súlyos mellékhatásai vannak, mint például a kéz-láb bőrreakcó. 2007 és 2016 között számos első és második vonalban használandó anyagot vizsgáltak, de az összes ilyen irányú klinikai vizsgálat sikertelen volt. Legújabban viszont négy anyaggal (regorafenib, lenvatinib, kabozantinib, ramucirumab) sikeresnek bizonyultak a 2017-ben és 2018-ban végzett klinikai vizsgálatok, és két anyag (regorafenib és lenvatinib) már használható is a klinikai gyakorlatban, a másik két szer (karbozantinib és ramucirumab) engedélyezése még folyamatban van. Továbbá folyamatban van öt olyan klinikai vizsgálat is, amelyekben a transarterialis chemoembolisatiót (TACE-t) és egy eddig sikertelen molekuláris célzott anyag adását kombinálják. Egy, a 2018-as ASCO-n elhangzott előadáson a TACE és a szorafenib (TACTICS vizsgálat) kombináció sikeréről számoltak be. Fázis III vizsgálatok vannak folyamatban immunellenőrzőpontgátlókkal, valamint immunellenőrzőpont-gátlók és molekulárisan célzott szerek kombinációjával, és remélhetően a HCC minden stádiumában, a korai, a középső és az előrehaladott stádiumban egyaránt drasztikusan meg fog változni a kezelés kialakult rendszere a közeljövőben.
Korai tapasztalataink CyberKnife-kezeléssel suprasellarisan is terjedő hypernephroma-áttét esetén
Intra-, suprasellarisan is terjedő daganatok között ritka az áttét; a leggyakoribb elsődleges daganat a tüdő- és az emlőcarcinoma. Cikkünkben intra- és suprasellarisan elhelyezkedő világossejtes veseáttétes beteg kórtörténetét ismertetjük.
Avelumabkezelés kemoterápiára refrakter, áttétes Merkel-sejtes carcinomában
A Merkel-sejtes carcinoma egy igen ritka, agresszív bőrdaganat, amelynek áttétes eseteiben a különböző kemoterápiás kezelések ellenére igen rossz a prognózis (az ötéves túlélés mindössze 0-18%). 100 000-ből 0,2-0,4 esetben fordul elő évente Európában, évente 0,79 esetről tudunk az Egyesült Államokban és 1,6 esetet írnak le (100 000 személyenként) évente Ausztráliában. A gyakoriság az utóbbi évtizedekben jelentősen emelkedett. A betegek átlagéletkora körülbelül 75 év körül van, közülük 5-12% a diagnózis idején már távoli áttétekkel jelentkezik.
Avelumab Merkel-sejtes tumorokban
Merkel-sejtes carcinoma (MCC) a bőr primer, agresszív, de ritkán előforduló rosszindulatú daganata, amely 33-46%-os halálozással jár. Az I-III. stádiumokban a műtét tekinthető kezelési standardnak, az áttétes, IV. stádiumban viszont a kemoterápia jön szóba. A daganat érzékeny a kemoterápiára, de a várható túlélés a kemoterápiára adott kezdeti jó válasz után sem haladja meg a 10 hónapot.
Immunonkológia
2017. MÁRCIUS 01.
Áttetes colorectalis daganatos betegek Masodvonalbeli kezelest kovető tovabbi kezelese: Szisztematikus attekintes
Háttér: Az áttétes colorectalis daganatos (mCRC) betegek másodikvonalbeli kezelése utáni optimális kemoterápiás kezelés kérdése még nem tisztázott. Anyag és módszer: A szerzők szisztematikusan kikeresték a Cochrane Database of Systematic Reviews-ban, az EMBASEben és a Medline-ban 2002. január és 2017. május között a témában megjelent publikációkat, valamint átnézték a 2014. január és 2017. június között tartott kongresszusok adatbázisait. A hatásosság, a biztonságosság és a betegek beszámolói alapján válogatták ki a monoterápiákat és kombinált kezeléseket, tekintet nélkül arra, hogy az mCRC betegség második vonalbeli kezelés utáni kezelése milyen dózisokkal és hány ciklusban történt. A tanulmányokat azok kialakítása és minősége szerint választották ki, és az adatokat minőségük szerint összesítve kísérelték meg a különböző kezeléseknek a teljes túlélésre és az egyéb, daganatos megbetegedésekkel összefüggő jellemzőkre gyakorolt hatását megérteni. Eredmények: A kutatás során 938 tanulmányt találtak a témában, amelyek közül 68 volt alkalmas minőségi összesítésre. Csak elég korlátozott bizonyítékokat találtak a kemoterápia, a célzott terápia vagy mindkettő újraindítására (a rechallenge-re). A trifl uridin/tipiracil (TAS-102 néven is ismert) kombináció, illetve a regorafenib kezelés a placebóhoz képest hosszabb teljes túléléssel járt előzetesen konvencionális kemoterápiával, vagy célzott terápiával kezelt betegeknél. Ugyanakkor ezen kezelések hatásossága között nem lehetett különbséget igazolni. Ilyen helyzetben a megfelelő kezelés kiválasztásához a betegek elvárásait és az életminőséget is fi gyelembe kell venni. Következtetések: Ezek a megfi gyelések alátámasztják másodikvonalbeli kezelésekre nem reagáló mCRC-ben az olyan törzskönyvezett kezelések használatát, mint a trifl uridin/tipiracil vagy a regorafenib.
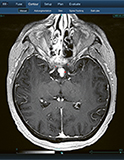
[A foramen jugulare schwannomája következtében kialakuló izolált nervus hypoglossus bénulás]
[Bevezetés - Habár a nyelv alatti ideg más agyidegekkel együtt gyakran érintett a patológiás agyi, agytörzsi folyamatokban, az izolált nervus hypoglossus bénulás diagnosztikus kihívást jelentő, ritka betegség. ]
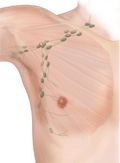
Aktualitások a férfi emlőrákról
A férfi emlődaganatok ritka betegségek, körülbelül az összes emlődaganat 1%-át teszik ki. A férfi emlődaganatok legnagyobb rizikófaktora a szervezetben előforduló emelkedett ösztrogénszint. Genetikai eltérések, mint a Klinefelter-szindróma, ösztrogénexpozíció és egyéb metabolikus deviancia elősegíthetik a férfi ak emlődaganatának kialakulását. A klinikai tünetek megjelenése és a diagnózis felállítása között hosszabb idő telik el, mint a nőknél, és a férfi emlődaganatokat idősebb korban, előrehaladott stádiumban ismerik fel. A BRCA2-mutáció körülbelül 10%-ban mutatható ki a férfi emlődaganatos betegekben. Leggyakoribb az invazív ductalis carcinoma ösztrogén- és progeszteronpozitivitással. A diagnosztikai, sebészi, sugárterápiás elvek és a kemoterápia közel megegyeznek a női emlődaganatok ellátásával. A szakmai ajánlások adjuváns és terápiás kezelés során tamoxifent és egyéb szelektív ösztrogénreceptor-modulátort javasolnak. Nagy nemzetközi adatbázisok alapján a túlélési adatok különböznek a férfi és a női emlődaganatos betegek között. Új biomarkerek, genetikai vizsgálatok vannak folyamatban, amelyek alapján jobban megismerhetővé válik a férfi emlődaganat.
Hírvilág
2019. FEBRUÁR 20.
Ritka Betegségek Világnapja a Szegedi Tudományegyetemen
A Szegedi Tudományegyetem a Ritka és Veleszületett Rendellenességgel Élők Országos Szövetségével (RIROSZ) együtt első alkalommal rendezi meg Szegeden a Ritka Betegségek Világnapja országos rendezvényét. A február 24-i program célja, hogy olyan fórumot teremtsen, ahol az érintett érdekcsoportok közösen tudják megvitatni a ritka betegségekkel élők helyzetét, terveit. Idén az egészségügy és a szociális ellátások közötti hídépítés, valamint a ritka betegségek kutatása, az új diagnosztikai és terápiás eljárásokat megalapozó fejlesztések kerülnek a fókuszba.
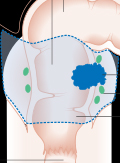
Az áttétes colorectalis rák molekuláris altípusai és a terápiás döntések fejlődése
A colorectalis ráknak (CRC) klinikailag igen jelentős molekuláris heterogenitása van, amely különböző szinteken jelentkezik: a genomikában, az epigenomikában, a transzkripcióban és a mikrokörnyezetben. A karcinogenezis során szerzett genomikus történések hajtják („drive”) áttétes helyzetben a rák progresszióját. Például a KRAS- és az NRAS-mutációk jelzik azokat a daganatsejt-populációkat, amelyek refrakterek az EGFR monoklonális antitestekre, a BRAFV600E-mutációt hordozók viszont rosszabb kimenetelre számíthatnak a standard kezelések és a kombinált célzott kezelések mellett, míg a HER2-amplifi káció arra utal, hogy a daganat különlegesen érzékeny egy kettős HER2-blokáddal szemben. A többszörös, ritka géneltérések által hajtott EGFR monoklonális antitestek elleni rezisztencia jelentős átfedésben van a primer, valamint a szerzett rezisztencia mechanizmusában a klónszelekciós folyamat során. Ebben a tekintetben refrakter esetekben a keringő tumor-DNS szekvenciális vizsgálata vezethet gyógyszerek kifejlesztéséhez. A ritka kinázfúziós események és a DNS-károsodás utáni repair-ben részt vevő gének komplex eltéréseit is leírták, amelyek a célzott kezelések targetjei lehetnek. Másrészt a transzkripció szubtípusai és a jelátviteli utak aktivációs jelei szintén prognosztikai és potenciálisan prediktív értékkel bírnak áttétes colorectalis rákban. Ezek a jelek a stromalis sejtek és az immunkörnyezeti sejtek, valamint a daganatsejtek közötti interakciókat jelzik. Például a mikroszatellita-instabilitást mutató (MSI) vagy a POLE ultramutáns CRC-daganatsejtek különlegesen érzékenyek az immunellenőrzőpont-gátlókra, míg az olyan mesenchymalis fenotípusú daganatok, amelyeket az immunszuppresszív molekulák aktivációja jellemez, jó tárgyai lehetnek egy új immunterápiás kombináció kialakítására. Ebben a cikkben átnézzük az áttétes CRC-ben kimutatott, célzott terápiára alkalmas onkogéneltéréseket és -szignatúrákat, valamint tárgyaljuk az új molekuláris diagnosztikus próbák klinikai alkalmazásának lehetőségeit.
1.
2.
3.
4.
5.
1.
Klinikum
Véletlen folytán, egy egyszerű vérvétellel derülhet ki az egyik legsúlyosabb gyerekbetegség2.
3.
4.
5.
Egészségpolitika
A Magyar Járóbeteg Szakellátási Szövetség állásfoglalása az ágazat helyzetéről