Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Terápiás területek
Neurológia
Neurológiai és pszichiátriai betegségek kezelése ketogén diétával
A 21. század kezdete óta exponenciálisan nő a ketogén diétával foglalkozó publikációk száma. A ketózis neurológiai betegségeket javító hatása már randomizált vizsgálatokban is bizonyítást nyert.
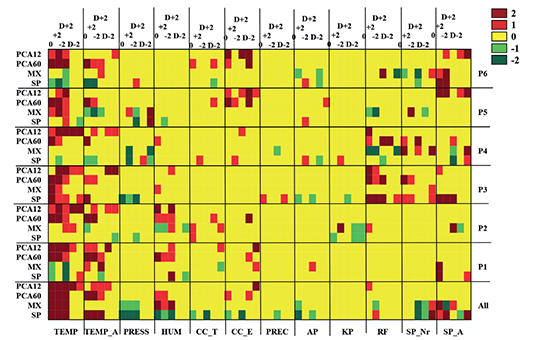
[Egyénre szabott fájdalom-időjárás kapcsolatelemzés: pilóta tanulmány ]
[A betegek beszámolója alapján jól ismert a fájdalom és az időjárás lehetséges összefüggése. Az eredmények azonban ellentmondóak, ami feltehetően az egyének közötti nagy érzékenységbeli különbségeknek köszönhető. Jelen tanulmány célja, hogy egyénre szabott módon jellemezze a fájdalom és az időjárás lehetséges kapcsolatait többféle statisztikai elemzés alkalmazásának kombinálásával.]
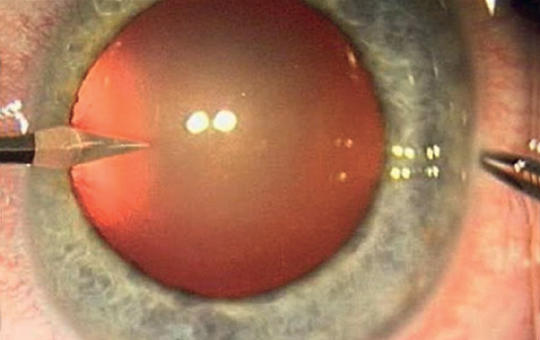
Arteria centralis retinae elzáródás thrombolysiskezelése és multidiszciplináris ellátása a hagyományos szemészeti kezelési formákkal összehasonlítva
Az arteria centralis retinae okklúzió eddigi konzervatív terápiái limitált hatékonyságúak, szemészeti osztályokon történtek, ahogyan az egységes protokoll nélküli etiológiai vizsgálatok is. Pedig az ACRO a központi idegrendszeri ischaemiás stroke analógiájának tekinthető, így a szisztémás thrombolysis és a multidiszciplináris ellátás hasonlóan hatékony lehet. Emiatt 2022 májusa óta a Semmelweis Egyetemen klinikai vizsgálat keretében a 4,5 órán belül diagnosztizált ACRO thrombolysiskezelését és etiológiai vizsgálatait végezzük egységes protokoll alapján.
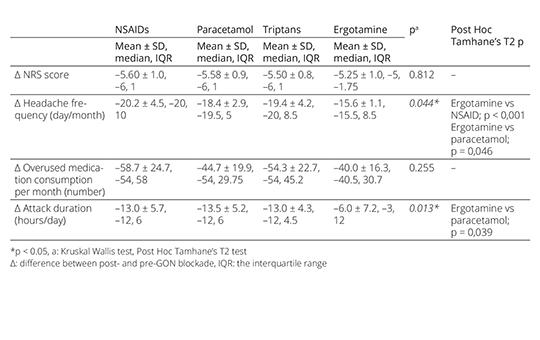
[A nervus occipitalis major gyógyszeres blokádjának hatása a gyógyszer-túlhasználathoz köthető fejfájás kezelésének megvonási időszakában ]
[A gyógyszerelés felfüggesztése továbbra is kulcsfontosságú elem a gyógyszertúlhasználathoz köthető fejfájás (medication overuse headache, MOH) kezelésében, azonban egyelőre nincs konszenzus a megvonási folyamat kivitelezésében. ]
Akut obstruktív hydrocephalus
Az American Heart Association (AHA) irányelvei alapján sikeres újraélesztést követően (return of spontaneous circulation, ROSC) a komatózus betegeknél 24 órán belül natív koponya CT-vizsgálat javasolt, mely a keringésmegállást követő neuroprognosztikáció részét képezi.
A nők és a migrén
A migrén a lakosság 14%-át érintő betegség, előfordulása a 20–64 év közötti, aktívan dolgozó és nagyrészt reproduktív korban lévő nők körében a legmagasabb, közel 20%. Migrénes nők 18–25%-ában jelent- kezik roham a menses idejében is, de 7%-uknak csak a menseshez kapcsolódóan van migrénrohama. Ezen rohamok kiváltásában az ösztrogénszint változásának van döntő szerepe a kezelésben.
1.
2.
3.
4.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről5.
1.
2.
Klinikai Onkológia
Hasnyálmirigyrák: az ESMO klinikai gyakorlati irányelve a diagnózishoz, kezeléshez, követéshez*3.
Klinikai Onkológia
Gyógyszerbiztonsági szemelvények – a múlt tanulságai és a jövő lehetőségei4.
5.