Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 73
A (K)RAS-mutáció molekuláris epidemiológiája emberi daganatokban
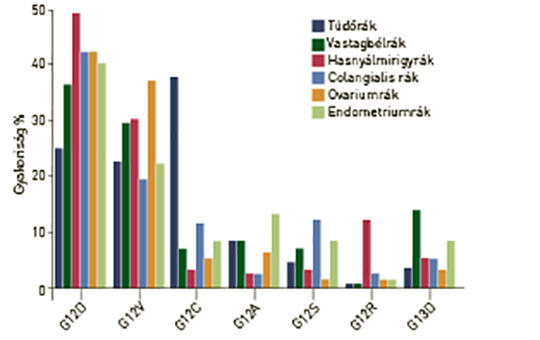
A RAS onkogén mutációja a leggyakoribb génhiba emberi daganatokban, és a három családtag közül a K-RAS-é a leggyakoribb, amit az N-RAS követ. A tipikus K-RAS-mutáns daganatok a hasnyálmirigyrák, vastagbélrák és tüdő-adenocarcinoma, amelyekben a mutáns variáns allélok gyakorisága igen heterogén, aminek hátterében eltérő karcinogenezis áll. A RAS-mutáns daganatok genetikai sokszínűségét tovább fokozza, hogy a mutáns allél homo- vagy heterozigóta formában van-e jelen. A sokszínűség egy másik forrása az, hogy a különféle daganatokban a K-RAS-mutánsok esetében sajátos kísérő mutációs mintázatú altípusok lehetnek. Mindezeknek az a következménye, hogy a K-RAS-mutáns daganatok biológiai viselkedése és nagy valószínűséggel terápiás érzékenysége is nagyon heterogén lehet. A K-RAS-inhibitorok klinikai debütálásával ezeknek a kérdéseknek egyre nagyobb jelentősége lesz.
miRNS-alapú terápiák idegrendszeri betegségekben: lehetőségek és kihívások
22 évvel azután, hogy kiderült: bármely gén elcsendesíthető, tucatnyi klinikai vizsgálat elemzi a miRNS-mimetikumok és -inhibitorok terápiás hatását. A módszert az idegrendszeri betegségek közül a neurodegeneratív kórképek, az epilepszia, az agytumorok és a cerebrális ischaemia kezelésében vizsgálják.
Diabetesgyógyszerek és Parkinson-kockázat
A Parkinson-kór incidenciája az átlaglakosságban 0,3%, azonban az előrejelzések szerint a következő 7 évben 18%-os kockázatnövekedésre számíthatunk, többek között ezért is nő a szakmai érdeklődés a glükózkontroll és a neurodegeneratív betegségek közötti lehetséges kapcsolat iránt.
[Myasthenia gravis-betegek autonóm rendellenességeinek elektrofiziológiás vizsgálata: prospektív tanulmány]
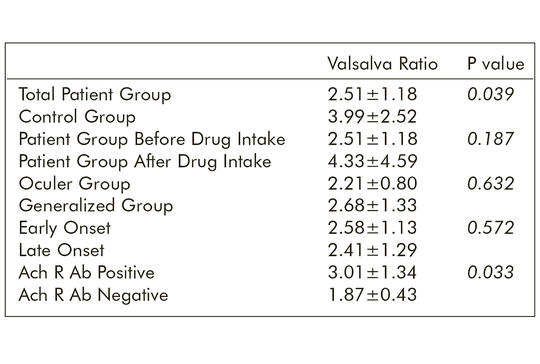
[A myasthenia gravis (MG) a neuromuscularis junctio autoimmun típusú megbetegedése. Az autonóm rendellenességeket nem gyakran társítják myasthenia gravishoz. A vizsgálat célja az volt, hogy megállapítsuk, milyen autonóm működés jellemzi az MG-betegek különböző alcsoportjait, és megvizsgáljuk az acetilkolinészteráz-inhibitorok hatásait. A vizsgálatba 30 autoimmun MG-beteget és 30 egészséges önkéntest vontunk be. Az autonóm működés tesztelése érdekében szimpatikus bőrreakció (SSR) és R-R intervallumvariáció analízis (RRIV) vizsgálatokat végeztünk. Az acetilkolinészteráz-inhibitor-kezelésben részesülő betegek körében kétszer végeztük el a vizsgálatokat. Az RRIV hiperventiláció alatti növekedése nagyobb (p = 0,006) és a Valsalva-arány alacsonyabb (p = 0,039) volt a kontrollcsoport tagjainál. Az SSR-amplitúdók alacsonyabbak voltak a gyógyszer bevétele után (p = 0,030). A gyógyszer bevétele után eltelt idő növekedésével megnyúlt SSR-látenciákat kaptunk (p = 0,043). A Valsalva-arány alacsonyabb volt az AchR antitestre negatív csoportban (p = 0,033). Mind az okuláris, mind a generalizált MG-betegek körében szubklinikus paraszimpatikus rendellenesség mutatható ki, különösen az AchR antitestre negatív csoportban. A piridostigmin perifériás szimpatikus kolinerg nonkumulatív hatással rendelkezik.]
A petefészekrák kezelésének frontvonalában: a PARP-gátlók szerepének megújítása
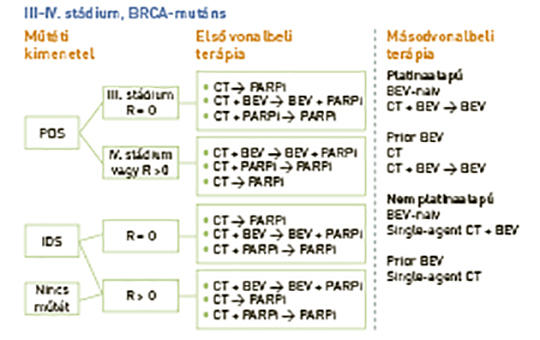
Kiújult petefészekrákban a poli(ADP-ribóz)polimeráz- (PARP-) gátlókkal történő kezelések megváltoztatták a platinaérzékeny daganatok kezelését. Az új adatok szerint a PARP-gátlókat a kezelési algoritmus korábbi szakaszában kell alkalmazni. A kutatók számba veszik azokat a fázis III vizsgálatokat, amelyekben a PARP-gátlók hatását értékelték újonnan diagnosztizált petefészekrákok primer, illetve fenntartó kezelésében. Megvitatják a gyógyszerek hatásosságát és biztonságosságát az összes daganat, illetve a biomarkerek szerint válogatott daganatok klinikai vizsgálataiban, és összevetik a különböző vizsgálatok előnyeit és korlátait. Fontolóra veszik a jövő kutatásainak prioritásait – különös tekintettel a betegek kiválasztására és a jövőben alkalmazandó, egyelőre hiányzó gyógyszeres regimenek megalkotására. Négy fázis III vizsgálatban (SOLO-1, PAOLA-1/ENGOT-OV25, PRIMA/ENGOT-OV26 és VELIA/GOG-3005) PARP-gátlók használatával (olaparib, niraparib vagy veliparib) a progressziómentes túlélés jelentős javulását figyelték meg petefészekrákos betegekben. A vizsgálatok eltérő kialakítása (kezelés vagy fenntartó kezelés, egy gyógyszeres vagy kombinációs kezelés, bevacizumabbal vagy bevacizumab nélkül), a betegek kiválasztása (műtéti eredmény, biomarkerek elérhetősége, prognózis szerint), a résztvevők eredeti megválasztása (intention-to-treat, BRCA-mutációs vagy homológ rekombinációdeficites pozitív) befolyásolták a vizsgálatokból levonható következtetéseket. A teljes túlélési adatok még függőben vannak, hosszú távú biztonságossági adatok is csak korlátozottan állnak rendelkezésre. A PARP-gátlók sarkalatos szerepet játszanak az újonnan kimutatott petefészekrák-ellátásban, és befolyásolják a további kezeléseket. Ki kell választani azokat a betegeket és gyógyszereket, akiknél az eddigi alkalmazott kezelések a PARP-gátlóknál kevesebb haszonnal járnának.
A méh rosszindulatú daganatainak korszerű onkológiai kezelése
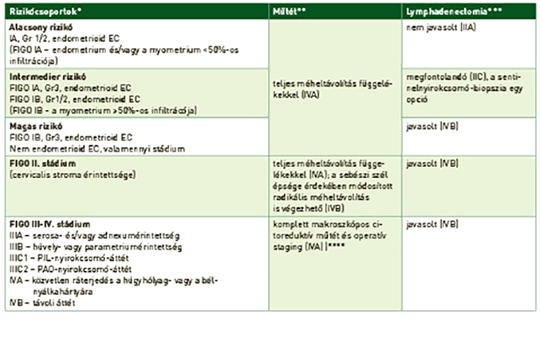
Világviszonylatban évente közel 400 000 nőnél igazolódik méhtestrák, amely 2018-ban körülbelül 90 000 nő halálát okozta. Az esetek túlnyomó részét a méhnyálkahártya hormonérzékeny hámjából kiinduló endometriumcarcinomák (EC) alkotják. A sarcomák a méhtestrákok alig 3%-át adják. Az EC-k 80-85%-a jó prognózisú, mivel alacsony gradusú és korai stádiumban kerül felismerésre, amikor a műtét és az esetleges posztoperatív kezelés révén a gyógyulás reális terápiás cél. Az előrehaladott stádiumban diagnosztizált EC és a nem endometrioid altípusok esetén a prognózis lényegesen rosszabb. A magas rizikójú EC optimális adjuváns kezelésére irányuló vizsgálatok egy része még folyamatban van, illetve a bővülő molekuláris ismeretek újabb vizsgálatokat generálnak. A méhtestsarcomák esetében is a sebészi eltávolítás jelenthet kuratív megoldást, az adjuváns kezelésre vonatkozó evidenciák bizonytalanok, egyéni mérlegelést igényelnek. A modern onkoterápia érájában már nemcsak a betegségmentes élet meghosszabbítására, hanem az élet minőségének minél teljesebb megőrzésére is törekszünk. A nőgyógyászati onkológiában ezt jelenti a fertilitás vagy a funkcionáló ováriumok lehetőség szerinti megőrzése; a magas morbiditással járó szisztémás lymphadenectomia indikációs körének szűkítése; a kedvezőbb mellékhatásprofilú brachytherapia alkalmazása a teljes kismedencei besugárzás helyett. A modern onkoterápia az úgynevezett biológiai kezelések által az előrehaladott betegségek ellátásának is a részévé vált: kemoterápia mellett/után progrediáló esetekben a pembrolizumab az EC és a sarcomák esetén is alkalmazható mikroszatellita-instabilitás vagy magas tumormutációs terheltség esetén, míg az NTRK fúziós gén jelenlétében larotrectinib vagy entrectinib mint célzott tirozinkináz-gátlók javasolhatók. Az EC-k 70-80%-át kitevő mikroszatellita-stabil esetekben (nem endometrioid altípusokban is!) a pembrolizumab lenvatinibbel kombinációban adható a kemoterápia után. Az EC területén gyarapodnak továbbá az egyéb célzott terápiás szerekkel szerzett tapasztalatok is (anti-HER2 serosus carcinomában, mTOR-gátló kezelés, endokrin terápia, más immun checkpoint inhibitorok, tirozinkináz-gátlók, PARP-gátlók és kombinációs kezelések). A jelen munka a méhtestrákok onkoterápiájáról kíván rövid összefoglalást nyújtani az aktuális szakmai ajánlások és a folyamatban lévő vizsgálatok bemutatásával.
A RAAS-gátlók pozitív hatása COVID-19-betegek körében
A metaanalízis célja annak megállapítása volt, hogy milyen hatással bírnak a hipertenzív, illetve bármely egyéb okból RAAS-gátlót szedő COVID-19-betegek morbiditására és mortalitására a SARS-CoV-2 vírus sejtbe lépését esetlegesen befolyásoló szerek.
Petefészekrákban szenvedő betegek nem sebészi kezelése
A petefészekrákban szenvedő betegek kezelésében alapvető a kellően radikális műtét, amely az egyéb módszerek eredményességét is meghatározza. Az ezt követően, egy ülésben végzett hyperthermiás intraperitonealis kemoterápia 40,5–42,5 Celsius-fokos citosztatikus oldat perfúziójával történik. A szisztémás kezelések megválasztásában a hat hónapos progressziómentesség a mérföldkő, ezentúl platinaszenzitív, ezen belül -refrakter vagy -rezisztens betegségről van szó. A citosztatikus kezelés fejlődése az alkilálószerektől a platinaszármazékokon át a paklitaxel alkalmazásáig terjed, különféle kombinációkkal, egyre jobb eredményekkel és mind kevesebb mellékhatással. A célzott terápiában az érújdonképződés-gátlók (főleg a bevacizumab) és a DNS-hibák javítását megakadályozó, PARP-gátlók a legjelentősebbek; ez utóbbiak esetében általában a platinaérzékenység feltétel, míg a BRCA-mutáció már nem mindig követelmény. Az utóbbi időben az immunterápiával kapcsolatban is ígéretes vizsgálatok folynak. A hormonkezelés fő előnye a jó tolerálhatóság. A gyógyszerek alkalmazásának sikerei mellett visszaszorulni látszik a sugárterápia, pedig a teljes peritonealis felszín ellátása – különösen a korszerű besugárzási technikák alkalmazása mellett – a kemoterápia alternatívája lehet, a palliatív irradiáció pedig a tünetek csökkentése mellett a gyógyszermentes időszakot is megnyújthatja, s a kombinálás lehetőségei további távlatokat nyitnak meg.
Hogyan befolyásolja a BRCA-státusz az emlőrák ellátását 2019-ben?
A germinalis BRCA-státusz korai vagy előrehaladott/áttétes emlőrákban egyaránt befolyásolja az ellátás menetét. Így ideális esetben a beteg informáltan dönthet a műtét típusáról, a sugárkezelés elkerüléséről; a BRCA-státusz a legújabb eredmények alapján befolyásolja a neoadjuváns, adjuváns, palliatív kemoterápia megválasztását, továbbá új, hatékony célzott (target) terápia alkalmazását vetheti fel. Specifikus terápiának számítanak a DNS-támadáspontú citosztatikumok, mindenekelőtt a platinakészítmények és a szintetikus letalitás elve alapján ható PARP-inhibitorok. E speciális gyógyszercsoportok optimális helye és sorrendje egyelőre nem ismert. A nemzetközi ajánlások valamennyi HER2-negatív (NCCN) vagy legalább a mutatók alapján valószínű BRCA-mutációt hordozó (ESMO) előrehaladott/áttétes emlőrákos esetben sürgetik a BRCA-státusz-vizsgálatot a megfelelő terápiás stratégia meghatározása érdekében. Az elmúlt időszakban a BRCA-státusz meghatározására szolgáló módszerek óriási fejlődésen mentek át, és egyre szélesebb körben elérhetőek különféle szolgáltatók kínálatában. A mutáció azonosításához a teljes gének szekvenálása szükséges, amelyre a korábbi módszereknél gyorsabb és költséghatékonyabb megoldást nyújt az új generációs szekvenálóplatformok (next generation sequencing - NGS) alkalmazása. A kezelőorvos felelőssége, hogy amennyiben a részletes családi anamnézis, a beteg életkora, esetleges megelőző daganatos betegsége és nem utolsósorban a daganatjellemzők alapján felmerül, gondoljon patogén BRCA-mutáció jelenlétére, mérlegelje a teszt indokoltságát, illetve vesse fel a beteg számára a lehetőséget.
A relabáló epithelialis petefészekrákok kezelése
A petefészekrák a leggyakoribb nőgyógyászati daganat okozta halálozási ok, és a legtöbb betegség előrehaladott FIGO stádiumban kerül diagnosztizálásra. Az iniciális debulking műtét és az első vonalbeli paclitaxel/carboplatin kombinációs kemoterápia alkalmazásának ellenére, a betegek közel kétharmada relabál az első három évben. A petefészekrák kezelésére irányuló kutatások az utóbbi években elsősorban a fenntartó kezelésekre irányultak, a betegek progressziómentes időszakainak hoszszabbítása céljából. A relapszusok molekuláris biológiájának egyre jobb megértése az angiogenezis-gátló bevacizumab és kemoterápiák kombinációinak bevezetéséhez vezetett, melyek az iniciális, a fenntartó és a relabáló (platinaszenzitív és platinarezisztens) daganatok esetében egyaránt hatásosnak bizonyultak. Az utóbbi időben egy új fenntartó kezelés került alkalmazásra a mindennapi klinikai rutinban, a PARP-gátló olaparib monoterápia, mely a platinaszenzitív, relabáló, magas grádusú szerózus petefészekrákok kezelésében bizonyult hatásosnak. Az új terápiák bevezetésének ellenére azonban még számos tisztázatlan kérdés van a relabáló epithelialis petefészekrákok kezelésében. Jelen áttekintés célja a kiújuló, progrediáló petefészekrákok terápiás lehetőségeinek összefoglalása az evidenciák és az új terápiás modalitások tükrében.
1.
2.
3.
4.
5.
1.
Egészségpolitika
A Magyar Járóbeteg Szakellátási Szövetség állásfoglalása az ágazat helyzetéről2.
Gondolat
Üdv nálunk! Van már, aki írja a fekete pontjaid? – Nyomasztás a közoktatásban3.
4.
5.