Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 606
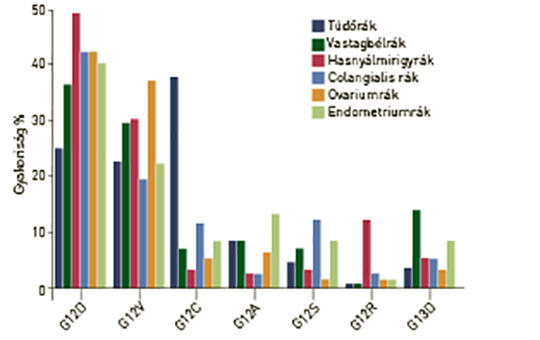
A (K)RAS-mutáció molekuláris epidemiológiája emberi daganatokban
A RAS onkogén mutációja a leggyakoribb génhiba emberi daganatokban, és a három családtag közül a K-RAS-é a leggyakoribb, amit az N-RAS követ. A tipikus K-RAS-mutáns daganatok a hasnyálmirigyrák, vastagbélrák és tüdő-adenocarcinoma, amelyekben a mutáns variáns allélok gyakorisága igen heterogén, aminek hátterében eltérő karcinogenezis áll. A RAS-mutáns daganatok genetikai sokszínűségét tovább fokozza, hogy a mutáns allél homo- vagy heterozigóta formában van-e jelen. A sokszínűség egy másik forrása az, hogy a különféle daganatokban a K-RAS-mutánsok esetében sajátos kísérő mutációs mintázatú altípusok lehetnek. Mindezeknek az a következménye, hogy a K-RAS-mutáns daganatok biológiai viselkedése és nagy valószínűséggel terápiás érzékenysége is nagyon heterogén lehet. A K-RAS-inhibitorok klinikai debütálásával ezeknek a kérdéseknek egyre nagyobb jelentősége lesz.
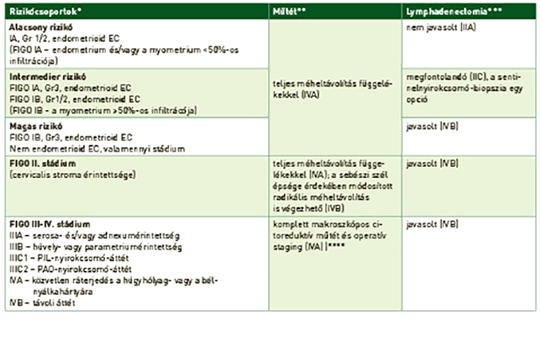
A méh rosszindulatú daganatainak korszerű onkológiai kezelése
Világviszonylatban évente közel 400 000 nőnél igazolódik méhtestrák, amely 2018-ban körülbelül 90 000 nő halálát okozta. Az esetek túlnyomó részét a méhnyálkahártya hormonérzékeny hámjából kiinduló endometriumcarcinomák (EC) alkotják. A sarcomák a méhtestrákok alig 3%-át adják. Az EC-k 80-85%-a jó prognózisú, mivel alacsony gradusú és korai stádiumban kerül felismerésre, amikor a műtét és az esetleges posztoperatív kezelés révén a gyógyulás reális terápiás cél. Az előrehaladott stádiumban diagnosztizált EC és a nem endometrioid altípusok esetén a prognózis lényegesen rosszabb. A magas rizikójú EC optimális adjuváns kezelésére irányuló vizsgálatok egy része még folyamatban van, illetve a bővülő molekuláris ismeretek újabb vizsgálatokat generálnak. A méhtestsarcomák esetében is a sebészi eltávolítás jelenthet kuratív megoldást, az adjuváns kezelésre vonatkozó evidenciák bizonytalanok, egyéni mérlegelést igényelnek. A modern onkoterápia érájában már nemcsak a betegségmentes élet meghosszabbítására, hanem az élet minőségének minél teljesebb megőrzésére is törekszünk. A nőgyógyászati onkológiában ezt jelenti a fertilitás vagy a funkcionáló ováriumok lehetőség szerinti megőrzése; a magas morbiditással járó szisztémás lymphadenectomia indikációs körének szűkítése; a kedvezőbb mellékhatásprofilú brachytherapia alkalmazása a teljes kismedencei besugárzás helyett. A modern onkoterápia az úgynevezett biológiai kezelések által az előrehaladott betegségek ellátásának is a részévé vált: kemoterápia mellett/után progrediáló esetekben a pembrolizumab az EC és a sarcomák esetén is alkalmazható mikroszatellita-instabilitás vagy magas tumormutációs terheltség esetén, míg az NTRK fúziós gén jelenlétében larotrectinib vagy entrectinib mint célzott tirozinkináz-gátlók javasolhatók. Az EC-k 70-80%-át kitevő mikroszatellita-stabil esetekben (nem endometrioid altípusokban is!) a pembrolizumab lenvatinibbel kombinációban adható a kemoterápia után. Az EC területén gyarapodnak továbbá az egyéb célzott terápiás szerekkel szerzett tapasztalatok is (anti-HER2 serosus carcinomában, mTOR-gátló kezelés, endokrin terápia, más immun checkpoint inhibitorok, tirozinkináz-gátlók, PARP-gátlók és kombinációs kezelések). A jelen munka a méhtestrákok onkoterápiájáról kíván rövid összefoglalást nyújtani az aktuális szakmai ajánlások és a folyamatban lévő vizsgálatok bemutatásával.
Az immunválasz néhány újonnan felismert hatásmechanizmusa és az immunológia szemléleti átalakulása
Az immunológia az egészséges és kóros immunválaszt tanulmányozó komplex tudomány. Ez az élettani, patofiziológiai tudományág az egyes mechanizmusok megértését elsősorban sejt- és molekuláris biológiai, genetikai, epigenetikai és (neuro)endokrinológiai megközelítéssel, illetve a patológiás folyamatok részleteinek feltárásával végzi. Az immunológia egyike a nagyon gyorsan fejlődő tudományoknak, eredményei visszahatnak más diszciplínákra is elméleti (például hálózattudományok, rendszer-biológia) és módszertani (monoklonális ellenanyagok, biomarkerek, immunoassay-ek) szinten egyaránt. Az immunológusok az elmúlt évtizedekben számos szemléleti változást értek meg, és sok, a hatásmechanizmusokban megnyilvánuló lényegi részletkérdés érvényesülését ismerték fel.
[Heveny vestibularis szindróma képében jelentkező késői meningitis carcinomatosa – klinikopatológiai esetismertetés]
[Célkitűzés – Bár a szédülés a leggyakrabban előforduló panaszok egyike, a vestibularis perifériák hirtelen kialakult tónusaszimmetriája hátterében mégis ritkán találunk perifériás eredetű betegséget utánzó malignus koponyaűri tumorokat. Dolgozatunk egy heveny vestibularis szindróma klinikai képében jelentkező, késői, temporalis csontot is beszűrő, disszeminált, generalizált mikrometasztázisokkal járó meningitis carcinomatosa esetet mutat be, ami egy primer pecsétgyűrűsejtes gyomorcarcinoma felébredését követően jelent meg. Kérdésfelvetés – Célul tűztük ki, hogy azonosítjuk azon patofiziológiai folyamatokat, melyek magyarázatul szolgálhatnak a daganat felébredésére, disszeminációjára. A vestibularis tónusaszimmetria lehetséges okait szintén vizsgáltuk. Ötvenhat éves férfi betegünk interdiszciplináris orvosi adatait retrospektíven elemeztük. Összegyűjtöttük és részletesen újraértékeltük az eredeti klinikai és patológiai vizsgálatok leleteit, majd új szövettani festésekkel és immunhisztokémiai módszerekkel egészítettük ki a diagnosztikus eljárásokat. Kórboncolás során a nagyagy és a kisagy oedamás volt. A bal piramiscsont csúcsát egy 2 × 2 cm nagyságú daganatmassza szűrte be. A gyomorreszekátum eredeti szövettani metszeteinek újraértékelése submucosus daganatinfiltrációt igazolt vascularis invázió jeleivel. Immunhisztokémiai vizsgálatokkal dominálóan magányosan infiltráló daganatsejteket láttunk cytokeratin 7- és vimentinpozitivitással, valamint részleges E-kadherin szövettani festésvesztéssel. A kórboncolás során nyert szövetminták ezt követő hisztológiai vizsgálatai igazolták a disszeminált, többszervi mikroszkopikus daganatinváziót. Az újabb eredmények igazolták, hogy a vimentin kifejeződése, valamint az E-kadherin elvesztése szignifikáns (p < 0,05) kapcsolatot mutat az előrehaladott stádiummal, a nyirokcsomóáttétek jelenlétével, a vascularis és neuralis invázióval, valamint a nem differenciált szöveti típussal. Betegünk középkorú volt és nem volt immunhiányos állapotban, így a gyomorcarcinoma kilenc éven át tartó alvó állapotot követő felébredését nem tudtuk megmagyarázni. A daganat szervspecifikus tropizmusa, melyet a „seed and soil” teóriával magyaráznánk, kifejezetten váratlan volt, mivel a gyomorrákok ritkán képeznek áttétet az agyburkokon, hiszen a daganatsejtek elenyésző számban jutnak át a vér-agy gáton. Következtetések – Az előzményben szereplő malignus folyamat, valamint egy új neurológiai tünet megjelenése fel kell, hogy keltse a klinikus figyelmét a központi idegrendszer daganatos érintettségére, melyet adekvát, célzott diagnosztikus és terápiás stratégia megtervezése kell, hogy kövessen. Ehhez célzott szövettani festési eljárások, specifikus antitestek alkalmazása szükséges. A közelmúlt eredményei sejtkultúrákon igazolták a metformin epithelialis-mesenchymalis transitiót erősen gátló hatását gyomorrák esetében. Így további kutatást kell végezni azon esetekben, amelyekben az epithelialis-mesenchymalis transitióra pozitív eredményeket kapunk.]
A citokinek fájdalomkeltő szerepe a központi idegrendszerben – az anticitokin-terápia közvetlen analgetikus hatása
A krónikus fájdalom érzékelésében, továbbításában, feldolgozásában és az agyi fájdalomkép megformálásában nociceptiv, neuropathiás és centrális mechanizmusok vesznek részt. A kórokozó jelenlétét vagy a szövetkárosodást jelző és a védekezést riadóztató molekulák, az alarminok kóros folyamatok sorát indítják el, amelyek gyulladásos fájdalomingert váltanak ki. A gyulladáskeltő citokineknek a fájdalom idegrendszeri szinten való megjelenítésében van döntő szerepe. A folyamatos gyulladásos ingerek az idegsejtek perifériás és központi érzékenyítésével aktiválják a fájdalomérzéssel kapcsolatos agyi területeket és kialakítják az összetett fájdalomképet, a fájdalommátrixot. Az agyi funkcionális kapcsolatok hálózatokban működnek és funkcionális MRI-vel képezhetők le. A citokinek a neuronokat közvetlenül, vagy más neuromediátorok révén közvetve aktiválják. A citokinreceptorok megjelennek a nociceptorokon és a magasabb rendű neuronokon is, valamint a különféle nem neuralis sejteken, mint a microglia vagy az astrocyták. Az idegrendszerben szinte mindenütt fellelhető citokinek a tumornekrózis-faktor és az interleukin 6. Jeladási útvonalaik a nukleáris faktor κB és a Janus-kináz enzimrendszere. Ezért a gyulladáskeltő citokinek és a Janus-kináz elsőrendű terápiás célpontok. Az anticitokin biologikumok és a kismolekulájú kinázgátlók rheumatoid arthritisben csökkentik a fájdalmat és javítják a működőképességet. A fájdalomcsökkenés nagyobb, mint ami csak a gyulladás klinikai biomarkereinek csökkenésétől várható lenne. A célzott biológiai és kémiai-biológiai válaszmódosítók korai és gyors fájdalomcsökkentő hatását az agyban kifejtett közvetlen analgetikus hatásnak tulajdonítják.
A fej-nyaki daganatok komplex kezelése – áttekintés
A fej-nyaki laphámsejtes daganatok (head and neck squamous cell carcinoma – HNSCC) kezelése rendkívül komplex feladat, amely megkívánja a fej-nyak sebész, sugárterápiás szakember és klinikai onkológus szoros együttműködését. Elsődleges célnak a jó tumorkontrollt kell tekintenünk, de a terápia megválasztásánál szem előtt kell tartanunk az onkológiai radikalitás mellett az elfogadható életminőséget, ismervén, hogy a legtöbb lokális terápia nagyban befolyásolja a betegek légzés-, nyelés- és/vagy beszédfunkcióját. A megfelelő diagnosztikus vizsgálatok alapján a betegséget besorolhatjuk korai stádiumba, lokálisan/regionálisan előrehaladott stádiumba, illetve távoli áttétes és/vagy kiújult stádiumba. Kategóriánként eltérő terápiás modalitások jönnek szóba, amelyeket tovább bonyolít a primer tumor, az áttétek elhelyezkedése, a beteg állapota, társbetegségei, a daganat biológiai viselkedése. Jelen áttekintő közleményben a szerzők összefoglalják a fej-nyaki laphámrákok terápiájának alapelveit.
A hypoxia jelentősége a rosszindulatú daganatok progressziójában: terápiás lehetőségek, út a Nobel-díjhoz
Az elmúlt évtizedek kutatásai világossá tették, hogy a malignus daganatok egyik meghatározó jellemzője hypoxiás állapotuk és az ennek következtében aktiválódó genetikai, biokémiai és biológiai programok. A felismerés jelentőségét mi sem bizonyítja jobban, mint hogy 2019-ben az orvosi Nobel- díjat ezért ítélték oda a terület meghatározó tudósainak. A daganatszövetben keletkező hypoxia fő oka a proliferációval lépést nem tartó ereződés, de másik fontos oka a daganatos beteg szisztémás hypoxiája is. A hypoxiára adandó sejtes válaszok alapja a hypoxia indukálta (transzkripciós) faktorok stabilizálódása és aktivizálódása, ami azonban daganatokban az onkogén jelpályák konstitutív aktivitása miatt is bekövetkezhet hypoxia nélkül is. A daganatos hypoxia következménye az angiogén fenotípus, a sejtmetabolizmus átprogramozódása és a daganatellenes immunológiai válaszreakciók kedvezőtlen modulációja. A daganatszövet hypoxiája azonban negatívan befolyásolja a kemo-, sugár- és immunterápia hatékonyságát is. Mindezek miatt nagy szükség lenne a daganatos hypoxia célzott terápiájára, aminek első eszközei még csak most lépnek be a klinikai gyakorlatba. Fontos megjegyezni, hogy hazai kutatócsoportok nemzetközileg is elismert eredményekkel járultak hozzá ismereteink bővüléséhez ezen a területen.
A bél-agy-tengely újabb összefüggései
Gyulladásos bélbetegség esetén több mint duplájára nő a demencia kockázata; IBD-ben szenvedőknél 7 évvel korábban kezdődik az elbutulás.
Több mint 30 koronavírus elleni kutatási projektben vesz részt a Szegedi Tudományegyetem
Két hónap alatt harmincnál is több orvos- és élettudományi projektet kezdeményeztek a Szegedi Tudományegyetemen a koronavírussal kapcsolatban. Az SZTE részt vesz egy ígéretes antivirális szer klinikai vizsgálatának előkészítésében, emellett az intézmény átfogó genetikai kutatást indított és tömeges szűrési módszerek fejlesztésében is közreműködik. A kutatások a betegség minden szakaszára kiterjednek, kezdve a megelőzéstől és a diagnosztikától a korai és intenzív terápiákon át egészen a rehabilitációig.
Egy biosimilar gyógyszer kifejlesztése és tízéves története a binocrit® példáján keresztül
A szabadalmak lejárata számos biológiai termék esetén alternatív változatok kifejlesztésére sarkallta a gyógyszergyárakat. Ezeket a változatokat „biosimilar” termékeknek nevezzük, amelyek minősége, biztonságossága, hatásossága a már engedélyezett (licenccel rendelkező) gyógyszerekéhez hasonló (amely utóbbiakat referenciagyógyszereknek is szokás nevezni). Az onkológiában megjelent első biosimilar gyógyszerek az alapkezelések mellé társuló szupportív kezelések gyógyszerei voltak, mint például a filgrasztim vagy az epoetin. A Binocrit® (HX575) az epoetin-alfa biosimilar változata, amelyet az onkológiában a kemoterápia által indukált anaemia (CIA) kezelésére használnak. A Binocrit® biosimilarként való kifejlesztésének és engedélyeztetésének folyamata során először kiterjedt analitikai összehasonlításokat végeztek a referencia epoetin-alfával. Ezután következett a klinikai fejlesztés: a fázis I farmakokinetikai/farmakodinamikai vizsgálatok során igazolták az új szer és a referencia-gyógyszer közötti bioekvivalenciát, majd egy fázis III vizsgálatban bizonyították a CIA-ban való terápiás hatásosságot is. Törzskönyvezése óta a Binokrit® ma már kiterjedten használatos a mindennapi klinikai gyakorlatban. Már sok-sok adattal igazolható, hogy a Binocrit® segítségével a daganatos betegek kezelése során kialakuló CIA hatásos és jól tolerálható lehet.
1.
2.
3.
4.
5.
Egészségpolitika
Hadiállapotként kezeli és így is reagál a kormány az egészségügy „rendezésére”1.
Helyünk a világban
A felzárkózás kudarca – 5+1 súlyos megállapítás Orosz Éva tanulmányából2.
3.
Idegtudományok
Neurofeedback: az ADHD-val küzdő gyerekek fejlesztéséhez is használható módszert oktatnak Vácon4.
5.
Orvoslás és társadalom
Országos férfiegészség-kampány és PSA-szűrés indul a prosztatarák ellen