Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Klinikai Onkológia - 2020;7(4)
Tartalom
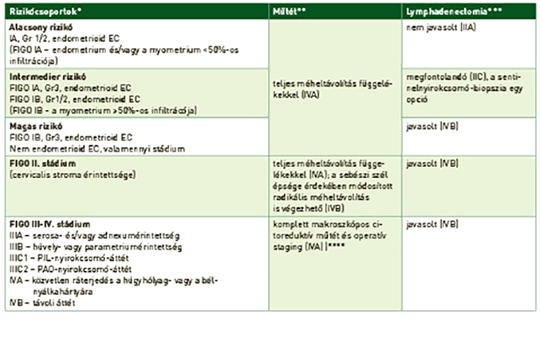
A méh rosszindulatú daganatainak korszerű onkológiai kezelése
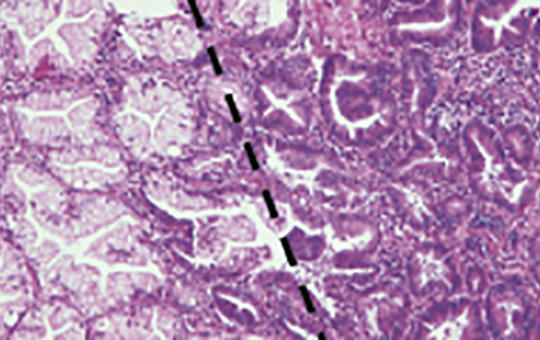
Világviszonylatban évente közel 400 000 nőnél igazolódik méhtestrák, amely 2018-ban körülbelül 90 000 nő halálát okozta. Az esetek túlnyomó részét a méhnyálkahártya hormonérzékeny hámjából kiinduló endometriumcarcinomák (EC) alkotják. A sarcomák a méhtestrákok alig 3%-át adják. Az EC-k 80-85%-a jó prognózisú, mivel alacsony gradusú és korai stádiumban kerül felismerésre, amikor a műtét és az esetleges posztoperatív kezelés révén a gyógyulás reális terápiás cél. Az előrehaladott stádiumban diagnosztizált EC és a nem endometrioid altípusok esetén a prognózis lényegesen rosszabb. A magas rizikójú EC optimális adjuváns kezelésére irányuló vizsgálatok egy része még folyamatban van, illetve a bővülő molekuláris ismeretek újabb vizsgálatokat generálnak. A méhtestsarcomák esetében is a sebészi eltávolítás jelenthet kuratív megoldást, az adjuváns kezelésre vonatkozó evidenciák bizonytalanok, egyéni mérlegelést igényelnek. A modern onkoterápia érájában már nemcsak a betegségmentes élet meghosszabbítására, hanem az élet minőségének minél teljesebb megőrzésére is törekszünk. A nőgyógyászati onkológiában ezt jelenti a fertilitás vagy a funkcionáló ováriumok lehetőség szerinti megőrzése; a magas morbiditással járó szisztémás lymphadenectomia indikációs körének szűkítése; a kedvezőbb mellékhatásprofilú brachytherapia alkalmazása a teljes kismedencei besugárzás helyett. A modern onkoterápia az úgynevezett biológiai kezelések által az előrehaladott betegségek ellátásának is a részévé vált: kemoterápia mellett/után progrediáló esetekben a pembrolizumab az EC és a sarcomák esetén is alkalmazható mikroszatellita-instabilitás vagy magas tumormutációs terheltség esetén, míg az NTRK fúziós gén jelenlétében larotrectinib vagy entrectinib mint célzott tirozinkináz-gátlók javasolhatók. Az EC-k 70-80%-át kitevő mikroszatellita-stabil esetekben (nem endometrioid altípusokban is!) a pembrolizumab lenvatinibbel kombinációban adható a kemoterápia után. Az EC területén gyarapodnak továbbá az egyéb célzott terápiás szerekkel szerzett tapasztalatok is (anti-HER2 serosus carcinomában, mTOR-gátló kezelés, endokrin terápia, más immun checkpoint inhibitorok, tirozinkináz-gátlók, PARP-gátlók és kombinációs kezelések). A jelen munka a méhtestrákok onkoterápiájáról kíván rövid összefoglalást nyújtani az aktuális szakmai ajánlások és a folyamatban lévő vizsgálatok bemutatásával.
A 2020-as ESMO virtuális kongresszusának újdonságai
A 2020-as év mindannyiunk számára váratlan nehézségekkel indult. A SARS-CoV-2 járvány régen tapasztalt kihívás elé állította a világ egészségügyi rendszereit. Minden országban megfigyelhető az egészségügyi források átcsoportosítása, a betegek orvoshoz fordulási hajlandóságának járványügyi szempontok alapján való megváltozása. Az online medicina elmúlt időszakban tapasztalható térhódítása tovább gyorsult. Egyre inkább kirajzolódik, hogy az orvos-beteg találkozások mely része valósítható meg digitálisan és milyen esetben elengedhetetlen a személyes találkozás. Ilyen közegben rendezték meg idén, rendhagyó formában, az ESMO virtuális kongresszust, ahol az eredményeket és előadásokat online követhettük, a korábban megszokott több tízezres forgatag helyett. A legfontosabb vizsgálati eredmények, újdonságok összefoglalóját olvashatjuk az alábbiakban.
Agnosztikus terápia onkológiai alkalmazása
A tumoragnosztikus terápia az onkológiai kezelés ígéretes lehetősége, azonban a potenciális célpontok klasszifikálása, validálása, azok egységes módszerek szerinti kimutatása elengedhetetlen. A tumoragnosztikus kezelések engedélyezése új típusú, biomarker-vezérelt klinikai vizsgálatok bevezetését tette szükségessé. Jelenleg három tumoragnosztikus molekuláris célpont ismert: a daganatok magas fokú mikroszatellita-instabilitása (MSI-H), a neurotrop-tirozinkináz-receptor (NTKR) gének fúziója, valamint a daganatok magas tumormutációs terhelése (TMB-H). A pembrolizumab (anti-PD-1 antitest) az első tumoragnosztikus indikációban is törzskönyvezett gyógyszer, amelyet először MSI-H daganatok kezelésére engedélyeztek, majd később a magas TMB is bekerült az indikációk közé. Az NTKR-fúziót hordozó daganatok kezelésére a larotrectinib és az entrectinib került engedélyezésre.
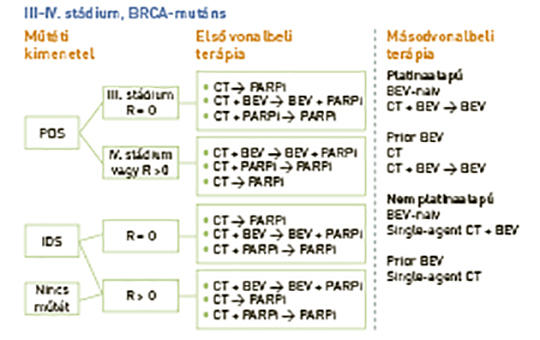
A petefészekrák kezelésének frontvonalában: a PARP-gátlók szerepének megújítása
Kiújult petefészekrákban a poli(ADP-ribóz)polimeráz- (PARP-) gátlókkal történő kezelések megváltoztatták a platinaérzékeny daganatok kezelését. Az új adatok szerint a PARP-gátlókat a kezelési algoritmus korábbi szakaszában kell alkalmazni. A kutatók számba veszik azokat a fázis III vizsgálatokat, amelyekben a PARP-gátlók hatását értékelték újonnan diagnosztizált petefészekrákok primer, illetve fenntartó kezelésében. Megvitatják a gyógyszerek hatásosságát és biztonságosságát az összes daganat, illetve a biomarkerek szerint válogatott daganatok klinikai vizsgálataiban, és összevetik a különböző vizsgálatok előnyeit és korlátait. Fontolóra veszik a jövő kutatásainak prioritásait – különös tekintettel a betegek kiválasztására és a jövőben alkalmazandó, egyelőre hiányzó gyógyszeres regimenek megalkotására. Négy fázis III vizsgálatban (SOLO-1, PAOLA-1/ENGOT-OV25, PRIMA/ENGOT-OV26 és VELIA/GOG-3005) PARP-gátlók használatával (olaparib, niraparib vagy veliparib) a progressziómentes túlélés jelentős javulását figyelték meg petefészekrákos betegekben. A vizsgálatok eltérő kialakítása (kezelés vagy fenntartó kezelés, egy gyógyszeres vagy kombinációs kezelés, bevacizumabbal vagy bevacizumab nélkül), a betegek kiválasztása (műtéti eredmény, biomarkerek elérhetősége, prognózis szerint), a résztvevők eredeti megválasztása (intention-to-treat, BRCA-mutációs vagy homológ rekombinációdeficites pozitív) befolyásolták a vizsgálatokból levonható következtetéseket. A teljes túlélési adatok még függőben vannak, hosszú távú biztonságossági adatok is csak korlátozottan állnak rendelkezésre. A PARP-gátlók sarkalatos szerepet játszanak az újonnan kimutatott petefészekrák-ellátásban, és befolyásolják a további kezeléseket. Ki kell választani azokat a betegeket és gyógyszereket, akiknél az eddigi alkalmazott kezelések a PARP-gátlóknál kevesebb haszonnal járnának.
Heterogenitás és a daganatok
A sejtek alapvető feladata, hogy fenntartsák az egyensúlyt a proliferáció és a programozott sejthalál között, amely lehetőséget ad a sejt számára, hogy specifikus feladatát végrehajtsa. Ez a folyamat szorosan összekapcsolódik a szomszédos sejtekkel, továbbá a sejtek közötti állománnyal is. Mindezek szabályozásában hibák keletkezhetnek, persze leggyakrabban mutációk. Ezek némelyike a sejt életében zavarokat okozhat, azonban a mutációk többsége nem játszik fontos szerepet. Jól ismert a benignitás és a malignitás elkülönítése, amelyből a daganatsejtek metasztatizálása az igazi veszély. (Tulajdonképpen klinikailag akkor lehet malignusnak tekinteni egy daganatot, ha képes a metasztatizálásra.) Ez az említett hiba lehet veleszületett és szerzett, amellyel a normális klonális jelenlétet fokozatosan uniklonálissá változtatja (inkább a hematológiai tumorokban, mintsem a szolidokban), és ez a poliklonalitás összezavarja a sejt funkcionális képességét. Érthető tehát, hogy ezt a két jelenséget, a metasztatizálást és a szelekciót tekinthetjük a terápia első számú célpontjának. A heterogenitás fontos szerepet játszik a sejtek életében.
Hányáscsillapítás az onkológiai kezelések során
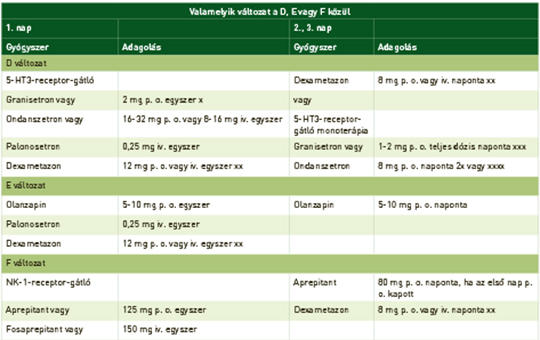
A hányinger és hányás egy többlépcsős folyamat, amely a központi idegrendszer irányítása alatt áll. A hányást kiváltó ingerek pszichés hatásra az agykéreg felől érkezhetnek vagy a nervus vaguson keresztül. A nyúltvelőben speciális magvak találhatók, amelyek a hányást kiváltják. Legfontosabb ingerületátvivő anyagok a szerotonin, a P-anyag és a dopaminok. A kemoterápiás szerek különböző arányban okoznak hányingert és hányást. Az 5-HT3- és NK-1-receptor-antagonisták a legjelentősebb hányinger-csillapítók. Szakmai ajánlások javasolják a gyógyszer-kombinációkat a különböző kemoterápiák okozta hányás csillapítására. A fix, szájon keresztül alkalmazható kombináció: netupitant és palonosetron (NEPA) növeli a betegek terápiahűségét. Az összefoglaló kitér a speciális hányingerek és hányások ismertetésére: áttöréses, többnapos kemoterápia okozta, sugárterápia során kialakult és a megelőlegezett hányásokra, valamint a gyermekkori hányáscsillapítás problematikájára is.
A CT-vizsgálatok mellékhatásai
A képalkotó radiológiai diagnosztikai eljárások körében egyre terjednek a viszonylag nagy dózisú sugárexpozíciót eredményező, de vitathatatlan diagnosztikus előnyt mutató komputertomográfiás (CT-) vizsgálatok. A sztochasztikus sugárhatások lineáris, küszöbdózis nélküli modellje alapján a legkisebb elszenvedett sugárdózis is kiválthatja daganatok keletkezését. A CT-vizsgálatok során elszenvedett sugárexpozíció miatt kialakuló daganatkeletkezés, magasabb sugárérzékenységük és várható hosszabb élettartamuk miatt, elsősorban a fiatal korosztályt érinti. A témakört vizsgáló legtöbb epidemiológiai tanulmány arra a következtetésre jutott, hogy a CT-vizsgálatok dózisfüggően megnövelik fiatalokban a leukémiák és agydaganatok kialakulásának a kockázatát. Az abszolút daganatszámok azonban nem jelentősek, így megfelelő indikáció esetén a vizsgálatot a lehető leghamarabb el kell végezni. Állapotos nőkön végzett, az alhasi régiót érintő CT-vizsgálatok fejlődési rendellenességek kialakulásához vezethetnek a magzatban. Az esetek túlnyomó többségében azonban csak sorozat-CT-vizsgálatok eredményezhetnek 100 mGy feletti magzati expozíciót, amely felvetheti a terhesség megszakítását. A sugárexpozícióval járó képalkotó vizsgálatok indokoltságáért, optimált elvégzéséért a kezelőorvos a felelős.
1.
2.
3.
4.
5.
1.
2.
Ideggyógyászati Szemle Proceedings
A Magyar Stroke Társaság XVIII. Kongresszusa és a Magyar Neuroszonológiai Társaság XV. Konferenciája. Absztraktfüzet3.
4.
5.
Egészségpolitika
A MOK és a MOSZ további lépéseket tesz a szakma és a biztonságos betegellátás érdekében