Az Alzheimer-kór mint szisztémás megbetegedés – amyloid-β metabolizmus a szervezetben
2017. OKTÓBER 24.
2017. OKTÓBER 24.
Szöveg nagyítása:
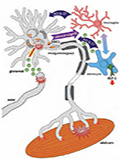
Az Alzheimer-kórral (AD) kapcsolatos kutatás tradicionálisan az agyra fókuszál, holott számos perifériás és szisztémás rendellenesség köthető a betegséghez, és napjainkban egyre nyilvánvalóbb, hogy ezek a rendellenességek hozzájárulnak a betegség progressziójához. Wang és munkatársainak áttekintő közleménye az AD egy fő jellegzetességére, az amyloid-β-ra (Aβ) fókuszál, számba veszi a szisztémás rendellenességek és az Aβ-metabolizmus összefüggéseit, és arra a következtetésre jut, hogy a szisztémás rendellenességek nem másodlagosan alakulnak ki, hanem alapvető szerepük van az AD progressziójában. Az AD szisztémás megközelítése lehetőséget adhat a jelenleg gyógyíthatatlan betegség megelőzésére, korai diagnózisára és terápiájára. Aβ-metabolizmus Az Aβ fiziológiás metabolizmusa nem csak az agyban, hanem a periférián is zajlik, az amyloid prekurzor protein (APP) nemcsak az agysejtekben fejeződik ki, de a perifériás szövetekben, így a mellékvesében, a vesében, szívben, májban, lépben, hasnyálmirigyben, vér- és endothelsejtekben is. A periférián létrejött Aβ az összmennyiség jelentős hányadát képezi, azonban az Aβ-koncentráció magasabb a központi idegrendszerben, mint a plazmában. Ez utóbbi magyarázhatja, hogy bár ritkán a perifériás szervekben (bőrben, bélben, szívben) is találhatók Aβ-aggregátumok, azok mégis leginkább az agyban rakódnak le. Az AD-esetek 99%-át adó sporadikus esetek kialakulásában fontos tényező az Aβ lebontásának és eltávolításának rendellenessége. Normális esetben az agyi Aβ 60%-a a perifériára kerül, ezért az Aβ perifériás eltávolításának hatékonysága nagyban befolyásolja az agy tisztulását. Mindazonáltal, kimutatták, hogy AD-ben az Aβ a perifériáról az agyba áramlik. Alzheimer-kór a periférián Pozitív visszacsatolás működik a periféria és az agy között: számos szisztémás rendellenesség felerősíti az AD progresszióját, majd az AD progressziója tovább rontja ezeket a szisztémás megbetegedéseket. Mivel az Aβ eltávolításában központi szerepet játszanak a perifériás mononukleáris fagociták, első helyen említendő az immunrendszer működészavara. Ebből a szempontból is különösen fontos, hogy a sporadikus AD kockázatát növelő gének a veleszületett immunitás fehérjéit kódolják. A vérben is kimutathatók különböző rendellenességek AD esetén: megnő a vérlemezkék APP-expressziója, csökken az Aβ-szállításban közreműködő albumin szintje, csökken a vörösvértestek Aβ-kötő képessége. A metabolikus betegségek közül a cukorbetegség esetén 1,4-2-szeresre nő az AD kockázata, az inzulinrezisztencia rontja a cirkuláló Aβ máj általi kiválasztását, a 2-es típusú diabéteszben szenvedők hasnyálmirigyében lerakódó, hibás térszerkezetű fehérje, az amylin az agyba bejutva felerősíti az Aβ-aggregációt. A cukorbetegség mellett a kóros lipidmetabolizmus is növeli az AD-rizikót; érdemes megjegyezni, hogy a többszörösen telítetlen zsírsav-fogyasztás pozitív hatással van az Alzheimer-kórosak kognitív funkciójára. A kardiovaszkuláris betegség a sporadikus AD gyakori kísérőbetegsége; AD-betegekben gyakori az intramiokardiális Aβ-lerakódás, ami hozzájárulhat a funkcióromláshoz. A cirkuláló Aβ-t elsődlegesen a máj távolítja el: egyrészt a májsejtek lebontják a molekulát, másrészt kiválasztják az epébe. Májbetegség esetén csökken a májsejtek Aβ-felvétele, továbbá az albumin- és lipidszintet befolyásoló indirekt hatások is fontosak az Aβ eltávolítása szempontjából. A máj Aβ-eltávolító képességének növelése az AD kezelésének egyik szisztémás megközelítése lehet. A vesefunkció csökkenése növeli a vérben keringő Aβ szintjét, így a vesefunkció javítása is hozzájárulhat az AD megelőzéséhez és kezeléséhez. Az obstruktív alvási apnoé és a krónikus obstruktív tüdőbetegség a hipoxia és a gyulladás miatt fokozhatja az AD progresszióját. A krónikus szisztémás gyulladással járó betegségek – pl. reumatoid arthritis, periodontitis - az AD megnövekedett kockázatával járnak együtt, a NSAID-használat csökkent AD-kockázattal jár együtt. Ezzel ellentétben az akut szisztémás gyulladásos reakció a makrofágok révén véd az AD ellen (legalábbis állatmodellben). A bél-mikrobiom zavarai (Gram-negatívok) közreműködnek az AD progressziójában, a probiotikumok javítják az AD-betegek kognícióját. Napjainkban egyre több pathogén baktériumot is kapcsolatba hoznak az AD-vel, azonban egyelőre nem ismert, hogy a pathogének működnek-e közre az AD progressziójában, vagy az AD miatt nő a szervezet pathogének iránti fogékonysága. Szisztémás és komplex terápiás megközelítések Mindezek amellett szólnak, hogy az AD nemcsak agyi, de perifériás, szisztémás megbetegedés is, ezért a szisztémás terápiás megközelítések nagyobb sikerrel járhatnának, mint azok, amelyek csak a központi idegrendszert veszik célba. A tradicionális megközelítés – „egy célpont – egy gyógyszermolekula” – ráadásul figyelmen kívül hagyja az AD komplex pathomechanizmusát; ez magyarázhatja, hogy eddig több mint száz féle, Aβ-t célzó monoterápiás kísérlet vallott kudarcot. Ehelyett olyan terápiákra van szükség, amelyek a betegség különböző stádiumaiban jelentkező különböző rendellenességeket veszik célba, a központi idegrendszerben és a periférián egyaránt. A specifikus terápiák kifejlesztéséig is alkalmazható viszont az ismert komorbiditások és rizikótényezők szisztémás kezelése, a homeosztázis fenntartása, ami segíthet az Alzheimer-kór megelőzésében, progressziójának lassításában. dr. Kovács Bence Eredeti közlemény: Nat Rev Neurol. 2017 Sep 29;13(10):612-623. A systemic view of Alzheimer disease - insights from amyloid-β metabolism beyond the brain. Wang J, Gu BJ, Masters CL, Wang YJ.
Az inzulinrezisztencia több betegség, szindróma pathogenezisében részt vesz, ezek közül a legfontosabb a metabolikus szindróma, a 2-es típusú cukorbetegség, a polycystás ovarium szindróma
A rheumatoid arthritis (RA) patomechanizmusának ismert résztvevői az aktivált T-sejtek által stimulált B-sejtek és a monocyta-macrophag rendszer sejtjei, amelyek jelentős mennyiségű gyulladásos citokint termelnek. A citokinek hatásukat a különböző sejteken megjelenő receptorok közvetítésével fejtik ki.
Klinikum
A húgysav keletkezésének vannak endogen (purinszintézis, sejtpusztulás) és exogen (táplálkozás) forrásai. A kezelésnek tehát ennek megfelelően kell, hogy legyen nem csak endogen, hanem exogen útja is, ami magát a táplálkozást (és a helyes életvitelt is) foglalja magába.
Gyulladásos bélbetegség esetén több mint duplájára nő a demencia kockázata; IBD-ben szenvedőknél 7 évvel korábban kezdődik az elbutulás.
Mint az akkor a kutatásszervező Ventavia Research Group alkalmazásában álló regionális igazgató a The BMJ-nek elmondta, a Ventavia adatokat hamisított, nem maszkolt/nem vak módon kezelte a betegeket, nem megfelelően képzett vakcinátorokat alkalmazott, és a III. fázisú vizsgálatok során nem követte megfelelően a betegek által jelentett adverz eseményeket. A cég minőség-ellenőrzéssel foglalkozó munkatársai olyan sok problémát találtak, aminek megoldására képtelenek voltak. Miután a Ventavia vezetését a regionális igazgató, Brook Jackson többször is tájékoztatta a problémákról, az FDA-nak is panaszos e-mailt írt – a Ventavia még aznap kirúgta.
Hírvilág
Egyes vérnyomáscsökkentő gyógyszerek csökkenthetik a demencia kialakulásának kockázatát - közölték amerikai kutatók.
Idegtudományok
A menopauza során jelentős mértékben módosul az agy struktúrája, konnektivitása és metabolikus profilja. A menopauzára ható új szerek ezért az agyat veszik célba.
A tartós antikolinerg kezelés nem csak átmenetileg, hanem hosszú távon is rontja a kognitív teljesítményt.
A felnőtt agyba ültetett idegsejtek közül a legaktívabbaknak van legnagyobb esélyük a túlélésre.
Az agyi idegsejtpótló terápiák egyik legfőbb problémája, hogy a beültetett neuronok túlnyomó többsége nem integrálódik a meglévő neuronális hálózatba...
Hírvilág
A nagy dózisú E-vitamin mérsékelten lassítja a funkcionális hanyatlást a halálozás járulékos növelése nélkül, de ennek klinikai jelentősége tisztázatlan.
1.
2.
3.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről4.
5.
1.
2.
Klinikai Onkológia
Hasnyálmirigyrák: az ESMO klinikai gyakorlati irányelve a diagnózishoz, kezeléshez, követéshez*3.
Klinikai Onkológia
Gyógyszerbiztonsági szemelvények – a múlt tanulságai és a jövő lehetőségei4.
5.
HOZZÁSZÓLÁSOK
0 hozzászólás