Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 523
Trombózismenedzsment
2020. DECEMBER 26.
Gastrointestinalis vérzés és colorectalis daganatok kockázata pitvarfibrillációban szenvedő, véralvadásgátló kezelésben részesülő betegeknél
Eredeti közlemény: Gastrointestinal bleeding and the risk of colorectal cancer in anticoagulated patients with atrial fibrillation Rasmussen PV, Dalgaard F, Gislason GH, Brandes A, Johnsen SP, Grove EL, Torp-Pedersen C, Dybro L, Harboe L, Münster AB, Pedersen L, Blanche P, Pallisgaard JL, Hansen ML. Eur Heart J 2020 Feb 7;ehz964.
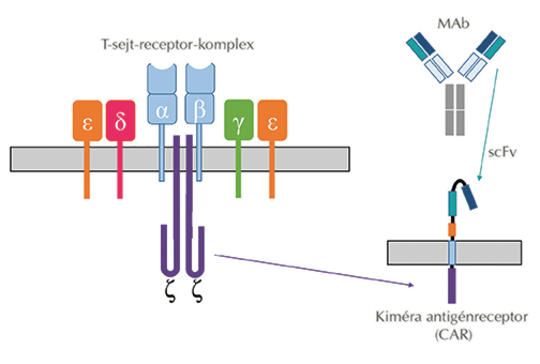
Génmódosított immunsejtek: új fegyverek nem csak daganatok ellen
Az elmúlt évtized onkológiai áttörése minden bizonnyal a CD19-specifikus CAR T-sejtek alkalmazása volt a különböző hematológiai kórképek kezelésében. A klinikai vizsgálatokban szerzett tapasztalatok, párosulva a magánszektor és gyógyszeripar befektetéseivel, a meglévő CAR T-sejt-készítmények kereskedelmi forgalmazásával, sok kutató figyelmét irányította rá az új típusú immunsejtekben rejlő lehetőségekre, és azok nem onkológiai célú felhasználására. A közlemény célkitűzése, hogy röviden bemutassa azokat a preklinikai alkalmazásokat, ahol a CAR T-sejteket sikerrel próbálták ki autoimmun és infektológiai kórképekben.
A vesetranszplantáció után „de novo” kialakult daganatok előfordulási gyakorisága és rizikófaktorai
A transzplantáció után alkalmazott immunszuppresszív terápia nemcsak fogékonnyá teszi a beteget a fertőzésekkel szemben, hanem a daganatsejtek felismerésének és eliminálásának funkcióját is károsítja. Vizsgálatunkat a Szegedi Tudományegyetem Sebészeti Klinikáján végeztük. A beválasztási kritériumok megállapítását követően 570 beteget vontunk be a vizsgálatba. Néztük a betegek életkorát, nemét, az alkalmazott immunszuppresszív terápiát, valamint kerestük a különböző immunszuppresszív szerek és a daganat típusa közötti kapcsolatot. 81 esetben diagnosztizáltunk „de novo” daganatot. A cyclosporint és tacrolimust szedők körében az átlagéletkorban (p = 0,734) és a testtömegindexben (p = 0,543) szignifikáns különbséget nem találtunk. A két betegcsoport között a graft működését tekintve szignifikáns eltérés nem mutatkozott (Tac vs. Cyc; 44 vs. 20). A vesetranszplantáltak körében a transzplantációtól a daganat diagnózisáig eltelt idő függvényében a prostata- és a méhnyakrák alakult ki a leghamarabb, de szignifikáns különbség nem mutatkozott. A bőrdaganatok előfordulása a leggyakoribb, ezt követik a poszttranszplantációs lymphoproliferativ betegségek. A tumorok kialakulásának növekvő kockázata legfőképpen az immunszuppresszív terápiára vezethető vissza.
A fej-nyaki daganatok komplex kezelése – áttekintés
A fej-nyaki laphámsejtes daganatok (head and neck squamous cell carcinoma – HNSCC) kezelése rendkívül komplex feladat, amely megkívánja a fej-nyak sebész, sugárterápiás szakember és klinikai onkológus szoros együttműködését. Elsődleges célnak a jó tumorkontrollt kell tekintenünk, de a terápia megválasztásánál szem előtt kell tartanunk az onkológiai radikalitás mellett az elfogadható életminőséget, ismervén, hogy a legtöbb lokális terápia nagyban befolyásolja a betegek légzés-, nyelés- és/vagy beszédfunkcióját. A megfelelő diagnosztikus vizsgálatok alapján a betegséget besorolhatjuk korai stádiumba, lokálisan/regionálisan előrehaladott stádiumba, illetve távoli áttétes és/vagy kiújult stádiumba. Kategóriánként eltérő terápiás modalitások jönnek szóba, amelyeket tovább bonyolít a primer tumor, az áttétek elhelyezkedése, a beteg állapota, társbetegségei, a daganat biológiai viselkedése. Jelen áttekintő közleményben a szerzők összefoglalják a fej-nyaki laphámrákok terápiájának alapelveit.
A hypoxia jelentősége a rosszindulatú daganatok progressziójában: terápiás lehetőségek, út a Nobel-díjhoz
Az elmúlt évtizedek kutatásai világossá tették, hogy a malignus daganatok egyik meghatározó jellemzője hypoxiás állapotuk és az ennek következtében aktiválódó genetikai, biokémiai és biológiai programok. A felismerés jelentőségét mi sem bizonyítja jobban, mint hogy 2019-ben az orvosi Nobel- díjat ezért ítélték oda a terület meghatározó tudósainak. A daganatszövetben keletkező hypoxia fő oka a proliferációval lépést nem tartó ereződés, de másik fontos oka a daganatos beteg szisztémás hypoxiája is. A hypoxiára adandó sejtes válaszok alapja a hypoxia indukálta (transzkripciós) faktorok stabilizálódása és aktivizálódása, ami azonban daganatokban az onkogén jelpályák konstitutív aktivitása miatt is bekövetkezhet hypoxia nélkül is. A daganatos hypoxia következménye az angiogén fenotípus, a sejtmetabolizmus átprogramozódása és a daganatellenes immunológiai válaszreakciók kedvezőtlen modulációja. A daganatszövet hypoxiája azonban negatívan befolyásolja a kemo-, sugár- és immunterápia hatékonyságát is. Mindezek miatt nagy szükség lenne a daganatos hypoxia célzott terápiájára, aminek első eszközei még csak most lépnek be a klinikai gyakorlatba. Fontos megjegyezni, hogy hazai kutatócsoportok nemzetközileg is elismert eredményekkel járultak hozzá ismereteink bővüléséhez ezen a területen.
A másodlagos májáttét eltávolításának indikációja – új terápiás megközelítések
A májsebészetben jelentős fejlődés volt megfi gyelhető az utóbbi évtizedekben: a műtét mortalitása rendkívüli mértékben csökkent, és az új technikák alkalmazásával a korábban technikailag nem műthető esetek váltak operálhatóvá. A máj a daganatok áttéteinek leggyakoribb helye, így a modernizáció a metasztázisok sebészetében is változásokat hozott. A műtéti mortalitás jelentős csökkenésével olyan szervek esetében is felmerült a májáttétek eltávolításának lehetősége, amelyeknél korábban nem tartottak műtétet indokoltnak (gyomor, pancreas). Az új technikák (laparoszkópia, portaembolisatio) alkalmazása óta eltelt idő alatt megjelent tanulmányok már lehetőséget adnak arra, hogy felmérjük onkológiai szempontból is az eredményeket. A laparoszkópos technika már nemcsak a primer tumorok, hanem a májáttétek kezelésében is teret nyert: a rövid és hosszú távú hatások, illetve az onkológiai eredmények szintén megfelelnek a nyitott műtétekének. Bár erre nagy esetszámú közlések nincsenek, a colorectalis daganatok szimultán májáttéteinek egy ülésben végzett reszekciójának növekedése várható a laparoszkópos technika alkalmazásától. A kiterjedt májáttétek esetében az érreszekcióval végzett májműtétek, elégtelen posztoperatív residualis májfunkció miatt végzett portaocclusio után végzett májreszekciókkal is jobb eredmény érhető el, mint az onkológiai kezeléssel. A májáttétek esetében az onkológus és a sebész közös döntése szükséges a megfelelő terápiás terv felállításához.
Beköszöntő
Magazinunk jelen száma a tüdőrák immunológiai kezelésének témáját járja körbe, de kitekintést ad - hírek és referátumok formájában - más daganatok ígéretes immunológiai kezeléséről is.
A COVID-19 epidemiológiája és terjedése Kína Sencsen tartományában 391 igazoltan fertőzött és 1286 közvetlen kontakteset retrospektív kohorsz-vizsgálata alapján
A Lancet tudományos folyóiratban megjelent közlemény a kínai Vuhan városban (Sencsen tartomány) a járvány legkorábbi időszakában összegyűjtött adatokat dolgozta fel. A szemlézőnek nem célja a tanulmány összes adatsorának részletes bemutatása és külön-külön értelmezése, sokkal inkább a munka következtetéseit szándékozik röviden összefoglalni.
Daganattúlélők nőihormon-pótló kezelése – Irodalmi áttekintés
Az onkológia gyors fejlődése az onkológiai betegek mind hosszabb túléléséhez vezet. Közülük egyre többen érik el a természetes menopauzát, vagy onkoterápiájuk mellékhatásaként idő előtt tapasztalják a gonadalis funkciók megszűnését, vazomotoros tünetekkel és hosszú távú negatív cardiovascularis és csontrendszerre gyakorolt hatásokkal. Egyre növekvő számban kérnek ilyen betegek endokrinológiai segítséget hormonpótló terápia (HRT) formájában. A WHI (Women’s Health Initiative) tanulmány eredményeinek téves értelmezése irracionális félelemhez vezetett a nőihormon-pótlás tekintetében mind a betegek, mind az orvosok körében. Számos orvos számára logikus és biztonságos következtetésnek tűnik a HRT elkerülése, feltételezve, hogy ez a hozzáállás biztosan nem okoz kárt, míg az ösztrogén önmagában vagy gesztagénekkel történő alkalmazása onkológiai és thrombemboliás kockázatokat hordoz, szövődmények esetén pedig peres eljárásokhoz is vezethet. Ugyanakkor már a WHI-tanulmány eredményei előtt is ismert volt, hogy a korai menopauza és hypogonadismus a skeletalis és a cardiovascularis hatások révén évekkel csökkenti a nők várható élettartamát, és ez a negatív hatás korrelál a hypoestrogenaemiás időszak hosszával. HRT-ről való döntés esetén ezeket a pró és kontra érveket kell mérlegelni úgy, hogy a HRT onkológiai kockázatát rendkívül nehéz objektíven felbecsülni. Összefoglaló tanulmányunkban áttekintjük a témával kapcsolatos legfrissebb evidenciákat az in vitro kísérletektől a klinikai vizsgálatokig, mind nőgyógyászati, mind nem nőgyógyászati daganatok túlélőinek vonatkozásában. Ez alapján a következő csoportokat határoztuk meg: a „HRT előnyös” (például I-es típusú endometriumcarcinoma, méhnyak-adenocarcinoma, malignus hematológiai betegségek, lokális melanoma malignum, colorectalis carcinoma, hepatocellularis carcinoma); a „HRT neutrális” (például BRCA 1/2 mutációt hordozóknál tumoros megbetegedés nélkül, II-es típusú endometriumcarcinoma, méhcarcinosarcoma és adenosarcoma, egyes ovariumtumorok, méhnyak-, hüvelyi és vulvalaphámrák, prolactinoma, veserák, hasnyálmirigyrák, pajzsmirigyrák); a „HRT relatíve ellenjavallt” különféle okok miatt (például leiomyosarcoma, bizonyos petefészekrákok, agydaganatok, előrehaladott metasztatikus malignus melanoma, tüdőrák, gyomorrák, húgyhólyagrák esetén); a „HRT kedvezőtlen hatású, ezért ellenjavallt” (például emlőrák, endometrium-, stromasarcoma, meningioma, glioma, hormonreceptor-pozitív gyomor- és hólyagrák).
A biológiai óra és a daganatok
Jelen összefoglalásban képet adunk a biológiai ritmusok közül a cirkadián ritmusról, annak szabályozásáról és a tumorgenezissel való kapcsolatáról. Cirkadián ritmusnak nevezzük azt a biokémiai, fiziológiai folyamatokban fellépő nagyjából 24 órás ciklust, amely az egysejtűektől a gerincesekig megtalálható. Ez a biológiai ritmus az endogén belső óráink és a fény mint fő „Zeitgeber” szinkronizációjának eredménye. Az emlősökben a hypothalamus területén elhelyezkedő nucleus suprachiasmaticus (SCN) tekinthető a szervezet „főórájának”, ami felelős a különböző szervrendszerekben található perifériás órák összehangolásáért. A cirkadián ritmus szabályozása az úgynevezett „circadian locomotor output cycles kaput”, a CLOCK géneknek a feladata. A CLOCK gének más effektor génekre hatva, a fehérjeszintézis diurnalis ritmusát szabályozzák. A cirkadián ritmus celluláris mechanizmusainak feltárását 2017-ben Nobel-díjjal jutalmazták. Egyre több adat bizonyítja a CLOCK gének és a daganatok kialakulása közötti összefüggést. Több tanulmány kapcsolatot mutat a váltott műszakban történő munkavégzés és az emlő-, valamint prosztatarák kialakulása között, valamint egyes cirkadián ritmust szabályozó gének mutációja és a tumoros elváltozás kifejlődése között. Egyre több adat utal a tumormetabolizmus és a CLOCK gének, azok szabályozása közötti kapcsolatra is. Mindezen adatok alapján a cirkadián ritmus, így a napszakok figyelembevétele a daganatterápiás kezelés során indokolttá válhat.
1.
2.
3.
4.
5.
1.
2.
3.
4.
Egészségpolitika
A Magyar Járóbeteg Szakellátási Szövetség állásfoglalása az ágazat helyzetéről5.
Gondolat
Üdv nálunk! Van már, aki írja a fekete pontjaid? – Nyomasztás a közoktatásban