Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 119
Migrénes stroke, migrén és stroke
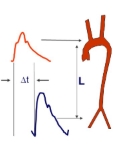
A migrén és a stroke kapcsolata több szintű. Mivel mindkettő gyakori, így ischaemiás stroke más okból migrénben is szenvedő betegnél is kialakul. Az ischaemiás stroke tünetei hasonlíthatnak aurás migrénre, és valódi migrénes infarktus (MI) is kialakulhat. Ez utóbbiról akkor beszélünk, ha a migrénroham teljesíti az alábbiakat: Aurás migrénben szenvedő betegnél jelentkezik, megfelel a korábbi rohamoknak, kivéve, hogy egy vagy több auratünet tovább tart, mint 60 perc, képalkotó vizsgálat infarktust igazol a megfelelő területben és más ok kizárható. A migrénes infarktus incidenciája alacsony, az összes ischaemiás stroke 0,2–0,5%-a. Ez a fiatalok körében azonban 13% is lehet. Az MI gyakoribb nőkben, elsősorban a hátsó érterületet érinti (posterior: 70–80%), általában kisméretű (64,7%), többszörös laesio észlelhető az esetek 41,2%-ában.
Idegtudományok
2022. MÁJUS 17.
Centrális vénajel a sclerosis multiplex képalkotó diagnosztikájában
A sclerosis multiplex (SM) diagnosztikáját jelentősen megnehezíti, hogy számos kórkép, mint például a migrén, bizonyos vascularis eltérések és egyéb gyulladásos megbetegedések, az SM-hez hasonló képet mutat. Az SM diagnosztikájában használt McDonald-kritériumrendszer az egyértelműen demyelinisatióra utaló esemény megléte esetén jól működik, ugyanakkor az atípusos, nonspecifikus vagy tünetmentes betegekben hibás SM-diagnózishoz vezethet, főleg, ha az MR-képanyag olyan eltéréseket mutat, melyek ismeretlen jelentőséggel bírnak. A centrális vénajel megfelelő határértékek megválasztása esetén magas specificitással bír az SM és az SM-utánzó kórképek differenciálásánál. A T2*-súlyozott szekvenciák alkalmazása tovább növelheti a jel szenzitivitását is.
NMDAR-encephalitissel átfedő demyelinisatiós szindróma – diagnosztikai és terápiás kérdések
Az anti-N-metil-D-aszpartát-receptor (NMDAR-) encephalitis az NMDAR GluN1 alegysége elleni IgGantitestekkel társuló autoimmun kórkép. A tünetek súlyossága ellenére csak a betegek 35%-ánál mutatható ki koponya-MRI-vel károsodás, ami leggyakrabban monofázisos formában fordul elő. A legfrissebb adatok alapján azonban az anti-NMDAR encephalitisben szenvedők kis százalékánál további relapszusok jelentkezhetnek, melyek hátterében demyelinisatiós laesiók mutathatók ki. A szakirodalomban egyre több adat lelhető fel, miszerint az NMDAR-encephalitis átfedést mutathat más autoimmum, demyelinisatiós kórképpel, leggyakrabban neuromyelitis optica spektrum betegséggel (főként anti- MOG ellenanyag-pozitív estekben), ritkábban sclerosis multiplexszel. A felmerülő diagnosztikai nehézségeket egy eset kapcsán mutatjuk be. A 24 éves férfi pszichiátriai beutalást követően 2 hónapos tünetkezdetet követően először 2014 májusában került felvételre a Neurológiai Klinikára memóriazavar, bal oldali latens hemiparesis kivizsgálása céljából. Akkor készült koponya-MRI-n disszeminált, gócos agyi folyamat ábrázolódott, gyűrűszerű kontrasztanyag-halmozással, kétoldali hippocampus-érintettséggel. A látott kép leginkább ADEM-nek felelt meg. A liquorban oligoklonális gammopathia látszott. A virális és paraneoplasiás eredetet kizártuk. Intravénás szteroidterápiára átmeneti javulás jelentkezett, azonban a terápia leépítését követően ismételt állapotrosszabbodás következett be. A szteroidterápia ismétlése érdemi változást nem hozott, plazmaferézisben részesült, azathioprinterápiát kapott. A diagnosztikai vizsgálatok során az ellenanyag-vizsgálat alapján anti- NMDAR encephalitis diagnózist állítottuk fel. PET CTvel követtük 3 évig. Állapota stagnált, koponya-MRI-n sem jelent meg új laesio, kifejezett jobb oldali hippocampalis atrophia látszott. Imuran elhagyását követően 2 évvel kettős látása jelentkezett, koponya-MRI-vizsgálaton novum fehérállományi laesiók jelentek meg. A látott radiológiai kép és a korábbi liquorlelet, valamint a klinikum alapján felmerült sclerosis multiplex lehető- sége, intravénás nagy dózisú szteroidterápiát alkalmaztunk. Szérum-aquaporin-4, anti-MOG, anti-NMDAR ellenanyag- vizsgálat a szteroidterápiát követően készült, negatív eredményt adott. A szakirodalmat részletesen áttekintve az anti-MOG ellenanyag-pozitív NMO szövődik leggyakrabban az NMDA-R encephalitisszel átfedő demyelinisatiós szindrómával, a sclerosis multiplex ettől jóval ritkább. A közös hatékony terápiás opció a rituximab, aminek támogatását kérvényeztük.
[Heveny vestibularis szindróma képében jelentkező késői meningitis carcinomatosa – klinikopatológiai esetismertetés]
[Célkitűzés – Bár a szédülés a leggyakrabban előforduló panaszok egyike, a vestibularis perifériák hirtelen kialakult tónusaszimmetriája hátterében mégis ritkán találunk perifériás eredetű betegséget utánzó malignus koponyaűri tumorokat. Dolgozatunk egy heveny vestibularis szindróma klinikai képében jelentkező, késői, temporalis csontot is beszűrő, disszeminált, generalizált mikrometasztázisokkal járó meningitis carcinomatosa esetet mutat be, ami egy primer pecsétgyűrűsejtes gyomorcarcinoma felébredését követően jelent meg. Kérdésfelvetés – Célul tűztük ki, hogy azonosítjuk azon patofiziológiai folyamatokat, melyek magyarázatul szolgálhatnak a daganat felébredésére, disszeminációjára. A vestibularis tónusaszimmetria lehetséges okait szintén vizsgáltuk. Ötvenhat éves férfi betegünk interdiszciplináris orvosi adatait retrospektíven elemeztük. Összegyűjtöttük és részletesen újraértékeltük az eredeti klinikai és patológiai vizsgálatok leleteit, majd új szövettani festésekkel és immunhisztokémiai módszerekkel egészítettük ki a diagnosztikus eljárásokat. Kórboncolás során a nagyagy és a kisagy oedamás volt. A bal piramiscsont csúcsát egy 2 × 2 cm nagyságú daganatmassza szűrte be. A gyomorreszekátum eredeti szövettani metszeteinek újraértékelése submucosus daganatinfiltrációt igazolt vascularis invázió jeleivel. Immunhisztokémiai vizsgálatokkal dominálóan magányosan infiltráló daganatsejteket láttunk cytokeratin 7- és vimentinpozitivitással, valamint részleges E-kadherin szövettani festésvesztéssel. A kórboncolás során nyert szövetminták ezt követő hisztológiai vizsgálatai igazolták a disszeminált, többszervi mikroszkopikus daganatinváziót. Az újabb eredmények igazolták, hogy a vimentin kifejeződése, valamint az E-kadherin elvesztése szignifikáns (p < 0,05) kapcsolatot mutat az előrehaladott stádiummal, a nyirokcsomóáttétek jelenlétével, a vascularis és neuralis invázióval, valamint a nem differenciált szöveti típussal. Betegünk középkorú volt és nem volt immunhiányos állapotban, így a gyomorcarcinoma kilenc éven át tartó alvó állapotot követő felébredését nem tudtuk megmagyarázni. A daganat szervspecifikus tropizmusa, melyet a „seed and soil” teóriával magyaráznánk, kifejezetten váratlan volt, mivel a gyomorrákok ritkán képeznek áttétet az agyburkokon, hiszen a daganatsejtek elenyésző számban jutnak át a vér-agy gáton. Következtetések – Az előzményben szereplő malignus folyamat, valamint egy új neurológiai tünet megjelenése fel kell, hogy keltse a klinikus figyelmét a központi idegrendszer daganatos érintettségére, melyet adekvát, célzott diagnosztikus és terápiás stratégia megtervezése kell, hogy kövessen. Ehhez célzott szövettani festési eljárások, specifikus antitestek alkalmazása szükséges. A közelmúlt eredményei sejtkultúrákon igazolták a metformin epithelialis-mesenchymalis transitiót erősen gátló hatását gyomorrák esetében. Így további kutatást kell végezni azon esetekben, amelyekben az epithelialis-mesenchymalis transitióra pozitív eredményeket kapunk.]
A kemoterápia daganatkeltő hatása
Kemoterápia nélkül a felfedezett daganatos betegségek ötéves túlélési rátája – daganatfüggően – 0–15% között lenne, a jelenlegi terápia alkalmazásával 17-85%. Ugyanakkor számos figyelmeztetés hívja fel a figyelmet a kemoterápia által indukált nemkívánatos mellékhatások, legfőképpen a lehetséges tumorindukciós képesség veszélyeire, ami az öt éven túl gyógyult betegek 5-10%-át is érintheti. A szisztémás kemoterápiában használt egyes gyógyszerek (alkilálószerek, etopozid, arzén-trioxid) képesek a szervezet egészséges sejtjeiben mutációt okozni, amivel megnő a valószínűsége annak, hogy a mutációt szenvedett sejtek egy későbbi (szekunder) daganatképződést indítsanak el. A mutagén hatások mellett egyes kemoterapeutikumok a szervezet normális myeloid és epithelialis sejtjeire fejtenek ki olyan hatásokat, amelyek a szöveti mikrokörnyezet átalakításával megteremtik a malignus transzformáció lehetőségét. Ebben a folyamatban igen fontos szereplők a tumorokkal asszociáló makrofágok (TAM), amelyek a daganatsejt által szekretált faktorok és mikroszómák hatására megváltoztathatják génexpressziós mintázatukat, és prokarcinogén szignálokkal segítik a tumorsejtek megmaradását, invazivitását, csökkentik a citotoxikus T-sejtek aktivitását. Mindezen okok miatt kiemelten fontos az, hogy a daganatkeltő mutagénekkel dolgozó orvosok, gyógyszerészek, technikusok és nővérek ne kerüljenek közvetlen érintkezésbe ezekkel a veszélyes anyagokkal, hanem használjanak megfelelő védőfelszerelést.
A COVID-19 és a kardiovaszkuláris rendszer
A SARS- CoV-2-fertőzés nemcsak pneumoniát, de akut myocardialis és krónikus kardiovaszkuláris sérülést is okozhat. A Nature Review Cardiology-ban megjelent kommentár összefoglalja a COVID-19-cel kapcsolatos kardiológiai tudást.
A sclerosis multiplex néhány aktuális kérdése: a szekunder progresszív forma
A sclerosis multiplexben szenvedő betegek klinikai statusának hosszú távú romlása sok esetben független a relapsusoktól és az MRI-n igazolt új laesióktól. A szekunder progresszív sclerosis multiplex esetén az állapotrosszabbodás - megközelítően hat hónapos intervallum alatt - függetlenül halad előre a relapsus(ok)tól. Ugyanakkor a korai gyulladásos aktivitás és a gerincvelő-laesio mértéke hosszú időre előre jelzi a relapsussal kezdődő kórforma lefolyását.
Multiplex tüdőtályoggal társuló súlyos polymyositis esete
BEVEZETÉS - Az idiopathiás inflammatorikus myopathiák a harántcsíkolt izmok immunmediált gyulladásával jellemezhető autoimmun betegségek.
EMT (epithelialis-mesenchymalis átmenet) – CSC (daganatos őssejtek)
A daganatellenes kezelés hatékonysága rendszerint korlátozott a gyógyszerekkel szembeni rezisztencia miatt. A szerzett rezisztencia egyik fontos oka az intratumoralis heterogenitás, ami a daganatsejtek fenotípusa közötti változatosságot jelenti egy tumoron belül. Ez a heterogenitás a genotípust érinti elsősorban. A daganatos őssejtek (cancer stem cell, CSC) a koncepció szerint képesek meghatározni a daganat progresszióját, a klinikai onkológia legnagyobb kihívásaként metasztázisok létrejöttét. Hogy ez kialakuljon, a tapasztalatok szerint hámeredetű daganatoknál az epithelialis karaktert mesenchymalisnak kell felváltania (epithelial-mesenchymal transition), ha nem is teljesen. A CSC fenotípusához tartozik, a normális szöveti őssejtekhez hasonlóan. a szerekkel szembeni rezisztencia, illetve a károsításokat követő regeneráció. Ezeknek a tulajdonságoknak a szabályozó mechanizmusa még alig ismert, de minden bizonnyal ebben genetikai és epigenetikai tényezők egyaránt szerepet játszanak. Ha ezeket terápiás célpontként megismerjük, talán a leghatékonyabb kezelési stratégia birtokába juthatunk.
A relabáló epithelialis petefészekrákok kezelése
A petefészekrák a leggyakoribb nőgyógyászati daganat okozta halálozási ok, és a legtöbb betegség előrehaladott FIGO stádiumban kerül diagnosztizálásra. Az iniciális debulking műtét és az első vonalbeli paclitaxel/carboplatin kombinációs kemoterápia alkalmazásának ellenére, a betegek közel kétharmada relabál az első három évben. A petefészekrák kezelésére irányuló kutatások az utóbbi években elsősorban a fenntartó kezelésekre irányultak, a betegek progressziómentes időszakainak hoszszabbítása céljából. A relapszusok molekuláris biológiájának egyre jobb megértése az angiogenezis-gátló bevacizumab és kemoterápiák kombinációinak bevezetéséhez vezetett, melyek az iniciális, a fenntartó és a relabáló (platinaszenzitív és platinarezisztens) daganatok esetében egyaránt hatásosnak bizonyultak. Az utóbbi időben egy új fenntartó kezelés került alkalmazásra a mindennapi klinikai rutinban, a PARP-gátló olaparib monoterápia, mely a platinaszenzitív, relabáló, magas grádusú szerózus petefészekrákok kezelésében bizonyult hatásosnak. Az új terápiák bevezetésének ellenére azonban még számos tisztázatlan kérdés van a relabáló epithelialis petefészekrákok kezelésében. Jelen áttekintés célja a kiújuló, progrediáló petefészekrákok terápiás lehetőségeinek összefoglalása az evidenciák és az új terápiás modalitások tükrében.
1.
2.
3.
4.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről5.
1.
2.
Klinikai Onkológia
A rosszindulatú daganatok fenotípusának plaszticitása és az immunogén mimikri3.
Klinikai Onkológia
A szarkopénia mérése komputertomográfiával és jelentősége az onkológiai betegeknél4.
5.