Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 435
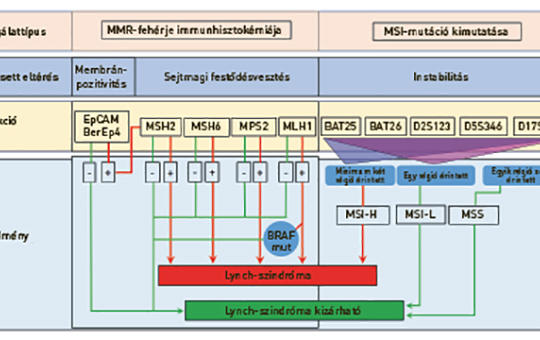
Mikroszatelliták mint a genom „szeizmográfjai”
A genetikai állomány fehérjét nem kódoló, monotonon ismétlődő, 1–6 nukleotidot tartalmazó szakaszain, a mikroszatellitákon a DNS-kettőződésért felelős polimerázok könnyen hibáznak. Így azok rövidülnek vagy hosszabbak lesznek. Ha az ilyen típusú DNS-hibákat javító enzimek működőképesek, a mutációk kijavítódnak. Ha nem, akkor különböző hosszúságú szakaszokként, instabil formában adódnak át az utódsejtekbe. Nemcsak korán jelzik a fokozott mutációs hajlamot, hanem önmagukban is, keretleolvasási problémát okozva, továbbiakat generálnak. Következésképpen a mikroszatellita-instabil (MSI) daganatok nagyobb arányban fejeznek ki idegen antigéneket, mint ezen eltérést nem mutatók, ami a tumorellenes immunválasz fokozott hatékonyságát valószínűsíti. Az MSI tehát nemcsak a genetikai instabilitásra, hanem az immunellenőrzőpont-gátló szerek hatásosságára is utal. Jelenlétét lehet közvetlenül, nukleotidfelbontási szintű PCR-alapú eljárással vagy közvetve, a hibajavító fehérjék kimutatásával, immunhisztokémiával vizsgálni, de ma már új generációs szekvenálási adatokból és mesterséges intelligencia képi elemzésből is kinyerhetők ilyen információk. Az MSI-meghatározás módszertanát és klinikai jelentőségét foglaljuk össze.
Sugárterápia indukálta másodlagos daganatok
Az onkológiai kezelések szerves részét képezi a sugárterápia, amiben a betegek közel fele részesül. A modern onkológiai kezeléseknek köszönhetően a túlélés egyre hosszabb, így a betegek körülbelül egyötöde megéli azt is, hogy egy második tumor kialakuljon. Több tanulmány szerint maga az onkológiai kezelés is összefüggésbe hozható a másodlagos primer tumor kialakulásával, ami egyes becslések szerint az esetek 5-8%-ában lehet a sugárterápia következménye. Nagy kihívást jelent, hogy megértsük a sugárterápia okozta hatásokat az esetlegesen túlélő daganatsejtekben, a daganatot körülölelő egészséges szövetekben, az alacsony dózisban részesült területekben, illetve az egyáltalán nem irradiált szövetekben, ahol abszkopális hatások érvényesülhetnek. Ezek együttes hatása tehető felelőssé az úgynevezett radiokarcinogenezis kialakulásáért. Manapság számos tanulmány foglalkozik a sugárterápia daganatindukáló hatásaival. Ez az összefoglaló arra hivatott, hogy áttekintse a témával kapcsolatos ismereteinket a patogenezis, radiogenomikai, sugárfizikai és sugárbiológiai szempontok alapján, továbbá tárgyalja a megelőzés és a szűrés lehetőségeit. A sugárterápia kétélű fegyver, amely egyrészt nagyon jól alkalmazható a daganatos betegségek kuratív kezelésében, másrészt azonban potencionálisan másodlagos daganatot indukálhat, amely évekkel később jelentkezik. Emiatt a jövőben a maximálisan optimalizált, személyre szabott sugárterápiának lehet csak létjogosultsága.
Angiogenezis-gátlók és immunjelátviteli pontokra ható szerek kombinációja egymás hatásának potencírozására
A daganatok nem sebészi kezelésében mind az angiogenezis gátlásának, mind az immunfolyamatok befolyásolásának jelentős és egyre növekvő szerepe van. A tumoros neo-angiogenezis kedvezőtlenül befolyásolja az immunrendszer működését, ezért gátlása serkenti a kulcsfontosságú T-lymphocyták és azok működését támogató egyéb tényezők hatását, kedvezően befolyásolja a daganat mikrokörnyezetét, miközben az immunjelátviteli pontokra ható kezelés segít az érrendszer normalizálásában. A két támadáspont együttes befolyásolása ezért kedvező hatású lehet. A szerzők vesesejtes rákban, melanoma malignumban, nem kissejtes tüdőrákban, vastag- és végbél-, valamint hepatocellularis és emlőrákban mutatják be a két hatásmechanizmusú csoportba tartozó szerek alkalmazását és kombinálását, megállapítva, hogy sikerrel zárult fázis III vizsgálatok döntően a világos sejtes (vagy világos sejtes komponenst is tartalmazó) vesesejtes rákokban történtek. Hangsúlyozzák, hogy az immunterápiához általában szükséges az érzékenységet előrevetítő paraméterek (megfelelő PD-L1, MSI-H, dMMR, TMB-H) kimutatása, és a tumoragnosztikus kezelés terápiás filozófiája mellett is figyelembe kell venni a törzskönyvezett javallatokat.
A daganatos elváltozások hatékony diagnosztikáját segítő labort alakítottak ki Szegeden
A daganatos elváltozások hatékony diagnosztikáját segítő laboratóriumot alakítottak ki uniós támogatással a Szegedi Tudományegyetem (SZTE) patológiai intézetében – tájékoztatta a felsőoktatási intézmény közkapcsolati igazgatósága az MTI-t.
A méhnyakrák korszerű onkológiai kezelése
Világszerte évente több mint félmillió nőnél igazolódik méhnyakrák, és körülbelül 300 000 halálesetet okoz a betegség. A nyugati társadalmakban a cervixcarcinoma incidenciája és mortalitása csökken a humán papilloma vírus (HPV) elleni vakcinációnak és a populációs szintű szűrésnek köszönhetően. A fejlődő világ országaiban azonban továbbra is emelkedő a tendencia. A rákmegelőző állapotok és a korai méhnyakrák definitív onkológiai ellátása a stádiumfüggő kiterjesztéssel végzett műtétek révén lehetséges. A posztoperatív sugárkezelés vagy kemoradioterápia szükségessége a patológiai rizikófaktorok alapján határozható meg. Előrehaladott méhnyakrákban a definitív kemoradioterápia vagy a szisztémás kezelés a terápiás alternatívák. A fiatal betegek részéről gyakran felmerülő kívánság a fertilitásmegtartás, amely az onkológiai elvekkel csak jól definiált határok között egyeztethető össze, alapos felvilágosítást követően. A terhesség alatt felismert méhnyakrák becsült incidenciája 1,4-4,6 eset/100 000 szülés, amelynek ellátása során, az onkológiai szempontokon túl, a magzat biztonságát is szem előtt kell tartanunk az anya preferenciái alapján. A klasszikus kemoterápia mellett a biológiai szerek is megjelentek a közelmúltban a méhnyakrák szisztémás kezelési lehetőségei között: első vonalban bevacizumabbal egészíthető ki a ciszplatin-paclitaxel kombináció közel négy hónapos túlélési előnyt nyújtva a betegek számára; míg másodvonalban pembrolizumab adható mikroszatellita-instabil vagy PDL-1-et expresszáló (combined positive score [CPS] ≥1), illetve magas tumormutációs terheltséget (TMB ≥10) mutató daganatok esetén. A jelen munka egy rövid összefoglalót szolgáltat a méhnyakrák megelőzéséről, kivizsgálásáról és onkológiai ellátásáról.
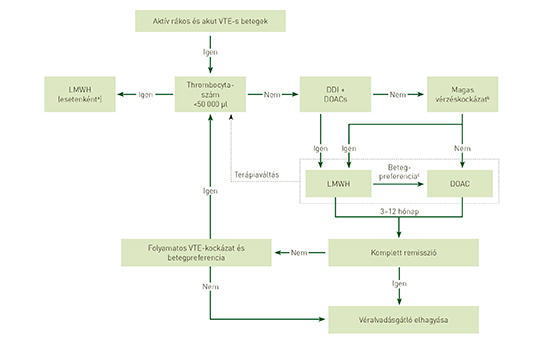
A daganatos betegségekhez társuló vénás thromboembolia a szájon át szedhető direkt antikoagulánsok korában
A daganatokhoz társuló vénás thromboembolia (VTE) kérdése kihívást jelent, mivel a K-vitamin-antagonisták és a kis molekulasúlyú heparinok (LMWH-k) adagolásának kényelmetlenségei miatt komplikációk jelenhetnek meg, mint például a vérzés vagy a kemoterápiás szerekkel való összeférhetetlenség. A szájon át szedhető direkt antikoagulánsok (direct oral anticoagulants – DOAC-ok) részben kiküszöbölik ezeket a problémákat, de daganatos betegek adatait tartalmazó nagy klinikai vizsgálatokban mostanáig nem mérték ezen szerek hatásosságát és biztonságosságát. A szerzők az alábbi közleményben összefoglalják a kezelési ajánlásokat, az antikoagulánsok kiválasztásának vizsgálati és gyakorlati bizonyítékait, a daganatos betegek VTE-jében a DOAC szerepét vizsgáló legújabb klinikai kutatások eredményeit (Hokusai-VTE-Cancer, SELECT-D, CARAVAGGIO és ADAM VTE), és a DOAC-ok használatával kapcsolatos egyéb, speciális megfontolásokat. A klinikai guideline-ok a rendelkezésre álló adatokra alapulva azt javasolják, hogy a daganatos betegségek mellett fellépő VTE-k esetén a betegnek legalább három-hat hónapig LMWH-kezelést kell adni, ugyanakkor ezek a betegek az LMWH-kat az alkalmazás nehézségei miatt az orális antikoagulánsokhoz képest mégsem kellő mértékben használják. Másrészt a DOAC-ok használatát egyre több klinikai adat is alátámasztja. A Hokusai-VTE-Cancer vizsgálatban az edoxaban nem teljesített gyengébben a dalteparinnál („not inferior”) az ismétlődő VTE-k és a nagy vérzések összesített mértékében (12,8% versus 13,5%), számszerűleg viszont kevesebb volt az ismétlődő VTE-k száma (7,9% versus 11,3%). Csak azokban a gastrointestinalis daganatos esetekben volt szignifikánsan több edoxaban mellett a jelentős vérzés (6,9% versus 4,0%), ahol magasabb volt a vérzés kockázata is. A SELECT-D vizsgálatban a rivaroxaban mellett számszerűleg kevesebb volt a VTE-k kiújulásainak a száma (4% versus 11%), a nagy vérzések száma hasonló volt (6% versus 4%) és számszerűen több volt a klinikailag releváns kisebb vérzések száma (13% versus 4%) a dalteparinhoz képest. A legtöbb vérzés gastrointestinalis és urológiai jellegű volt, viszont a nyelőcső- és gastrooesophagealis daganatos betegeknél több jelentős vérzés fordult elő a rivaroxaban mellett (36% versus 11%). Az apixaban és a dalteparin összehasonlítása még jelenleg is folyik a CARAVAGGIO vizsgálatban, az ADAM VTE vizsgálat előzetes eredményei is biztatóak. A közlemény végső következtetései szerint a DOAC-ok a daganatos betegségekhez társuló VTE-kben az LMWH-k észszerű, elfogadható alternatíváit képviselik. Gastrointestinalis daganatos betegekben ugyanakkor a DOAC-ok használatát esetről esetre át kell gondolni, figyelembe véve az előnyöket és a relatív kockázatokat.
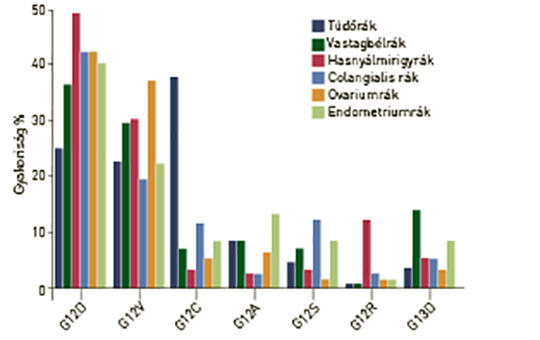
A (K)RAS-mutáció molekuláris epidemiológiája emberi daganatokban
A RAS onkogén mutációja a leggyakoribb génhiba emberi daganatokban, és a három családtag közül a K-RAS-é a leggyakoribb, amit az N-RAS követ. A tipikus K-RAS-mutáns daganatok a hasnyálmirigyrák, vastagbélrák és tüdő-adenocarcinoma, amelyekben a mutáns variáns allélok gyakorisága igen heterogén, aminek hátterében eltérő karcinogenezis áll. A RAS-mutáns daganatok genetikai sokszínűségét tovább fokozza, hogy a mutáns allél homo- vagy heterozigóta formában van-e jelen. A sokszínűség egy másik forrása az, hogy a különféle daganatokban a K-RAS-mutánsok esetében sajátos kísérő mutációs mintázatú altípusok lehetnek. Mindezeknek az a következménye, hogy a K-RAS-mutáns daganatok biológiai viselkedése és nagy valószínűséggel terápiás érzékenysége is nagyon heterogén lehet. A K-RAS-inhibitorok klinikai debütálásával ezeknek a kérdéseknek egyre nagyobb jelentősége lesz.
Hírvilág
2021. FEBRUÁR 03.
Rákellenes világnap
A Rákellenes Világnapot immár 21 éve tartják minden év február 4-én. Idén van a Nemzetközi Rákellenes Unió (UICC) hároméves „Ez vagyok és ezt teszem” (I am and I will) kampány utolsó éve. A Magyar Rákellenes Liga mindenkit hív, hogy sétáljon, fusson, mozogjon velük 30 percet a Rákellenes Világnapon.
A CT-vizsgálatok mellékhatásai
A képalkotó radiológiai diagnosztikai eljárások körében egyre terjednek a viszonylag nagy dózisú sugárexpozíciót eredményező, de vitathatatlan diagnosztikus előnyt mutató komputertomográfiás (CT-) vizsgálatok. A sztochasztikus sugárhatások lineáris, küszöbdózis nélküli modellje alapján a legkisebb elszenvedett sugárdózis is kiválthatja daganatok keletkezését. A CT-vizsgálatok során elszenvedett sugárexpozíció miatt kialakuló daganatkeletkezés, magasabb sugárérzékenységük és várható hosszabb élettartamuk miatt, elsősorban a fiatal korosztályt érinti. A témakört vizsgáló legtöbb epidemiológiai tanulmány arra a következtetésre jutott, hogy a CT-vizsgálatok dózisfüggően megnövelik fiatalokban a leukémiák és agydaganatok kialakulásának a kockázatát. Az abszolút daganatszámok azonban nem jelentősek, így megfelelő indikáció esetén a vizsgálatot a lehető leghamarabb el kell végezni. Állapotos nőkön végzett, az alhasi régiót érintő CT-vizsgálatok fejlődési rendellenességek kialakulásához vezethetnek a magzatban. Az esetek túlnyomó többségében azonban csak sorozat-CT-vizsgálatok eredményezhetnek 100 mGy feletti magzati expozíciót, amely felvetheti a terhesség megszakítását. A sugárexpozícióval járó képalkotó vizsgálatok indokoltságáért, optimált elvégzéséért a kezelőorvos a felelős.
A 2020-as ESMO virtuális kongresszusának újdonságai
A 2020-as év mindannyiunk számára váratlan nehézségekkel indult. A SARS-CoV-2 járvány régen tapasztalt kihívás elé állította a világ egészségügyi rendszereit. Minden országban megfigyelhető az egészségügyi források átcsoportosítása, a betegek orvoshoz fordulási hajlandóságának járványügyi szempontok alapján való megváltozása. Az online medicina elmúlt időszakban tapasztalható térhódítása tovább gyorsult. Egyre inkább kirajzolódik, hogy az orvos-beteg találkozások mely része valósítható meg digitálisan és milyen esetben elengedhetetlen a személyes találkozás. Ilyen közegben rendezték meg idén, rendhagyó formában, az ESMO virtuális kongresszust, ahol az eredményeket és előadásokat online követhettük, a korábban megszokott több tízezres forgatag helyett. A legfontosabb vizsgálati eredmények, újdonságok összefoglalóját olvashatjuk az alábbiakban.
1.
2.
3.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről4.
5.
1.
2.
Klinikai Onkológia
A rosszindulatú daganatok fenotípusának plaszticitása és az immunogén mimikri3.
Klinikai Onkológia
A szarkopénia mérése komputertomográfiával és jelentősége az onkológiai betegeknél4.
5.