Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 26
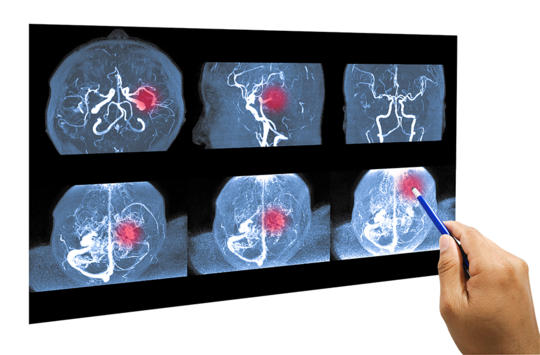
A tenectepláz biztonságossága és hatékonysága natív CT-vel értékelt ébredési stroke-ban
Roaldsen és munkatársai a The Lancet Neurology-ban megjelent cikkükben a TWIST-vizsgálat eredményeit mutatják be, amely a natív koponya-CT alapján indikált, 0,25 mg/kg dózisban alkalmazott tenectepláz hatását vizsgálja ébredési stroke-ban.
Gyermek- és felnőttkori high-grade gliomák komplex genetikai karakterizálása újgenerációs szekvenálással: Tapasztalatok és kutatási irányok
A központi idegrendszeri tumorok újgenerációs szekvenáláson (next-generation sequencing – NGS) alapuló panelek segítségével végzett komprehenzív genetikai analízise a terápiás célpontok keresése mellett a patogenezis egyre pontosabb megismerését teszi lehetővé.
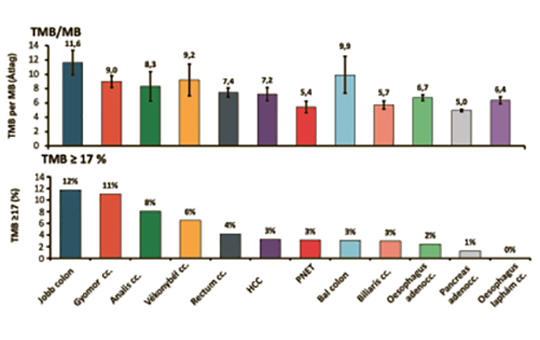
Biomarkerek szerepe a gastrointestinalis daganatok kezelésében
Összefoglaló – A komprehenzív molekuláris profilvizsgálatokon, a bioinformatika fejlődésén alapuló precíziós onkológiai megközelítés, célzott terápia és immunellenőrzőpont-inhibitorok (immune checkpoint inhibitors – ICI) gyökeresen változtatta meg az onkoterápia eredményeit. Az előrehaladott, metasztatikus stádiumú emésztőrendszeri daganatokban szenvedő betegek kedvezőtlen túlélési esélye jelentősen javult az új terápiás lehetőségek alkalmazásától. A sikeres terápia azonban számos molekuláris jellemző ismeretét, meghatározását igényli – PD-L1 expresszió, MSI (mikroszatellita-instabilitás)/dMMR (mismatch repair deficiency), TMB (tumor mutational burden), rezisztenciamutációk, genetikai variánsok jelenléte. Jelen összefoglaló célja áttekintést adni a gastrointestinalis (GI) traktus rosszindulatú daganatainak precíziós onkológiai szemléletű kezelésében alkalmazható prediktív és prognosztikus biomarkerek szerepéről, jelentőségéről.
Vegyi anyagok és daganatok
A daganatképződés hátterében nem letalis genetikai hibák állnak, elsősorban meghibásodott szabályozórendszerek, mint a szuppresszor gének inaktivációja, sérülése, elvesztése, a protoonkogének aktivációja, amplifi kációja, az apoptózisgének sérülése vagy a DNS-repair gének funkciócsökkenése. Számos vegyi anyag a sejtben DNS-mutációt hoz létre a fenti szabályozó génekben, ezzel iniciálja a sejtet a folyamatos proliferációra, teret adva további mutációk felszaporodásának. A mutációt okozó (genotoxikus) vegyi anyagok általában megnövelik a daganat-előfordulási rátát, karcinogének.
Az áttétes colorectalis rák molekuláris altípusai és a terápiás döntések fejlődése
A colorectalis ráknak (CRC) klinikailag igen jelentős molekuláris heterogenitása van, amely különböző szinteken jelentkezik: a genomikában, az epigenomikában, a transzkripcióban és a mikrokörnyezetben. A karcinogenezis során szerzett genomikus történések hajtják („drive”) áttétes helyzetben a rák progresszióját. Például a KRAS- és az NRAS-mutációk jelzik azokat a daganatsejt-populációkat, amelyek refrakterek az EGFR monoklonális antitestekre, a BRAFV600E-mutációt hordozók viszont rosszabb kimenetelre számíthatnak a standard kezelések és a kombinált célzott kezelések mellett, míg a HER2-amplifi káció arra utal, hogy a daganat különlegesen érzékeny egy kettős HER2-blokáddal szemben. A többszörös, ritka géneltérések által hajtott EGFR monoklonális antitestek elleni rezisztencia jelentős átfedésben van a primer, valamint a szerzett rezisztencia mechanizmusában a klónszelekciós folyamat során. Ebben a tekintetben refrakter esetekben a keringő tumor-DNS szekvenciális vizsgálata vezethet gyógyszerek kifejlesztéséhez. A ritka kinázfúziós események és a DNS-károsodás utáni repair-ben részt vevő gének komplex eltéréseit is leírták, amelyek a célzott kezelések targetjei lehetnek. Másrészt a transzkripció szubtípusai és a jelátviteli utak aktivációs jelei szintén prognosztikai és potenciálisan prediktív értékkel bírnak áttétes colorectalis rákban. Ezek a jelek a stromalis sejtek és az immunkörnyezeti sejtek, valamint a daganatsejtek közötti interakciókat jelzik. Például a mikroszatellita-instabilitást mutató (MSI) vagy a POLE ultramutáns CRC-daganatsejtek különlegesen érzékenyek az immunellenőrzőpont-gátlókra, míg az olyan mesenchymalis fenotípusú daganatok, amelyeket az immunszuppresszív molekulák aktivációja jellemez, jó tárgyai lehetnek egy új immunterápiás kombináció kialakítására. Ebben a cikkben átnézzük az áttétes CRC-ben kimutatott, célzott terápiára alkalmas onkogéneltéréseket és -szignatúrákat, valamint tárgyaljuk az új molekuláris diagnosztikus próbák klinikai alkalmazásának lehetőségeit.
Klinikai Onkológia
2017. MÁJUS 10.
Miért nem hatékonyak az immunellenőrzőpont-gátlók colorectalis carcinomában?
Az elmúlt években kimutatták, hogy az immunellenőrzőpont-gátlók hatásosak különféle malignus daganatok kezelésére, de kevésbé alkalmazhatók colorectalis carcinomában (CRC). Miközben egy egykaros fázis II. klinikai vizsgálatban a CRC mikroszatellit-instabilitást (MSI, vagy MMR-defi ciens, mismatch repair defi - cient) mutató alcsoportja közepes mértékű válaszreakciót mutatott a pembrolizumabra, a mikroszatellit-stabil (MSS) tumorok nem reagáltak rá. Ebben a cikkben a CRC-ben az immunválaszt lehetségesen befolyásoló mechanizmusok kerülnek áttekintésre, hogy a hiszton-deacetiláz (HDAC) -gátlás visszafordíthatja-e az előrehaladott CRC-k esetén gyakran észlelt immunológiai editálást, és visszaállítja-e az immunellenőrzőpont-blokáddal szembeni szenzitivitást.
A DNS-hibajavítás hibái
Sejtjeink DNS-ében raktározódnak azok az információk, amelyek a feladataik ellátásához elengedhetetlenek. Az információkat hordozó DNS épségét, a genom integritását, meg kell őrizni. Mivel a sejtekben, főleg a DNS-ben, állandóan keletkeznek hibák, öröklöttek vagy szerzettek (külső ok pl. sugárzások, vagy belső ok pl. ROS miatt), ezért a hibák javításáról gondoskodni kell. A DNS hibái sokfélék lehetnek (bázis-, nukleotid-, mismatch-hibák, száltörések), ezért a javítás mechanizmusai is különbözőek. A hibajavító rendszernek vagy sikerül helyreállítani a normális állapotot, vagy nem, akkor pedig aktiválódik a programozott sejthalál, mert a szabályozás szerint genetikai/epigenetikai hibák nem kerülhetnek át a leánysejtekbe. Sajnos megtörténhet, hogy a hibák ellenére a sejt életben marad, ekkor a genom instabillá válhat, és megnőhet a daganatok kialakulásának esélye (pl. BRCA1 - emlő-, petefészekrák). Ilyen állapotot idézhetnek elő a hibajavító rendszer hibái, vagy a hibák mennyisége meghaladja a rendszer kapacitását. A DNS hibái természetesen nem azonos értékűek, az esetek többségében a hibák fenotípusosan meg sem jelennek, de lehetnek nagyon súlyosak, több szervet érintő szindrómák, daganatok. A kijavítatlan hibák között gyakoriak a kettős lánctörések a DNS-ben, amelyet azonban a még működő hibajavítók megpróbálnak helyrehozni. Ha azonban utóbbiakat gátoljuk, akkor a két esemény (pl. BRCA1-mutáció és PARP-gátlás) együttesen a daganatsejtek (a BRCA1-mutációt hordozók) pusztulásához vezet. Ez a stratégia a szintetikus letalitás, amelynek jelentőségét már a klinikumban is alkalmazott szer, az oliparib hatékonysága is bizonyítja. A szintetikus letalitás terápiás előnyeit új szerek, klinikai vizsgálatok igyekeznek kihasználni.
A glükokortikoid-receptorok jelentősége lupusos betegek glükokortikoidra adott terápiás válaszának meghatározásában - A Figyelő 2015;1
A szisztémás lupus erythematosus (SLE) kezelése a mai napig kihívást jelenthet mind a kezelőorvos, mind a beteg számára, a „treat-to-target”, azaz a célterápia, természetesen a remisszió elérése mellékhatások nélkül. A komplett remisszió klinikai és szerológiai tünetmentes állapotot, stabilitást jelent, amely során a beteg terápiamentes állapotban van.
Antimikrobás szerek a patikai gyakorlatban
A baktériumfertőzés esetén alkalmazható készítmények széles tárháza áll a gyógyítók rendelkezésére. Egyes csoportjaik eltérő hatásmechanizmussal pusztítják el a kórokozókat. Jelen cikkben a baktériumok sejtfalszintézisére ható gyógyszerekkel ismerkedünk meg részletesebben.
1.
2.
3.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről4.
5.
1.
2.
Klinikai Onkológia
Hasnyálmirigyrák: az ESMO klinikai gyakorlati irányelve a diagnózishoz, kezeléshez, követéshez*3.
Klinikai Onkológia
Gyógyszerbiztonsági szemelvények – a múlt tanulságai és a jövő lehetőségei4.
5.