Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 145
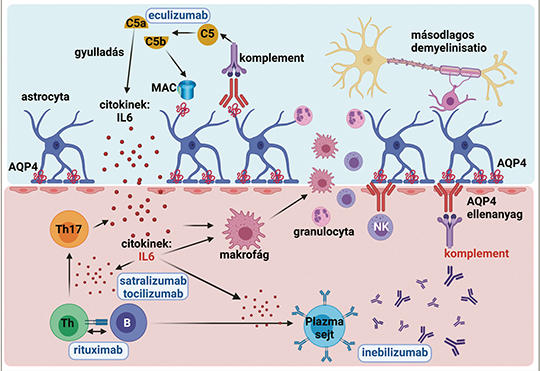
Terápiás megközelítés és új evidenciák a neuromyelitis optica spektrum kezelésében
A neuromyelitis optica spektrum betegség (NMOSD) az esetek körülbelül 80%-ában AQP4-ellenanyaggal társul. A szeronegatív betegek körülbelül negyedében a központi idegrendszeri myelin oligodendrocyta glikoprotein (MOG) ellen mutatható ki ellenanyag, és ez a kórkép a MOG-ellenanyag-asszociált betegség (MOGAD) elnevezést kapta. Jelen közlemény áttekinti az off-label azathioprin és mycophenolat mofetil, valamint az evidenciákon alapuló B- és plazmasejt-depletio, az IL-6-jelátvitel és a komplement útvonal antagonizálás klinikai aspektusait NMOSD-ben. Az összefoglaló tárgyalja az NMOSD-terápia terhességi vonatkozásait, és a MOGAD – NMOSD-től eltérő – kezelési megközelítését. Az NMOSD kezelése kapcsán az utóbbi két évben több, III. fázisú klinikai tanulmányon alapuló I. osztályú evidencia jelent meg. A monoklonális ellenanyagokkal végzett vizsgálatok a rituximab (anti-CD20), az inebilizumab (anti-CD19), a tocilizumab (anti-IL6R), a satralizumab (anti-IL6R) és az eculizumab (anti-C5) hatékonyságát és biztonságosságát jelzik egyéb immunterápiákkal kombinálva vagy monoterápiában. A MOGAD kezelését bonyolítja, hogy az esetek körülbelül fele monofázisos, és a MOG ellenanyag a betegség lefolyása során spontán vagy kezelés hatására eltűnhet. A tartós immunszuppresszió igényét MOGAD-ban a relapsusterápiát követő, leépített orális szteroidkezelés után célszerű eldönteni. NMOSD-ben a fenntartó terápia folytatása javasolt terhesség és szoptatás alatt is, és ezt az optimális kezelés kiválasztásánál fertilis nőbetegeknél figyelembe kell venni. Az új evidenciák terápiarezisztens NMOSD-ben is több lehetőséget kínálnak, és a MOGAD kezelési stratégiája is körvonalazódik.
Angiogenezis-gátlók és immunjelátviteli pontokra ható szerek kombinációja egymás hatásának potencírozására
A daganatok nem sebészi kezelésében mind az angiogenezis gátlásának, mind az immunfolyamatok befolyásolásának jelentős és egyre növekvő szerepe van. A tumoros neo-angiogenezis kedvezőtlenül befolyásolja az immunrendszer működését, ezért gátlása serkenti a kulcsfontosságú T-lymphocyták és azok működését támogató egyéb tényezők hatását, kedvezően befolyásolja a daganat mikrokörnyezetét, miközben az immunjelátviteli pontokra ható kezelés segít az érrendszer normalizálásában. A két támadáspont együttes befolyásolása ezért kedvező hatású lehet. A szerzők vesesejtes rákban, melanoma malignumban, nem kissejtes tüdőrákban, vastag- és végbél-, valamint hepatocellularis és emlőrákban mutatják be a két hatásmechanizmusú csoportba tartozó szerek alkalmazását és kombinálását, megállapítva, hogy sikerrel zárult fázis III vizsgálatok döntően a világos sejtes (vagy világos sejtes komponenst is tartalmazó) vesesejtes rákokban történtek. Hangsúlyozzák, hogy az immunterápiához általában szükséges az érzékenységet előrevetítő paraméterek (megfelelő PD-L1, MSI-H, dMMR, TMB-H) kimutatása, és a tumoragnosztikus kezelés terápiás filozófiája mellett is figyelembe kell venni a törzskönyvezett javallatokat.
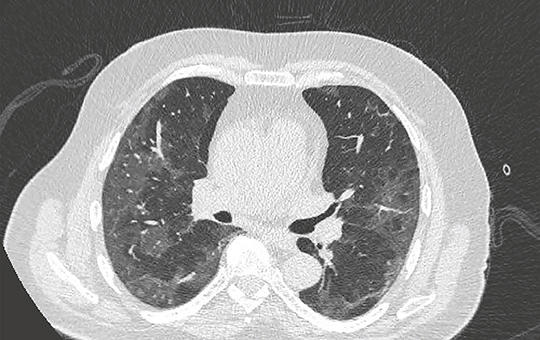
SARS-CoV-2 fertőzés okozta tüdőkárosodás. Tüdőrák és a Covid-19 a TERAVOLT vizsgálat tükrében
A Covid-19-járvány remélhetőleg vége felé, cikkünkben rövid áttekintést kívánunk adni a fertőzésről, a kórokozóról, a második hullám végére kialakult hatékonynak tűnő kezelési lehetőségekről, a tüdőkárosodásról és a TERAVOLT klinikai vizsgálatról, amely összefoglalja tüdőrákban szenvedő, kezelést kapó és/vagy nem kapó SARS-CoV-2 vírussal fertőződött betegek életkilátásait, a diagnosztika területén létrejött szabályokat (bronchoszkópia, mellkasröntgen, mellkasi CT), és néhány szóban a védőoltásokról is szó esik. A szerzők rövid áttekintést adnak a légzőszervi és daganatos betegek fertőzés alatti kezeléséről, az inhalációs készítmények, immunterápia, kemoterápia folytathatóságáról.
Tüdőrák harminc év távlatából. Gondolatok a küzdelmes múltról, a jelen eredményeiről és az ígéretes jövőről
Az elmúlt 30 évben a tüdőrák komplex kezelésében óriási fejlődés történt. Ez a fejlődés főként az utóbbi évtizedhez köthető. A tüdőrák kezelésével kapcsolatos nihilizmus már a múlté, realitássá vált az is, hogy az előrehaladott stádiumú betegek is megfelelő kezeléssel gyógyíthatóvá válhatnak, illetve betegségük folyamatos aktív daganatellenes terápia mellett krónikussá szelídíthető. Az előrehaladott stádiumban lévők harminc évvel ezelőtt elérhető 6-8 hónapos várható túlélési mutatói manapság már jelentősen növekedtek, bizonyos esetekben akár az 5 évet is meghaladhatják. Ehhez szükséges a megfelelő diagnosztikus háttér, amely lehetővé teszi a biomarkeralapú kezeléseket. Korai stádiumban alapvető a reszekciós tüdőműtét, beillesztve a komplex terápiás lehetőségeket neoadjuváns és adjuváns formában, illetőleg az új műtéti technikák is hozzájárulnak a terápiás eredmények javulásához. Elmondható ugyanez a sugárterápia vonatkozásában is. A gyógyszeres terápiás lehetőségek tekintetében is a komplex terápiás stratégia érvényesül, melyben alapvető szerepet játszanak a citotoxikus kemoterápiás, célzott kezelési és immunterápiás modalitások. A tüdőrák kezelési stratégiájának felállításában döntő szerepe van a tüdőrák-specifikus onkoteamek működésének. A jövő útját az újabb és újabb célzott terápiás lehetőségek megjelenése, az immunterápiás indikációk bővülése jelezheti a precíziós medicina alkalmazásával. Nem szabad azonban elfeledkeznünk a primer és szekunder prevencióról sem, mely a dohányzás elleni hatékony küzdelmet, illetőleg most már az evidenciává vált rizikócsoportos alacsony dózisú mellkasi CT-szűrés alkalmazását jelenti.
Hírvilág
2020. OKTÓBER 04.
Szeptember 15-e a Limfóma Világnapja
Minden év szeptember 15-e a Limfóma Világnapja. Ennek alkalmából a Magyar Rákellenes Liga ismét biciklis felvonulással kívánja felhívni a figyelmet a betegségre, annak tüneteire és a korai diagnosztizálásra.
A humán immunrendszer rendszerelvű megközelítése
A nukleotidpolimorfizmusok kutatása révén kiderült, hogy az autoimmun betegségek kialakulásában nagyon kis hatáserősséggel nagyon sok genetikai lokusz közreműködik, és itt is kiderült, hogy egy-egy kórkép molekuláris heterogenitása – pl. SLE esetén – milyen óriási. E betegségek kezelését forradalmasította a biologikumok rendszerimmunológiának köszönhető bevezetése.
A hypoxia jelentősége a rosszindulatú daganatok progressziójában: terápiás lehetőségek, út a Nobel-díjhoz
Az elmúlt évtizedek kutatásai világossá tették, hogy a malignus daganatok egyik meghatározó jellemzője hypoxiás állapotuk és az ennek következtében aktiválódó genetikai, biokémiai és biológiai programok. A felismerés jelentőségét mi sem bizonyítja jobban, mint hogy 2019-ben az orvosi Nobel- díjat ezért ítélték oda a terület meghatározó tudósainak. A daganatszövetben keletkező hypoxia fő oka a proliferációval lépést nem tartó ereződés, de másik fontos oka a daganatos beteg szisztémás hypoxiája is. A hypoxiára adandó sejtes válaszok alapja a hypoxia indukálta (transzkripciós) faktorok stabilizálódása és aktivizálódása, ami azonban daganatokban az onkogén jelpályák konstitutív aktivitása miatt is bekövetkezhet hypoxia nélkül is. A daganatos hypoxia következménye az angiogén fenotípus, a sejtmetabolizmus átprogramozódása és a daganatellenes immunológiai válaszreakciók kedvezőtlen modulációja. A daganatszövet hypoxiája azonban negatívan befolyásolja a kemo-, sugár- és immunterápia hatékonyságát is. Mindezek miatt nagy szükség lenne a daganatos hypoxia célzott terápiájára, aminek első eszközei még csak most lépnek be a klinikai gyakorlatba. Fontos megjegyezni, hogy hazai kutatócsoportok nemzetközileg is elismert eredményekkel járultak hozzá ismereteink bővüléséhez ezen a területen.
Beköszöntő - Kedves Kollégák!
Mondhatjuk, hogy a nyár és a Covid-19-pandémia közepén, a járvány lélegzetvételnyi szünetében, jólesik az immunterápia lehetőségein tépelődni. Ebben a számban nem is tudjuk elkerülni, hogy ne vessünk egy pillantást azokra a közleményekre, amelyek az immunterápia bevezetése és a Covid-19-fertőzés dilemmájáról szólnak. Nagykálnai Tamás, Kitekintő rovatunk egyik szerzője irányítja rá a figyelmet a témára. Megjelentek közlemények már márciusban arról, hogy az ICI-k hatásmechanizmusa és a Covid-19-fertőzés együttesen végzetes kimenetelű immun-hiperaktivitást okozhat, de mindenképpen megnő az amúgy ritkán észlelt halálos kimenetelű immunpneumonitis veszélye.
Van-e hatásosságbeli különbség a PD-1, illetve PD-L1 gátlók között szolid tumorok esetén?
Az immunterápia, ezen belül különösen az immunellenőrzőpont-gátlók (ICI), amelyek a programozott sejthalál receptor-1 (PD- 1) és PD-ligand 1-et (PD-L1) célozzák meg, számos daganatféleségben a rákterápiának az egyik legfontosabb áttörését jelentik. A klinikai vizsgálatok növekvő számával egyre több összefoglaló érhető el az anti-PD-1 és az anti-PD-L1 kezelések eltérő klinikai hatásosságát illetően.
Kutatások a hatékonyabb kezelésért - Interjú Ostoros Gyulával
„Az immunterápia forradalmasította a rákgyógyítást, két Nobel-díjas kutató Is döntően járult hozzá ehhez, amely Aztán viszonylag rövid időn belül már Közvetlenül a betegellátásban javítja a daganatos betegek életkilátásait” – ezt állítja Ostoros Gyula
1.
2.
3.
4.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről5.
1.
2.
Klinikai Onkológia
A rosszindulatú daganatok fenotípusának plaszticitása és az immunogén mimikri3.
Klinikai Onkológia
A szarkopénia mérése komputertomográfiával és jelentősége az onkológiai betegeknél4.
5.