Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 322
Az ezetimib + statin kombináció hatása a nem alkoholos zsírmájra
A nem alkoholos zsírmáj betegség (non-alcoholic fatty liver disease, NAFLD) gyakorisága világszerte növekedést mutat, és szoros összefüggésben áll a metabolikus szindróma jellemzőivel, beleértve az obesitast, az inzulinrezisztenciát, a dyslipidaemiát és a diabetes mellitust. Az NAFLD-ben szenvedő betegek körében a mortalitás fő okát a cardiovascularis (CV) betegségek jelentik.
A rosszindulatú daganatos fájdalom kezelése gyógyszerekkel és idegblokádokkal
A WHO szakértői 1986-ban fogalmazták meg a daganatos fájdalomcsillapítás alapelveit, amelynek lényege a kombinált gyógyszeres fájdalomcsillapítás, mert ez mindenütt kivitelezhető. Gyógyszeres fájdalomcsillapításra javasolt: minor analgetikum, gyenge opioid, erős opioid, és minden esetben úgynevezett adjuváns analgetikum. Kínzó daganatos fájdalom esetén azonnal erős opioid analgetikumot kell rendelni, nem szabad szenvedni hagyni a betegeket a gyengébb szerek kombinációjával.
Rezisztens és szekunder hypertoniák
A hypertonia a cardiovascularis események és halálozás vezető rizikófaktora világszerte. A terápiarezisztens hypertonia esetében a terápia ellenére fokozott a hypertoniával összefüggő cardiovascularis és renalis morbiditás. A valódi terápiarezisztens hypertoniában a szekunder hypertonia prevalenciája rendkívül magas. Mivel az időben történő adekvát kezelés nélkül nemritkán súlyos szövődmények várhatók.
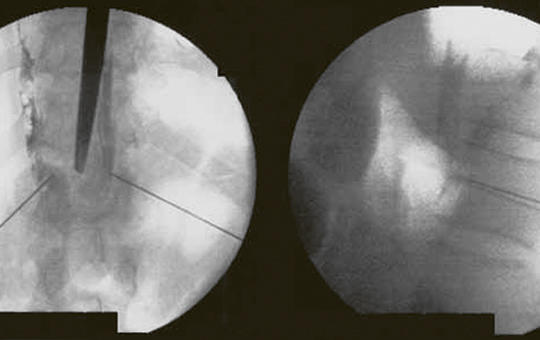
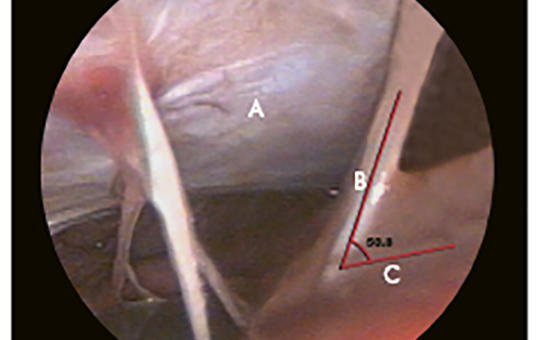
[A trochlearis ideg agytörzsi és cisternalis szegmensének endoszkópasszisztált craniometricus cadavervizsgálata ]
[Vizsgálatunk célja a trochlearis ideg és a neurovascularis struktúrák kapcsolatának feltárása volt craniometriás mérések segítségével. Célunk volt a trochlearis ideg lefutásának megértése és ezáltal az ideg sérülésének minimalizálása a sebészi beavatkozások során. Tíz friss cadaver húsz trochlearis idegét tanulmányoztuk bilateralisan endoszkópos segítséggel, lateralis infratentorialis-supracerebellaris és kombinált praesigmoidalis-subtemporalis transtentorialis megközelítésekből. A trochlearis idegeket mindkét oldalon feltártuk, és megmértük a következő hét paraméterüket: a trochlearis ideg cisternalis szegmense és az érstruktúrák (arteria cerebellaris superior és arteria cerebellaris posterior) közötti távolság; a trochlearis ideg eredete az agytörzsben; a tentorialis junctio szintjén mért szög; hossz; átmérő; a trochlearis ideg hossza a cisternalis szegmensben. Azonosítottuk az agytörzset és a trochlearis ideg cisternalis szegmensét. A lateralis infratentorialis-supracerebellaris megközelítés lehetővé tette a cisternalis szegmens (cruralis és ambiens cisternák) feltárását, ezen belül az ideg agytörzsi eredetének feltárását. A kombinált praesigmoidalis-subtemporalis transtentorialis megközelítés lehetővé tette az ideg cisternalis szegmensének és a tentorium szabad szélének vizualizálását. Mérésünk szerint a trochlearis ideg cisternalis szegmensének átlagos hossza és átmérője 30,3 és 0,74 mm volt. A trochlearis ideg hossza az eredetétől a durába lépéséig 37,2 mm volt. A trochlearis ideg tentorialis durába lépési szöge és az agytörzsből való kilépési szöge 127,0 fok, illetve 54 fok volt. A trochlearis ideg és az arteria cerebellaris posterior közötti távolság az ambiens cisterna közepén 7,3 mm volt. A trochlearis ideg és az arteria cerebellaris anterior közötti távolság az ambiens cisterna közepén 6,8 mm volt. A trochlearis ideg gyakran megsérül a sebészeti beavatkozások során. Ezt megelőzendő, fontos cisternalis szegmense anatómiájának pontos ismerete és az ideg neurovascularis struktúrákkal való kapcsolatának feltárása. A trochlearis ideg sérülésének minimalizálása érdekében a középső és a hátulsó koponyaalap műtétei során hasznos az ideg anatómiai és craniometriás adatainak ismerete. ]
Idegtudományok
2022. JÚLIUS 07.
Thrombectomia versus bridging-terápia ischaemiás stroke-ban
Az elmúlt években több randomizált, kontrollált vizsgálat hasonlította össze ischaemiás stroke-ban a kizárólagos intravénás thrombolysis és az úgynevezett kombinált bridging (áthidaló) terápia hatékonyságát, mely során az intravénás thrombolysist (IVT) endovascularis thrombectomia (EVT) követi. A vizsgálatok során a bridging terápia egyértelműen jobb eredményeket mutatott, mint a kizárólagos thrombolysis. A vizsgálatok alapján ajánlásaikban mind az amerikai, mind pedig az európai stroke-társaságok nagyérelzáródás esetén a tünetek kezdetétől számított 4 és fél órán belül az EVT-t megelőzően IVT elindítását javasolják. Ugyanakkor IVT mellett az EVT megkezdése előtti rekanalizáció aránya meglehetősen ritka (a fenti vizsgálatokat összesítő HERMES vizsgálatban ez az arány mindössze 7,6%). Noha az IVT-nek lehet egy thrombectomiát segítő hatása, az IVT alvadékfragmentációt és következményes distalis migrációt okozhat (azaz a széteső thrombus darabjai a távolabbi erekbe sodródhatnak), mely esetleg EVT-vel már nem kezelhető. A reperfúzió mértéke erős korrelációt mutat a klinikai kimenetellel, az viszont eddig nem volt ismert, hogy a távoli embolusok esetleges felszámolásából származó előny IVT mellett ellensúlyozza-e az EVT-re már nem alkalmas esetek számának potenciális növekedését. Mindemellett az IVT fokozhatja a tünetes intracerebralis vérzés (sICH) rizikóját is. A fent említett vizsgálatok adatai alapján sajnos ebben a kérdésben ellentmondásosak az eredmények.
Egytablettás fix kombinációk napi kétszeri alkalmazása a hypertonia kezelésében
A vérnyomáscsökkentő terápia optimalizálása legtöbbször nem a terápia egyszerűsítését jelenti. A legtöbb, napjainkban alkalmazott vérnyomáscsökkentő az alkalmazási előirat szerint 24 órás hatású, sok beteg esetében mégsem képesek megfelelő vérnyomáscsökkenést biztosítani. A kezelt hypertoniás betegek között azoknál fordul elő nagyobb arányban a nondipper jelenség, akik minden vérnyomáscsökkentőjüket egyszerre, reggel veszik be. A legújabb bizonyítékok arra utalnak, hogy jobb vérnyomáscsökkentő eredmények érhetők el akkor, ha az ACEi-ket, illetve az ARB-ket este adagolják és nem reggel. Arról nagyon kevés adat áll rendelkezésre – evidencia meg gyakorlatilag nem –, hogy egytablettás fix kombinációs készítményeket adagolnának naponta kétszer, akár ugyanabban a formában azonos vagy különböző adagban, akár két különböző kombinált készítményt.
Agresszív lefolyású akut sclerosis multiplexes beteg sikeres kombinált (plazmaferézis és alemtuzumab) kezelése
A sclerosis multiplex (SM) diagnosztikus és terápiás protokollja az utóbbi 3-4 évben jelentősen megváltozott. Az ECTRIMS 2020-ban közölt ajánlása meghatározta a magas betegségaktivitású SM -enotípus nomenklatúráját, diagnosztikus és terápiás protokollját. Ezt a fenotípust az ECTRIMS 2020 „agresszív SM”-ként definiálja, mely kórformát gyakori, súlyos relapszusok, rapid progresszió, magas gyulladásos és neurodegeneratív aktivitás jellemez.
Gyermek- és felnőttkori high-grade gliomák komplex genetikai karakterizálása újgenerációs szekvenálással: Tapasztalatok és kutatási irányok
A központi idegrendszeri tumorok újgenerációs szekvenáláson (next-generation sequencing – NGS) alapuló panelek segítségével végzett komprehenzív genetikai analízise a terápiás célpontok keresése mellett a patogenezis egyre pontosabb megismerését teszi lehetővé.
A célzott kezelések „célzott” mellékhatásai
A célzott gyógyszerek nem elég célzottak, gyakran a normális gének termékeire is hatnak, vagy nem elég szelektívek a mutáns változatokra, így egyáltalán nem elhanyagolható és sajátos mellékhatásaik vannak, aminek patomechanizmusát érdemes ismerni, mert általa a mellékhatások megelőzése vagy „célzott” kezelése lehetséges. Miután a célzott kezelések molekuláris mechanizmusai igen eltérők, ezen mellékhatások spektruma is széles és nagyon eltérő a hagyományos kemoterápiás szerekhez hasonlítva. Az angiogenezisgátlók mellékhatásai a VEGF-mediált folyamatok zavarai (vérzés, sebgyógyulás, vérnyomás-szabályozás), a csontáttét kezelésében használt szerek csontregenerációs zavarokhoz vezetnek az osteoclastfunkció blokkolásával, a HER-2-gátlók szelektív szívizom-károsítók lehetnek, mert ez a receptor kulcsfontosságú az izomregenerációban. Mivel az EGFR a felszíni hám folyamatos megújulásának fő szabályozója, az anti-EGFR-szerek bőrmellékhatásai csaknem természetesek. A multikináz-inhibitorok két fontos célpontja a csontvelő (a KIT kulcsszerepe miatt), illetve a melanocita (hasonló okokból). Az új TRK-inhibitorok esetében idegrendszeri mellékhatások léptek fel, miután az idegsejtek fontos szabályozója az NTRK. A mutáns BRAF-inhibitorok, sajnos, csak szelektívek, és alkalmazásuk során másodlagos, elsősorban RAS-mutáns daganatok keletkezése várható a RAS-RAF-MEK jelpálya sajátos visszacsatolási reakciói eredményeként. A lipidkináz-jelpálya különböző inhibitorai (PI3K, AKT vagy mTOR) megint csak jellegzetes mellékhatásokkal járnak, mint a hyperglykaemia vagy a hyperlipidaemia. Végül az immunellenőrzőpont-gátlók a daganatellenes immunválasz felszabadítása mellett, eddig kontroll alatt levő autoimmun mechanizmusokat is aktiválnak, amelyek adott esetben súlyosak is lehetnek vagy eddig még nem ismert formában manifesztálódnak (hypophysitis).
Idegtudományok
2022. MÁRCIUS 16.
Agitáció kezelése ketaminnal sürgősségi osztályon
A ketamin egy nem kompetitív NMDA-receptor-antagonista, mely alacsony adagban fájdalomcsillapító hatású, magasabb dózistartományban pedig disszociatív szedációt okoz, ezért procedurális és általános szedatívumként is alkalmazható. Gyors hatásbeállás, kedvező kardiovaszkuláris hatások és a légzési drive megtartása miatt, melyet az alkalmazásához társuló ritka cardiopulmonaris szövődményráta is igazol, a ketamin jó választás lehet gyors, biztonságos, agitált vagy erőszakos betegekben alkalmazható szedatívumként is.
1.
2.
3.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről4.
5.
1.
2.
Klinikai Onkológia
Hasnyálmirigyrák: az ESMO klinikai gyakorlati irányelve a diagnózishoz, kezeléshez, követéshez*3.
Klinikai Onkológia
Gyógyszerbiztonsági szemelvények – a múlt tanulságai és a jövő lehetőségei4.
5.