Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 152
Idegtudományok
2021. NOVEMBER 11.
A hosszú távú fluoxetinkezelés alapvetően megváltoztatja az agyi lipidösszetételt
A hosszú távú fluoxetinhasználat feltételezhető agyfejlődési zavart okozó hatásának mechanizmusát próbálták kideríteni német és orosz kutatók fiatal majmokat vizsgálva. Az International Journal of Molecular Sciences című szaklapban megjelent kutatás eredménye szerint a hosszú távú fluoxetinkezelés több mint százféle lipid agyi mennyiségének szignifikáns változásával jár együtt, különösen jelentős az idegsejtnyúlványok myelinisatiójában központi szerepet játszó, többszörösen telítetlen zsírsavak mennyiségének csökkenése. A többszörösen telítetlen zsírsavak anyagcseréjének változása azért is különös figyelmet érdemel, mert a közelmúltban kiderült: ezek a molekulák, illetve hiányuk szerepet játszik a pszichiátriai betegségek, a bipoláris és major depresszív kórkép, valamint a szkizofrénia patogenezisében.
Az immunrendszer öregedése
Az elmúlt évtizedben megtudtuk, hogy az öregedést mind az osztódó, mind a nem osztódó sejtekben az epigenetikai információk változásai kísérik, ez az immunrendszer különböző sejtjeire, illetve magára az immunválaszra is igaz. Az epigenetikai változások különböző szinteken fordulnak elő, ideértve a hiszton poszttranszlációs módosítá- sainak és a DNS metilációjának megváltozott mintáit és a megváltozott nem kódoló RNS- (például mikro-RNS-) expressziót, a telomeráz/telomer rendszer változásait és az autofágia szintjének módosulását az öregedés során. Az egészséges immunválaszban a memória-T- és -B-sejtek szintjének immungerontológiai változása mögött álló epigenetikai változásokról is új adatokat tudtunk meg. Ide tartozik a Covid-járvány első három hullámában kimutatott, életkorfüggő citokinvihar jelensége is. Meglepő módon, bizonyos típusú epigenetikai információk transzgenerációs módon működhetnek, és befolyásolják az utódok élettartamát. Ez azt jelenti, hogy a kizárólagos genetikai meghatározottság helyett az immunválasz elsősorban epigenetikailag meghatározott; az étrend és más környezeti hatások (fertőzések, gyógyszerek) az epigenetikai információk megváltoztatásával befolyásolhatják az immunválasz időtartamát. Az utóbbi nagyon lényeges a vakcinák védőhatásának időtartamát illetően is.
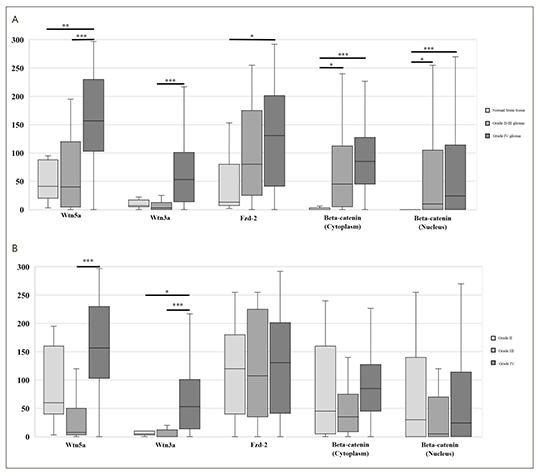
[Wnt-útvonalmarkerek alacsony és magas grádiusú gliomákban]
[A glioma kialakulásában szerepet játszik a Wnt-útvonal aberráns aktiválása az őssejtek differenciálódásának és fenntartásának szabályozása által. Kutatásunk célja volt meghatározni, hogy egyes Wnt-markerek milyen mértékben expresszálódnak a különböző grádiusú, szövettani eredetű és mutációs profilú gliomákban. Kilenc grádius II., 10 grádius III. és 72 grádius IV., műtéti úton eltávolított, formalinfixált paraffinba ágyazott gliomát vizsgáltunk. Az IDH1 132 kodon mutációs állapotát immunhisztokémia és piroszekvenálás módszereivel határoztuk meg minden tumorban. A II. és III. grádiusú astroglialis és oligodendroglialis tumorokat tovább vizsgáltuk p53- és ATRX-expresszióra immunhisztokémiával, és 1p19q kodelécióra fluoreszcens in situ hibridizációval. A nem kanonikus Wnt5a és Fzd2, valamint a kanonikus Wnt3a és β-katenin Wnt-útvonalmarkerek expressziós szintjét immunhisztokémiai úton határoztuk meg, és az expressziós értékeket összehasonlítottuk a tumorok grádiusa, hisztológiai eredete (asztrocitoid vs. oligodendroglioid) és az IDH1 R132H / C mutációk jelenléte vagy hiánya szerinti alcsoportokban. A normál agyi szövet vs. II–IV. grádiusú gliomák összehasonlítása során egy grádius szerinti fokozatos növekedést figyeltünk meg a Wnt5a, Wnt3a, Fzd2 és a β-katenin expressziójában. A II. és III. grádiusú gliomák astroglialis és oligodendroglialis szövettani eredetű összehasonlítása során csak a Wnt5a-expresszió volt szignifikánsan magasabb az asztroglia-alcsoportban. Az IDH1 R132H / C mutáns és vad típusú gliomák összehasonlítása során a Wnt3 emelkedését találtuk a vad típusú grade II–IV. gliomák csoportjában. Ezek az adatok kibővítik a korábbi megfigyelések eredményeit, és összefüggést mutatnak a Wnt-útvonal aktivitása, valamint a gliomagrádius között. A Wnt-markerek expressziós szabályozásának további vizsgálata gliomákban már folyamatban van szövettani eredet vagy IDH-génmutációs státusz szerint, nagy felbontású molekuláris vizsgálatok alkalmazásával.]
RAAS-gátló kezelés – Covid-pandémia
A SARS-CoV-2 okozta különböző méretű és lefolyású akut légzési szindróma ma az egészségügyi rendszerek legnagyobb kihívása világszerte. A Covid-19 klinikai képének kialakulásában döntő szerepe van a renin-angiotenzin-aldoszteron, valamint a kinin-kallikrein rendszernek, illetve ezen rendszereken belül két endopeptidáznak, az ACE és ACE-2 enzimeknek. Az ACE által stimulált Ang II/AT1R tengely káros hatásait (oxidáns, gyulladáskeltő hatás, vasoconstrictio) az ACE-2 által indukált AT2R- és MasR-aktivitás (antioxidáns, gyulladáscsökkentő hatás, vasodilatatio) ellensúlyozza. A SARS-CoV-2 azért okoz ilyen súlyos tüdő- és szisztémás gyulladást, mert az ACE-2-t, mint a tüdő fontos védelmi tényezőjét, károsítja a SARS-CoV-2 fehérjetüskéje az ACE-2-höz kötődéssel, ami az ACE-2-szint csökkenéséhez vezet. Ezzel párhuzamosan fokozott a bradikinintermelődés, amely a BKB1- és BKB2-receptorok révén ugyancsak erősíti a SARS-CoV-2 gerjesztette citokinvihart. Mivel a RAAS-gátló szerek (ACEI, ARB) különböző támadási helyeken és különböző mértékben befolyásolják a két említett szabályozó rendszert és enzimeket, sürgős volt szerepük tisztázása a Covid-fertőzés során, hiszen alkalmazásuk igen kiterjedt és nélkülözhetetlen pillére számos népbetegségnek (hypertonia, cardiorenalis anyagcsere-betegségek). A patofiziológiai és kísérletes adatok alapján jogosan feltételezhető, hogy Covid-fertőzésben a társbetegségekkel járó esetekben – kifejezetten az idős egyéneknél – a csökkent ACE-2-expressziót a RAAS-gátlók helyreállíthatják, és újra érvényesülni tud az elmaradt, vagy csökkent védőhatás. Ez a védőhatás mindkét RAAS-gátlóra érvényes. A klinikai vizsgálatok egyértelműen alátámasztják a különböző nemzetközi társaságok deklarált véleményét, miszerint a RAAS-gátlók alkalmazása nem növeli a Covid-19-előfordulást, illetve a súlyos, kritikus Covid-betegek megjelenésének kockázatát. Ennek értelmében az elindított RAAS-gátló kezelést folytatni lehet és szükséges a Covid-19 betegség kialakulása folyamán.
A MeCP2 szerepe a ketamin-jelátvitelben
A ketamin antidepresszáns hatásai két évtizede ismertek, az FDA pedig 2019-ben engedélyezte a gyógyszer használatát egyéb terápiás modalitásokkal szemben rezisztenciát mutató depresszió esetében. A ketamin két szempontból is különleges szer: egyrészt a gyógyszer hatásmechanizmusa eltér a hagyományos monoaminerg transzmisszióra ható szerekétől, másrészt pedig a ketamin már a kezeléstől számított néhány órán belül képes a depresszió tüneteinek enyhítésére. Fontos ugyanakkor megemlíteni, hogy a gyógyszer hosszú távú hatása egyénfüggő, ugyanakkor ezeknek az egyéni különbségeknek a molekuláris háttere egyelőre nem ismert.
Klinikum
2021. JÚNIUS 21.
Az immunitás nemi különbségeinek hatása a vakcinafejlesztésre
Bár a vakcináció az egyik legsikeresebb közegészségügyi intervenció, a klasszikus vakcinafejlesztés leginkább empirikus alapokon folyik, a vakcinák biztonságossági és immunogenitási profilja patogénspecifikus. Az oltási rezsimek minden beoltandó számára ugyanazt az oltást ajánlják, holott jól ismert: a beoltott egyén sajátosságai – életkor, nem, komorbiditások, egyéb infekciók, mikrobiom – jelentősen befolyásolják a vakcinációra adott individuális választ. A Frontiers in Immunology összefoglaló közleménye áttekinti a férfi, illetve női nem hatását az oltásokkal kapcsolatos immunválaszra, és az „ugyanazt az oltást mindenkinek”, illetve az „egy kórokozó, egy vakcina” szemlélet helyett a különböző populációkat figyelembe vevő oltásfejlesztési és oltási stratégia mellett érvel.
Lipidcsökkentés Covid-19-járvány alatt
A Covid-19-világjárvány mindenütt nagy kihívás elé állította az egészségügyet. Ennek fő oka a fertőzöttek nagy száma mellett az is, hogy olyan új helyzetet teremtett, amelynek megoldására nem voltak korábbi tapasztalatok. Különösen azoknak az orvosoknak hiányozhattak ezek a tapasztalatok, akik megszokták, hogy az általuk alkalmazott terápia mögött klinikai vizsgálati bizonyítékok sorakoznak, azaz a napi munkájukat a bizonyítékokon alapuló orvoslás elvei szerint végzik. A fertőzöttek kezelésére vonatkozóan folyamatosan gyarapodnak azok az új megfigyelések és javaslatok, amelyek a sürgősség miatt nem mindig voltak kellően megalapozottak. Ebben a helyzetben a kezelőorvosokban gyakran felmerülhet, hogy mi legyen a beteg korábbi gyógyszerezésével, amikor egy potenciálisan életveszélyes fertőzés kezelésére kellene fókuszálni. Ilyenkor még gyakrabban maradhat el olyan, eleve mostohán és gyakran félvállról végzett terápia, mint a lipidcsökkentés. A magas koleszterinszint csökkentésének alapgyógyszerei a statinok. Ezeket a koleszterinszint és a cardiovascularis események gyakoriságának csökkentésére alkalmazzuk, de emellett a vírusfertőzésre is kedvező hatással vannak. Ebben a statinok jól ismert gyulladáscsökkentő hatásán és az angiotenzinkonvertáló-enzim-2 expressziójának fokozásán túl egyéb mechanizmusok is szerepet játszanak. Ilyen lehet – egyebek mellett – az a hatás, amely elősegíti a lipidraftok lebontását, direkt módon gátolva az S-proteinen át a vírus sejtbe kerülését azzal, hogy a folyamathoz szükséges koleszterin mennyiségét csökkenti. Több mint 1200 SARS-CoV-2-fertőzött, statinnal kezelt betegen a 28-ik napnál 48%-kal alacsonyabb volt az összhalálozás, mint statint nem szedőkön. Egy közel kilencezer fő adatait feldolgozó metaanalízis szerint Covid-19-fertőzöttek körében a statint szedőknél 30%-kal kisebb volt a halálozás vagy a súlyos szövődmények aránya. Az eddigi megfigyeléses vizsgálatok azt támasztják alá, hogy a statinterápiát és a többi lipidcsökkentő szer adását Covid-19 betegség alatt is az irányelveknek megfelelően kell folytatni vagy elkezdeni.
miRNS-alapú terápiák idegrendszeri betegségekben: lehetőségek és kihívások
22 évvel azután, hogy kiderült: bármely gén elcsendesíthető, tucatnyi klinikai vizsgálat elemzi a miRNS-mimetikumok és -inhibitorok terápiás hatását. A módszert az idegrendszeri betegségek közül a neurodegeneratív kórképek, az epilepszia, az agytumorok és a cerebrális ischaemia kezelésében vizsgálják.
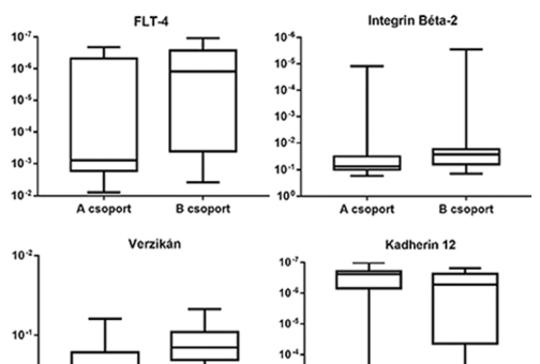
Az inváziós spektrum prognosztikai jelentősége glioblastomában
A glioblastoma a leggyakoribb központi idegrendszeri rosszindulatú daganat; sebészi kezelése a daganatok invazív jellegénél fogva nem lehetséges, onkoterápiája pedig csupán szerény eredményeket hoz – a betegek átlagos teljes túlélése (OS) 16–24 hónap. A betegek egy része alig reagál az alkalmazott kezelésre; a klinikumban jelenleg nincs olyan prognosztikai vagy prediktív marker, ami segítené a betegek túlélésében tapasztalható jelentős szórás érdemi feltérképezését és a kezelési algoritmus optimalizálását. Jelen kutatásban az invázióban szerepet játszó extracelluláris mátrix (ECM-) molekulák expressziójának prognosztikai jelentőségét kívántuk meghatározni. Eltérő prognózisú betegcsoportokat létrehozva (A csoport OS < 16 hónap, B csoport OS > 16 hónap) vizsgáltuk meg glioblastomás betegek gyorsfagyasztott tumormintáiban a szakirodalom által jelenleg elismert markerek (IDH1 mutációs és MGMT metilációs státusz) jelenlétét, továbbá 46 inváziós ECM-molekula mRNS-szintjét. A DE KK Idegsebészeti Klinikán operált és az Onkológiai Klinikán utókezelt betegek klinikai adatai nem mutattak jelentős különbségeket a túlélési adatokat (progressziómentes és teljes túlélés) és a reoperációs arányt leszámítva. Minden minta IDH vad típusú volt. Jelentős különbség volt a jobb és a rosszabb túlélésű betegek között az MGMT promoter hipermetiláció arányában (28,6% vs. 68,8%). Az inváziós ECM-molekulák expressziós mintázata, az inváziós spektrum szintén jelentős különbséget mutatott; szignifikáns különbség mutatkozott az integrin β2, kadherin-12, FLT4/VEGFR-3, verzikán molekulák expressziójában. Az inváziós spektrum megbízhatóságát statisztikai osztályozóval tesztelve a módszer a minták 83,3%-át sorolta a megfelelő prognosztikai csoportba (PPÉ: 0,93). A különböző túlélésű betegcsoportok összehasonlítása során a reoperációs arányban megfigyelhető különbség az irodalmi adatokkal összevágó tény. Az MGMT promoter metiláltságának vizsgálata hazai újdonság, az eredmény az eddigi ismereteket megerősítve sürgeti a vizsgálat rutinszerű bevezetését. Az inváziós spektrum vizsgálata többletinformációt ad a tumorról, prognosztikai markerként segíthet felismerni az agresszívabb tumorokat, továbbá felhívja a figyelmet az antiinvazív ágensek jövőbeni használatának szükségességére a GBM terápiájában.
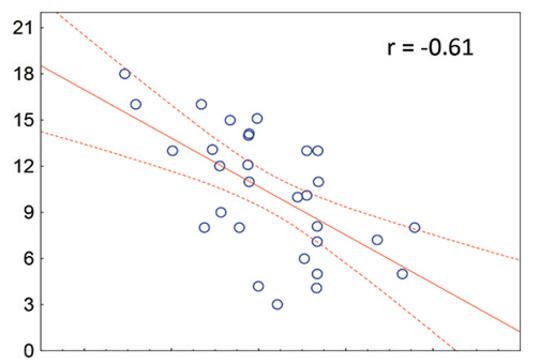
[TLR4- (Toll-like recetor-4-) expresszió és a frontocingularis régió térfogata szkizofréniában]
[Egyes patogénhez asszociált molekuláris mintázatfelismerő receptorok (Toll-like receptors, TLR) szerepet játszhatnak a szkizofrénia patogenezisében. Ezek a receptorok nemcsak a perifériás immunválaszban, de a neuroplaszticitás szabályozásában is fontosak. Ennek ellenére a perifériás TLR-expresszió és a szkizofréniára jellemző strukturális agyi eltérések közötti összefüggés nem ismert. A kérdés megválaszolására vizsgálatunkba 30 gyógyszermentes, első pszichotikus epizódját átélő szkizofrén beteget vontunk be. A TLR4+/TLR1+ monocytákat áramlási citometria segítségével detektáltuk. A résztvevőkről nagy felbontású agyi strukturális mágnesesrezonancia-felvételeket (T1 MR) készítettünk, amelyeket FreeSurfer szoftver segítségével értékeltünk ki, meghatározva a regionális agyi térfogatértékeket. Eredményeink szerint szignifikáns negatív korreláció mutatkozott a TLR4+ monocyták százalékos megoszlása és átlagos fluoreszcens intenzitása, valamint a frontális területek és az anterior cingulum térfogata között. Hasonló összefüggést TLR1+ monocyták esetében nem találtunk. Az eredmények felvetik annak a lehetőségét, hogy a kóros TLR-aktiváció hozzájárul a szkizofréniára jellemző regionális agyi térfogatcsökkenéshez.]
1.
2.
3.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről4.
5.
1.
2.
Klinikai Onkológia
Hasnyálmirigyrák: az ESMO klinikai gyakorlati irányelve a diagnózishoz, kezeléshez, követéshez*3.
Klinikai Onkológia
Gyógyszerbiztonsági szemelvények – a múlt tanulságai és a jövő lehetőségei4.
5.