Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 208
Lágyrész-sarcomák korszerű gyógyszeres kezelése
Adjuváns kezelésként az ismert standard doxorubicin-monoterápia vagy a doxorubicin + ifoszfamid kombináció az elfogadott a legtöbb esetben. Letisztult irányelv még nem jött létre, azokban az esetekben javasolt az adjuváns kezelés, akiknek nagyobb, mint 10 cm méretű, high grade sarcomájuk volt, a műtét nem volt kellően radikális, illetve radioterápia sem jöhet szóba. A lokálisan előrehaladott tumorok esetében végtagmegtartás miatt izolált végtagi perfúzió javasolható. Új vegyületként a helyi kezelésben alkalmazható hefnium-oxid nanopartikulumok (NBTXR3) intratumorális befecskendezése és sugárkezeléssel való kombinációja lehet iránymutató, azonban további vizsgálatok szükségesek. Metasztatikus tumorok gyógyításában a standard terápia mellett egyre inkább előtérbe kerülnek a célzott, új kezelések: leiomyosarcomában a trabectedin mellett a pazopanib és az olaratumab; liposarcomában a trabectedin és az eribulin; synoviosarcomában a pazopanib; imatinibrezisztens GIST esetében a sunitinib és a regorafenib. A lágyrész-sarcomák heterogén szövettani altípusokba sorolhatók, ritka daganatok, amelyek kezelésében kulcsfontosságú a szövettani altípus szerinti kezelés, valamint az interdiszciplináris együttműködés az ortopéd sebésszel, a sugárterapeutával és a patológussal az egyénre szabott megfelelő terápia meghatározásáért.
Malignus daganatos megbetegedések okozta neurológiai kórképek
Az onkológiai betegségek okozta neurológiai tünetek, tünetegyüttesek egy szerteágazó etiológiájú heterogén klinikai entitás, amely érintheti a központi és perifériás idegrendszert, lehet primer vagy szekunder, de létrejöhet akár immunmediált folyamatok útján is. Összefoglaló cikkünkben áttekintjük az onkológiai gyakorlatban előforduló neurológiai kórképeket és vezető tüneteket. Kiemelten tárgyaljuk a háttérben álló leggyakoribb daganatként az agyi metasztázisokat, amelyek jelenleg az új célzott és immunterápiák fókuszpontjába kerültek, s napjainkban is egyre bővül azon szerek köre, amelyek intracranialis aktivitást mutatnak. Részletezzük a daganatok okozta paraneoplasiás neurológiai szindrómákat, mert bár ritkák, de egyre jobban diagnosztizálhatók, és gyors felismerésük elengedhetetlen a háttérben álló daganatos folyamat detektálásában. Végül a tumorok kezelésének mellékhatásaként újabban megfi gyelhető neurológiai tüneteket ismertetjük, mint a PD1-gátló immunterápiák következtében közel 3%-ban fellépő neurológiai szövődmények. Nem megfeledkezve a kemoterápiák okozta polyneuropathiákról és a tüneti terápiaként alkalmazott antikonvulzív terápiás indikációkról.
Széchényi díjatt kapott Kásler Miklós
Rendkívül megtisztelő a kitüntetés, hiszen Széchenyi Istvánról kapta a nevét, aki történelmünk folyamán talán a legtöbbet tette a magyarságért - mondta el az MTI-nek Kásler Miklós onkológus
A szervtranszplantáció és a malignus daganatok
Mind a szervátültetés, mind az onkológia a közelmúltban olyan fejlődésen ment és megy jelenleg is keresztül, ami a transzplantáció korábban már megválaszolt, onkológiával kapcsolatos kérdéseit új megvilágításba helyezte, és szükségessé tette a válaszok revízióját. Így például, a „donor pool” bővítésének szándékával napjainkban valós kérdéssé vált, hogy mely esetekben végezhetünk szervátültetést daganatos anamnézisű donorból, úgy, hogy a tumor grafttal történő átvitelének és a recipiensben való manifesztációjának minimális legyen a kockázata. A másik, egyre gyakoribb kérdés, hogy szabad-e, és ha igen, hány év tumormentes túlélés után lehet olyan beteget transzplantálni, akinek rosszindulatú daganat szerepel a kórtörténetében. A modern immunszuppresszív kezelés eredményeként a szervtranszplantált betegek mind hosszabb ideig élnek. Az immunszupprimált állapot idejével arányosan növekszik azonban a rosszindulatú daganatok kialakulásának a kockázata, arányuk hosszú távon elérheti a 20-30%-ot is. A poszttranszplantációs „de novo” tumorok jelentőségét jelzi, hogy a transzplantált betegek vezető haláloki tényezőjévé váltak. A rosszindulatú daganatok tehát több szempontból is komoly problémát jelentenek. Megoldásuk alapfeltétele az onkológusok és a transzplantáció terén jártas szakemberek együttműködése, a megújult ismereteken alapuló közös gondolkodás és az egyénre szabott döntéshozatal.
Haemopoeticus őssejt-transzplantáció gyermekkori nem hematológiai szolid tumorokban
A nagy dózisú kemoterápiát követő autológ őssejt-átültetést és az allogén őssejttranszplantációt mintegy három évtizede alkalmazzák a gyermekkori nem hematológiai szolid tumorok kezelésében. Az autológ őssejt-transzplantáció számos rossz prognózisú kemoszenzitív daganattípus esetében a standard primer kezelés részévé vált (neuroblastoma, Ewing-sarcoma, medulloblastoma), számos betegségben recidiváló és refrakter esetek egy részében hatékonyan alkalmazhatóak (csírasejtes daganatok, Wilms-tumor). A csökkentett intenzitású kondicionálással végzett allogén őssejt-transzplantációk nem váltották be a hozzájuk fűződő reményeket a nem hematológiai szolid tumorok esetében. Jelen tanulmányban részletesen elemezzük az autológ és allogén transzplantáció helyét a különböző szolid tumorok kezelésében.
MEK és ERK - RAS és RAF ellen
A célzott terápia kezdeti klinikai hatása után a legtöbb esetben a tumor rezisztenssé válik a kezeléssel szemben, aminek megfordítása jelenleg az egyik legnagyobb probléma a klinikai onkológiai gyakorlatban. Ennek a szekunder rezisztenciának sok oka lehet, pl. új driver mutáció jelenik meg a kezelt tumorban, az eredeti célponttól eltérő hibát tartalmazó klón lesz a meghatározó, a tumorsejtek funkcióinak, elsősorban proliferációjának szabályozását egy másik jelút veszi át. (Az sem közömbös, hogy a célzott terápiára lokálisan előrehaladt és/vagy metasztatikus tumorok esetében kerül sor.) Ilyen változások igen gyakoriak a RAS-RAF-MEK-ERK jelátviteli úton. A zavarokat főleg mutációk okozzák, és vezetnek a tumorsejtek korlátlan szaporodásához, terjedéséhez. Az egyik kulcsproblémát a RAS mutációi jelentik, amelyek befolyásolása ma még megoldatlan. A leggyakoribb BRAF leggyakoribb mutációját gátlószerekkel sikerült átmeneti klinikai választ elérni, főleg melanomákon. Felmerült, hogy a kóros jelátvitel megakadályozását a jelúton a MEK és/vagy ERK gátlásával lehetne elérni, hiszen ezek aktivitása a fenti hibák miatt fokozottá válik. Ezek a próbálkozások a logikus elgondolás ellenére áttörő sikert még nem értek el. Ez az összefoglaló elsősorban a MEK-kel kapcsolatos eredményeket, a további lehetőségeket tekinti át.
Klinikai Onkológia
2017. MÁJUS 10.
Miért nem hatékonyak az immunellenőrzőpont-gátlók colorectalis carcinomában?
Az elmúlt években kimutatták, hogy az immunellenőrzőpont-gátlók hatásosak különféle malignus daganatok kezelésére, de kevésbé alkalmazhatók colorectalis carcinomában (CRC). Miközben egy egykaros fázis II. klinikai vizsgálatban a CRC mikroszatellit-instabilitást (MSI, vagy MMR-defi ciens, mismatch repair defi - cient) mutató alcsoportja közepes mértékű válaszreakciót mutatott a pembrolizumabra, a mikroszatellit-stabil (MSS) tumorok nem reagáltak rá. Ebben a cikkben a CRC-ben az immunválaszt lehetségesen befolyásoló mechanizmusok kerülnek áttekintésre, hogy a hiszton-deacetiláz (HDAC) -gátlás visszafordíthatja-e az előrehaladott CRC-k esetén gyakran észlelt immunológiai editálást, és visszaállítja-e az immunellenőrzőpont-blokáddal szembeni szenzitivitást.
A random variancia mint karcinogén tényező?
Egyes ráktípusoknál egy eddig nem tárgyalt, független tényező is hozzájárulhat a rák megjelenéséhez — mégpedig a DNS osztódása során megjelenő véletlenszerű hibák okozta mutációk, a random variancia hatása.
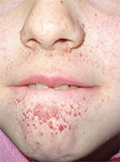
[Sclerosis tuberosás betegek gondozása]
[A sclerosis tuberosa egy autoszomális dominánsan öröklődő genetikai betegség, mely a legkülönbözőbb szervekben manifesztálódik benignus tumorok, illetve proliferációs zavarok formájában.]
Az apoptózisgátlás gátlása – fókuszban az MCL1
Az apoptózis szabályozásáért az úgynevezett Bcl-2 gén-, illetve proteincsalád tagjai a felelősek (Bcl-2: B-cell lymphoma 2), amelyek közül egyesek serkentik a sejthalált (pl. BAX, BAK), míg mások (pl. Bcl-X, Bcl-2, MCL1) gátolják.
1.
2.
3.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről4.
5.
1.
2.
Klinikai Onkológia
Hasnyálmirigyrák: az ESMO klinikai gyakorlati irányelve a diagnózishoz, kezeléshez, követéshez*3.
Klinikai Onkológia
Gyógyszerbiztonsági szemelvények – a múlt tanulságai és a jövő lehetőségei4.
5.