Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 453
Idegtudományok
2020. DECEMBER 30.
A Covid-19 neurológiai manifesztációi
A koronavírusokkal kapcsolatos eddigi ismereteink arra engednek következtetni, hogy a SARS-CoV-2 ritkán okoz központi és perifériás idegrendszeri problémát, a fertőzöttek nagy száma miatt mégis sok neurológiai betegre kell számítani; encephalitis és stoke következtében kialakuló krónikus állapotokra is fel kell készülni.
Az agyi plaszticitás kulcsa
A felnőtt korban született neuronok jóval a neurogenezis hanyatlása után is hozzájárulnak az agy flexibilitásához, állapította meg a Journal of Neuroscience tanulmánya.
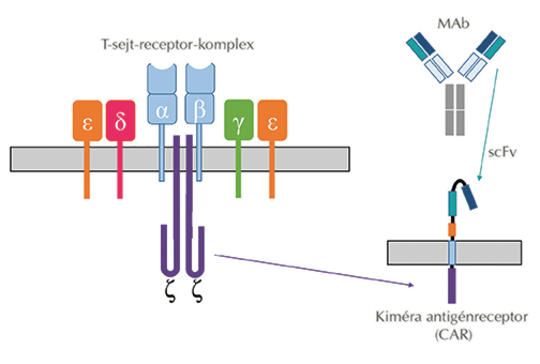
Génmódosított immunsejtek: új fegyverek nem csak daganatok ellen
Az elmúlt évtized onkológiai áttörése minden bizonnyal a CD19-specifikus CAR T-sejtek alkalmazása volt a különböző hematológiai kórképek kezelésében. A klinikai vizsgálatokban szerzett tapasztalatok, párosulva a magánszektor és gyógyszeripar befektetéseivel, a meglévő CAR T-sejt-készítmények kereskedelmi forgalmazásával, sok kutató figyelmét irányította rá az új típusú immunsejtekben rejlő lehetőségekre, és azok nem onkológiai célú felhasználására. A közlemény célkitűzése, hogy röviden bemutassa azokat a preklinikai alkalmazásokat, ahol a CAR T-sejteket sikerrel próbálták ki autoimmun és infektológiai kórképekben.
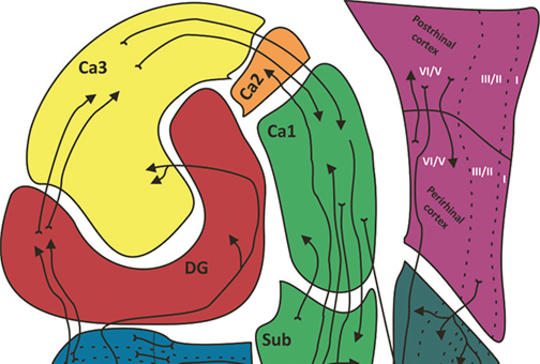
[A navigációban és memóriában szerepet játszó főbb hippocampalis sejttípusok]
[A hippocampalis formáció navigációban és memóriában betöltött szerepét a 20. század második felére fokozódó érdeklődés övezte, ami részben Henry G. Molaison esetére vezethető vissza, aki bilaterális medialis temporalis lobectomián esett át epilepsziája kezelése végett. A kezelést követően egyértelművé vált, hogy az eltávolított entorhinalis kéreg és a hippocampus jelentős része elengedhetetlen a memória kialakításában, ami számos kutatót ösztönzött e régiók további vizsgálatára. A hippocampalis „place” sejtek vagy helysejtek későbbi felfedezése vezette be számos más funkcionális sejttípus és neuronalis hálózat leírását a Papez-körben, amelyek kulcsszerepet játszanak a memóriafolyamatokban és a tér-idő információk kódolásában (sebesség, fejirány, határok, grid, objektum-vektor stb.) Ezen sejttípusok mindegyike egyedi tulajdonságokkal rendelkezik, és együttesen alkotják az úgynevezett „agyi GPS-t”. E közlemény célja, hogy bemutassa a limbicus rendszerben, különösképpen a temporalis lebenyben található sejttípusokat és neuronalis hálózatokat, melyek gyakran áldozatai különböző patológiai elváltozásoknak. A korai felfedezések eredményei mellett áttekintjük a legfrissebb megfigyeléseket is, és rávilágítunk arra, hogy a hippocampalis formáció legfőbb sejttípusai milyen szereppel bírnak a térbeli navigációban és a memóriafolyamatokban. Az utóbbi néhány évtizedben számtalan új, funkcionálisan elkülöníthető sejttípust írtak le ebben a régióban, de valószínűleg továbbiak még felfedezésre várnak. Az idegrendszeri betegségek jobb megértése érdekében hasznos lehet mélyebb betekintést nyerni a dinamikusan bővülő idegtudományi irodalomba. A memóriafolyamatokat és a térbeli navigációt érintő betegségek jelentős közegészségügyi terhet képviselnek, és öregedő társadalmunkban a helyzet folyamatosan romlik. Ez különösen ösztönzően hat ennek az agyterületnek a pontosabb megismerésére és funkcionális feltérképezésére.]
A humán immunrendszer rendszerelvű megközelítése
A nukleotidpolimorfizmusok kutatása révén kiderült, hogy az autoimmun betegségek kialakulásában nagyon kis hatáserősséggel nagyon sok genetikai lokusz közreműködik, és itt is kiderült, hogy egy-egy kórkép molekuláris heterogenitása – pl. SLE esetén – milyen óriási. E betegségek kezelését forradalmasította a biologikumok rendszerimmunológiának köszönhető bevezetése.
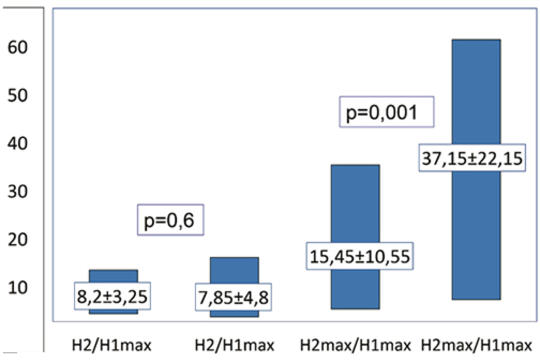
Változik-e a soleus-motoneuronok rekurrens gátlása Jendrassik-műfogás során?
Célkitűzés és kérdésfeltevés – A Jendrassik-műfogás alatti reflexélénkülésre eddig ellentmondó magyarázatok születtek. Munkánk során azt vizsgáltuk, hogy kétoldali erős kézszorítás során változik-e a soleus motoneuronjaira ható rekurrens gátlás. Módszer – A nervus tibialis ingerlésével soleus-H-reflexet váltottunk ki teljes nyugalmi állapotban és erős kétoldali kézszorítás alatt, váltakozva egyes (H1), illetve kettős ingerléssel (H2). A kettős ingerlésnél 10, 15, 20, illetve 25 ms ingerközti intervallumot és szupramaximális tesztingert használtunk. A H1- és H2-hullám amplitúdóit az M-hullám maximális amplitúdójának százalékos arányaként fejeztük ki. Páros Student-teszt és Bonferroni-korrekció segítségével összehasonlítottuk a kettős ingerlés során nyugalmi állapotban mért, százalékosan kifejezett H2max/H1max és H2/H1max amplitúdóarány értékeit a kézszorítás során kapott értékekkel. Vizsgálati alanyok – A vizsgálatban 28 egészséges önkéntes vett részt. Eredmények – A kézszorítás alatt kapott H1max/Mmax × 100 (37,5 ± 10,1) értékei (átlag ± 2SD) szignifikánsan magasabbak voltak a nyugalmi állapotban kapott (27,1 ± 7,4) értékekhez képest. A páros ingerlés során kapott H2max/ H1max × 100 értékei szignifikánsan magasabbnak bizonyultak kézszorítás alatt, mint nyugalmi állapotban, miközben a H2/H1max × 100 arány vonatkozásában a kézszorítás alatt, illetve a nyugalmi állapotban kapott értékek között szignifikáns különbséget nem találtunk. Következtetések – A H2max/H1max értékét a motoneuronok excitabilitása és a kondicionáló inger által kiváltott rekurrens gátlás egyaránt meghatározza, miközben a H2/ H1max értékét csak a rekurrens gátlás befolyásolja. Eredményeink alapján a Renshaw-sejtek megtartják gátló hatásukat a soleus motoneuronjaira távoli izomkontrakció esetén is. A Jendrassik-műfogás alatt megfigyelt soleus-H-reflex-növekedés nem magyarázható a rekurrens gátlás csökkenésével.
A dohányzás COVID-19 esetében sem tesz jót a légutaknak
Az American Journal of Respiratory Critical Care Medicine április 24-i elektronikusan megjelent közleményében a szerzők tudományosan bizonyították, hogy a dohányzás fokozza a tüdőben a SARS-CoV-2 receptoraként működő ACE2 gén expresszióját.
Táplálkozási ajánlások a CoVID-19 miatti karantén idején
A karanténhoz társuló stressz alvászavarokat is okozhat, ami tovább fokozhatja a stresszt és ezáltal a táplálékbevitelt, ami egy ördögi kör kialakulásához vezethet. Fontos, hogy vacsorára olyan ételeket fogyasszunk, amelyek szerotonint vagy melatonint tartalmaznak vagy elősegítik ezeknek a szintézisét.
A SARS-CoV-2 fertőzés (nem is olyan) ritka kardiális szövődménye: a szívizomgyulladás
Érdekes közlemény jelent meg a Lancet Klinikai esetbemutatások rovatában április 23-án egy Dél-Franciaországban észlelt myocarditis kapcsán, melyet a COVID-19 egyértelmű szövődményének tartottak a szerzők. Egy korábban jó karban lévő, 69 éves Lombardiából érkezett olasz férfi nizzai nyaralása során hasmenést, hányást tapasztalt, majd 7 nappal később a COVID-fertőzés tipikus tüneteit produkálva (köhögés, 39 C fokos láz, légszomj) került a Nizzai Egyetemi Kórház Sürgősségi Osztályára, ahonnan azonnal az Intenzív Osztályra szállították. Súlyos heveny légzési elégtelenség, respiratorikus distress, súlyos hypoxia miatt mechanikus lélegeztetésre szorult. Laborértékeiben normális Hb- és vérlemezkeszint, leukocytosis (Fvs: 14.9 G/l), balra tolt vérkép (neutrofil: 89%, lymphocyta: 7%, monocyta: 4%, eosinophil és basophil sejtek: 0-0%) igazolódott. Astrupja acidózist (pH: 7.27), 45.3 Hgmm-es pCO2-t és 146 Hgmm-es PO2-t mutatott, 98.2%-os O2-szaturációval. A beteg előzményeiben mindössze hypertonia szerepelt, melyre 2.5mg bisprolol kezelést kapott, tehát súlyos alapbetegsége nem volt.
A kemoterápia daganatkeltő hatása
Kemoterápia nélkül a felfedezett daganatos betegségek ötéves túlélési rátája – daganatfüggően – 0–15% között lenne, a jelenlegi terápia alkalmazásával 17-85%. Ugyanakkor számos figyelmeztetés hívja fel a figyelmet a kemoterápia által indukált nemkívánatos mellékhatások, legfőképpen a lehetséges tumorindukciós képesség veszélyeire, ami az öt éven túl gyógyult betegek 5-10%-át is érintheti. A szisztémás kemoterápiában használt egyes gyógyszerek (alkilálószerek, etopozid, arzén-trioxid) képesek a szervezet egészséges sejtjeiben mutációt okozni, amivel megnő a valószínűsége annak, hogy a mutációt szenvedett sejtek egy későbbi (szekunder) daganatképződést indítsanak el. A mutagén hatások mellett egyes kemoterapeutikumok a szervezet normális myeloid és epithelialis sejtjeire fejtenek ki olyan hatásokat, amelyek a szöveti mikrokörnyezet átalakításával megteremtik a malignus transzformáció lehetőségét. Ebben a folyamatban igen fontos szereplők a tumorokkal asszociáló makrofágok (TAM), amelyek a daganatsejt által szekretált faktorok és mikroszómák hatására megváltoztathatják génexpressziós mintázatukat, és prokarcinogén szignálokkal segítik a tumorsejtek megmaradását, invazivitását, csökkentik a citotoxikus T-sejtek aktivitását. Mindezen okok miatt kiemelten fontos az, hogy a daganatkeltő mutagénekkel dolgozó orvosok, gyógyszerészek, technikusok és nővérek ne kerüljenek közvetlen érintkezésbe ezekkel a veszélyes anyagokkal, hanem használjanak megfelelő védőfelszerelést.
1.
2.
3.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről4.
5.
1.
2.
Klinikai Onkológia
A rosszindulatú daganatok fenotípusának plaszticitása és az immunogén mimikri3.
Klinikai Onkológia
A szarkopénia mérése komputertomográfiával és jelentősége az onkológiai betegeknél4.
5.