Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Ideggyógyászati Szemle - 2006;59(03-04)
Tartalom
A neurourológia aktuális kérdései
A szerző összefoglaló áttekintést nyújt a neurogen hólyagdiszfunkció patofiziológiájáról, az egyes idegrendszeri megbetegedésekben észlelhető leggyakoribb hólyagműködési eltérésekről, valamint a terápiás lehetőségekről.
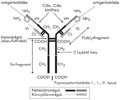
A nocicepció plaszticitása: a funkcionális-strukturális fájdalom kutatás újabb eredményei (angol nyelven)
A tradicionális szemlélet szerint a fájdalomrendszer három neuronból áll. Ezek közül az első, a primer nociceptív neuron a nociceptorokkal kezdődik és a gerincvelő hátsó szarváig tart. A második, a spinothalamicus neuron a canalis centralis előtt kereszteződve a hátsó szarvat köti össze a thalamusszal. A harmadik, a thalamocorticalis neuron, az agykéreg „fájdalomközpontjaiban” ér véget.
Az intravénás immunglobulin alkalmazása autoimmun neuromuscularis betegségekben
Az autoimmun neuromuscularis betegségekben az intravénás immunglobulin egymással összhangban álló komplex hatások révén befolyásolja az immunrendszert. Ezek a következők: 1. az Fc-receptorok expressziójának és funkciójának módosítása, 2. a komplement- és a citokinhálózat aktiválódásának befolyásolása, 3. antiidiotipikus antitestek neutralizálása, 4. a T- és B-sejt-aktiválódás, -differenciálódás és -effektorfunkció módosítása. Kontrollcsoportos
A metiléntetrahidrofolsav-reduktáz gén C677T- és A1298C-mutációinak interakciója ischaemiás stroke-ban
A metiléntetrahidrofolsav-reduktáz (MTHFR) C677T és A1298C mutációi, mint kedvezőtlen genetikai faktorok, emelkedett szérumhomocisztein-szintet okozva hozzájárulhatnak az ischaemiás stroke kialakulásához. A fenti két mutáció ischaemiás stroke-ban betöltött szerepét vizsgáltuk.
A magzat kedélyállapotára utaló, szonográfiával kimutatható arckifejezések - A mimika a magzati etológia része
A szerző a terhesgondozás folyamán ultrahangkészülékkel vizsgálta koronális síkban a magzatok arcát és arcvonásaiknak változását. A gyermekek és a felnőttek magatartásából kiindulva az arckifejezések változásai a kedélyállapotra utalnak.
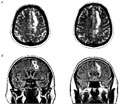
A subcorticalis ischaemiás agyi károsodás spektrális EEG-jellemzőiEsetelemzés
Az ischaemiás stroke-ot jellemző EEGelváltozások régóta ismertek, de az irodalmi adatok több vonatkozásban nem egységesek. A szerzők az egyoldali subcorticalis stroke kapcsán nyert EEG-adatokat elemezték, hangsúlyt fektetve a szemnyitásra bekövetkező változások dinamikájának értelmezésére.
Drogproblémák, ifjúsági pszichopatológia, szociokulturális háttértényezők
Az előadás célja a drogprobléma bemutatása, a teljesség igénye nélkül, elsősorban a társadalmi méretű drogértelmezés és drogkezelés - problémakezelés -, illetve a megelőzés szempontjából, hangsúlyozva a pszichoszociális és a szociokulturális tényezőket.
A bazális ganglionkárosodások funkcionális konzekvenciái
Basal ganglia are large subcortical nuclear masses that are interconnected with all cortical areas, and that receive updating (via thalamus) from most of the pathways leaving and targeting the cortex. This strategic position enables the basal ganglia to play a leading role in the synchronization of a wide range of central nervous system functions.
Válaszlevél éralagútügyben az „utolsó szó” jogán
Megdöbbenve olvastam a lap 2006. januári számában megjelent, véglegesnek deklarált idegsebészeti szakmai kollégiumi állásfoglalást (2005. július 1. keltezéssel) az éralagútmódszerről [Clin Neurosci/Ideggy Szle 2006;59(1-2):63-66].
1.
2.
3.
4.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről5.
1.
2.
Klinikai Onkológia
A rosszindulatú daganatok fenotípusának plaszticitása és az immunogén mimikri3.
Klinikai Onkológia
A szarkopénia mérése komputertomográfiával és jelentősége az onkológiai betegeknél4.
5.