Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 310
Migrénes stroke, migrén és stroke
A migrén és a stroke kapcsolata több szintű. Mivel mindkettő gyakori, így ischaemiás stroke más okból migrénben is szenvedő betegnél is kialakul. Az ischaemiás stroke tünetei hasonlíthatnak aurás migrénre, és valódi migrénes infarktus (MI) is kialakulhat. Ez utóbbiról akkor beszélünk, ha a migrénroham teljesíti az alábbiakat: Aurás migrénben szenvedő betegnél jelentkezik, megfelel a korábbi rohamoknak, kivéve, hogy egy vagy több auratünet tovább tart, mint 60 perc, képalkotó vizsgálat infarktust igazol a megfelelő területben és más ok kizárható. A migrénes infarktus incidenciája alacsony, az összes ischaemiás stroke 0,2–0,5%-a. Ez a fiatalok körében azonban 13% is lehet. Az MI gyakoribb nőkben, elsősorban a hátsó érterületet érinti (posterior: 70–80%), általában kisméretű (64,7%), többszörös laesio észlelhető az esetek 41,2%-ában.
Idegtudományok
2022. MÁJUS 17.
Centrális vénajel a sclerosis multiplex képalkotó diagnosztikájában
A sclerosis multiplex (SM) diagnosztikáját jelentősen megnehezíti, hogy számos kórkép, mint például a migrén, bizonyos vascularis eltérések és egyéb gyulladásos megbetegedések, az SM-hez hasonló képet mutat. Az SM diagnosztikájában használt McDonald-kritériumrendszer az egyértelműen demyelinisatióra utaló esemény megléte esetén jól működik, ugyanakkor az atípusos, nonspecifikus vagy tünetmentes betegekben hibás SM-diagnózishoz vezethet, főleg, ha az MR-képanyag olyan eltéréseket mutat, melyek ismeretlen jelentőséggel bírnak. A centrális vénajel megfelelő határértékek megválasztása esetén magas specificitással bír az SM és az SM-utánzó kórképek differenciálásánál. A T2*-súlyozott szekvenciák alkalmazása tovább növelheti a jel szenzitivitását is.
Idegtudományok
2022. MÁJUS 09.
Stroke-kockázat szemmozgatóideg-bénulást követően
Az izolált szemmozgatóideg-bénulások (ocular motor cranial nerve palsies, OCNP), melyek a III., IV., vagy VI. agyidegek funkciójának zavarával járnak, jelentős számban fordulnak elő a szemészeteken. Az ischaemiás OCNP-k az összes OCNP mintegy 17-20%-át teszik ki, viszont ez az arány az idősekben, nem traumás eredetű, fájdalmatlan, akut, izolált OCNP-k esetében a 83–99%-ot is elérheti. Az ischaemiás OCNP-k rizikófaktorai nagyban megegyeznek a stroke rizikófaktoraival, úgymint hypertonia, diabetes mellitus, dyslipidaemia és dohányzás. Az ischaemiás szemmozgatóideg-bénulások egy a TIA-val megegyező nagyságrendű rizikótényezőt jelentenek egy bekövetkező stroke-ra nézve, így bekövetkezésük esetén fontos a cardiovascularis rizikótényezők agresszív kezelése, valamint a primer stroke-prevenció megkezdése.
A krónikus stressz szerepe az essentialis hypertonia kialakulásában. A rilmenidin helye a stressz által kiváltott hypertonia kezelésében
A hypertonia a cardiovascularis betegségek egyik önálló rizikótényezője. Kialakulásában számos tényező játszik szerepet. Ezek közül a krónikus stressz a szimpatikus aktivitás fokozásán keresztül eredményezheti a magasvérnyomás-betegség kialakulását. A szimpatikus idegrendszeri aktivitás emelkedésének jeleit elsősorban a hypertonia kezdeti – perctérfogat-fokozódással járó – szakaszában észlelhetjük. A szimpatikus aktivitás fokozódása a hemodinamikai következményeken (perctérfogat-emelkedés, tachycardia, coronariavasoconstrictio, proarrhythmia) túl számos kedvezőtlen következménnyel járhat. A metabolikus (inzulinrezisztencia, dyslipidaemia), strukturális és trofikus hatásokon túl (endotheldiszfunkció, vascularis hypertrophia, myocardium-hypertrophia), thromboticus és humorális (prokoaguláció, thrombocytaaggregáció-fokozódás, nátriumretenció, renin-angiotenzin-aldoszteron tengely aktivációja) folyamatok indulhatnak el, amelyek több támadásponton károsíthatják a szervezet működését. A fokozott szimpatikus aktivitás kedvező befolyásolására számos antihypertensiv gyógyszercsoport áll rendelkezésünkre. Idetartoznak a perifériásan ható alfa- és béta-blokkolók, továbbá a centrálisan ható vegyületek. Ez utóbbiak első generációját (például clonidin, guanfacin, alfa-metildopa) – jelentős mellékhatásprofiljuk miatt – jelenleg ritkán, egyáltalán nem vagy csak szűk indikációs körben alkalmazzuk. A második generációs, centrálisan ható vegyületek közül a rilmenidin, az imidazolin-I1-receptorok stimulációjának útján fejti ki kedvező hatásait, amelyeket kihasználhatunk a szimpatikus idegrendszer fokozott aktivitásával járó enyhe vagy mérsékelt hypertoniában.
Klinikum
2022. ÁPRILIS 15.
A szérum D-vitamin-koncentrációja és a dementiakockázat közötti összefüggés 2-es típusú cukorbetegeknél
Néhány év óta csökken a cukorbetegek vascularis mortalitása és nő körükben a dementia miatti halálozás. Az általános populációban a jó D-vitamin-státusz csökkenti a dementia kockázatát, de igaz-e ez a diabetesesek körében is?
Érfali rugalmatlanság, az artériás stiffness klinikai jelentősége időskorban
A magasvérnyomás-betegség és a cardiovascularis kockázat az életkor előrehaladtával egyre gyakoribbá válik. Ugyanakkor az öregedés folyamata bizonyos egyénekben sokkal gyorsabbnak tűnik, ami tükröződik a korai vascularis öregedés (early vascular aging, EVA) tünetegyüttesében. Az ütőerek falának rugalmatlanná válásában, az artériás stiffness kialakításában a hypertonia és az öregedés játssza a legfőbb szerepet, amely lényege az EVA-nak: a nagy elasztikus artériák (főleg az aorta) falának középső rétege veszít a rugalmasságából. Ez a folyamat jól mérhető a pulzushullám terjedési sebességével. Az idős hypertoniás egyénekben a nagy artériák rugalmatlansága, a szisztolés és diasztolés vérnyomás különbsége fokozódik, a pulzusnyomás megnő, köszönhetően a hullám-visszaverődésnek. Az érfali rugalmatlanságnak prediktív szerepe van a későbbi szív-ér rendszeri események (koszorúér-betegség, stroke, vascularis dementia), de még az összmortalitás szempontjából is. A korai vascularis öregedés és a szupernormális vascularis öregedés (supernormal vascular aging, SUPERNOVA) koncepciója segít értelmezni, miért alakulnak ki egyesekben korai célszervkárosodások és érrendszeri szövődmények, mások miért maradnak jóval „fiatalabbak” kronológiai életkoruknál. Új gyógyszereket fejlesztettek az EVA kezelésére, melyeknek akkor lehet szerepük, ha az életmódkezelés és a hagyományos, rizikófaktorokat csökkentő gyógyszerek hatása már nem elegendő.
A cardiovascularis rehabilitáció főbb sajátosságai posztakut Covid-19-ben
A SARS-CoV-2-fertőzés okozta pandémia nagy kihívás világszerte. A döntően légúti károsodást okozó járvány intézményi ellátásának alappilléreit az akut és az intenzív ellátás adja. Ugyanakkor, a túlélők funkcionális állapotának és életminőségének javítása, valamint a szövődmények hatásának csökkentése érdekében a rehabilitációnak kiemelt jelentősége van. Becslések szerint az elbocsátott betegek 40-50%-a igényel valamilyen egészségügyi támogatást, illetve 4-5%-uk fekvőbeteg-rehabilitációt. A respiratórikus rendszer érintettsége mellett a Covid-19 okozta cardiovascularis hatások (szívelégtelenség és myocarditis, akut coronariaszindróma, ritmuszavar, vénás thromboembolia) is részei a szisztémás gyulladásos folyamatoknak, melyek a hospitalizált betegek 7–28%-át érinthetik, továbbá tartós életminőség-romláshoz és munkaképesség-elvesztéshez vezethetnek. Az összefoglaló a rendelkezésre álló tudományos adatbázisok, szakértői konszenzusok és európai szakmai társasági ajánlások alapján mutatja be a posztakut-Covid kardiológiai rehabilitáció és ezen belül a fizikai gyakorlatok ajánlott módját, feltételeit, intenzitását. Kitér a munkába és a sporttevékenységhez való visszatérés javasolt feltételeire. A strukturált tréning a kardiológiai rehabilitáció egyik igen fontos és alacsony kockázatú eleme, amely csökkenti a cardiovascularis komplikációkat, a thromboemboliás szövődményeket, a szisztémás gyulladást és a mortalitást, javítva a funkcionális felépülést és az endothelfunkciót. A fizikai tréning tervezését a betegek komplex felmérése kell, hogy megelőzze. Rizikófelmérés, teljesítőképesség és funkcionális felmérések szükségesek az egyénre szabott tréning intenzitása, gyakorisága és a mód kiválasztása érdekében. Mindez megfelelő szekunder prevenciós gyógyszeres kezeléssel, monitorozással, dietoterápiával és pszichoterápiával kell, hogy párosuljon a fokozatosság elvének betartása mellett. A konszenzusajánlások hangsúlyos szerepet javasolnak az otthoni (home-based), illetve a telerehabilitációnak, figyelembe véve a rehabilitációt is sújtó járványügyi kapacitásokat érintő korlátozásokat.
Idegtudományok
2022. JANUÁR 28.
Antikoaguláció agyvérzést követően
Pitvarfibrilláló betegekben, akik túléltek egy antikoagulációval asszociált intracerebralis vérzést, visszatérő kérdés, hogy hosszú távon érdemes-e újrakezdeni az antikoagulációt stroke- és szisztémás thromboembolisatio-prevenciós célzatból. Sokáig a betegek csak egy töredék részében folytatták az antikoagulációt és akkor is csak sok hónappal a vérzéses eseményt követően. Újabb, megfigyeléses vizsgálatok amellett érveltek, hogy a pitvarfibrilláló betegekben az antikoaguláció folytatása alacsonyabb mortalitási kockázatot jelent, valamint jobb funkcionális kimenetelt eredményez, mint az antikoaguláció elhagyása. Ezek az összefüggések attól függetlenül fennálltak, hogy a vérzés lobaris vagy nem lobaris volt. Emellett az ischaemiás stroke kockázata intracerebralis vérzést követően hasonlóan magas lehet, mint a rekurrens vérzésé. Két obszervációs vizsgálatokat összefoglaló metaanalízisben az antikoagulációt folytató betegek ischaemiás stroke-kockázata alacsonyabb, míg a vérzéses kockázata ugyanolyan magas volt, mint a nem antikoagulált betegekben. Ezekben a vizsgálatokban ugyanakkor a legtöbb beteg K-vitamin-antagonista kezelésben (VKA) részesült. A direkt orális antikoagulánsok (DOAC-ok) alacsonyabb vérzéses kockázatot mutatnak a VKA-knál mind primer, mint TIA-t vagy ischaemiás stroke-ot követő szekunder prevencióban pitvarfibrilláló betegekben, ezért a DOAC-ok egy biztonságosabb alternatívát jelenthetnek a VKA-knál intracerebralis vérzést követő antikoaguláció tekintetében.
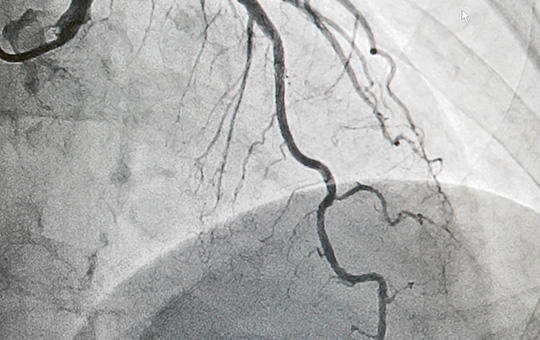
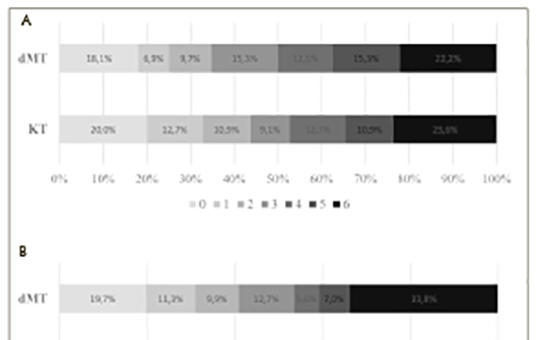
A mechanikus thrombectomiát megelőző intravénás thrombolysis szerepe az akut agyi nagyérelzáródások kezelésében
Az intravénás thrombolysis (IVT) hatékonysága a nagyérocclusio (NÉO) okozta akut ischaemiás stroke (AIS) ellátásában mérsékelt, szemben a mechanikus thrombectomiáéval (MT). Az MT-t megelőző IVT kontraindikációval nem rendelkező betegek esetében jelenleg evidencián alapuló eljárás, melynek szükségességét az elmúlt évek vizsgálatai megkérdőjelezték. Vizsgálatunk célja a centrumunkban akut agyi NÉO miatt végzett direkt mechanikus thrombectomia (dMT) és a kombinált terápia (KT) hatékonyságának és biztonságosságának értékelése volt. Vizsgálatunkba 4,5 órán belüli tünetkezdetű, NÉO okozta AIS-os betegeket választottunk be, akik 2017 novembere és 2019 augusztusa között MT-n estek át centrumunkban. A betegek adatait stroke-regiszterünkbe rögzítettük. A betegeket két csoportba osztottuk, attól függően, hogy dMT vagy KT került elvégzésre. Elsődleges végpontként a 30. és 90. napon felvett módosított Rankin-skála (mRS) alapján mért funkcionális kimenetelt tekintettük. Másodlagos kimeneti végpontként a 30. és 90. napos mortalitást, a rekanalizáció mértékét és a szimptómás vérzéses transzformációk előfordulását értékeltük. Vizsgálatunkba összesen 142 (életkor: 68,3 ± 12,6 év, 53,5% nő), 4,5 órán belüli NÉO-t elszenvedett beteget vontunk be, közülük 81 (57,0%) esetében dMT történt, 61 (43,0%) beteg pedig KT-ban részesült. A dMT-val kezelt csoportban szignifikánsan magasabb volt a vascularis rizikófaktorok és a komorbiditások aránya. A 30. napon a kedvező kimenetelek aránya 34,7% volt a dMT-ban, míg 43,6% a KT-ban részesültek körében (p = 0,307), a 90. napra 40,8% vs. 46,3%-ra (p = 0,542) változott ez az arány. A 30. napon a mortalitások aránya 22,2% és 23,6% (p = 0,851), a 90. napon 33,8% és 25,9% (p = 0,343) volt. Az eredményes rekanalizáció aránya 94,2% volt a dMT-val kezelt betegeknél, illetve 98,0% a KT-ban részesülteknél (p = 0,318). A dMT-val kezelt betegek 2,5%-ánál, míg a KT-ban részesültek 3,4%-ánál (p = 0,757) mutatott szimptómás vérzéses transzformációt a 24 órás képalkotó vizsgálat. Vizsgálatunk eredményei a KT-ban részesült betegek mérsékelten jobb funkcionális kimenetelére utalnak. Az MT-t megelőzően alkalmazott IVT nem növeli szignifikánsan a szimptómás intracranialis vérzések gyakoriságát.
Extrapulmonalis többszervi károsodás és funkciózavar Covid-19-ben
A SARS-CoV-2 vírus nemcsak a tüdőt támadja meg, hanem számos más szervet (szív, vese, máj, gyomor-bél traktus, pancreas, agy, vérképzés) és szabályozórendszert (RAAS, immunrendszer) is különböző mértékben és különböző patomechanizmussal. Ennek megfelelően sejtpusztulás, szövetkárosodás, illetve az egyes szervek funkciózavara vagy akár elégtelensége alakul ki. Közleményünk az extrapulmonalis károsodások gyakoriságát, a klinikai megnyilvánulásokat és azok hátterében álló patomechanizmusokat részletesen elemzi. Ezen sokszervi károsodás elsősorban a súlyos Covid-esetekben fordul elő, de mérsékelt vagy enyhe lefolyású esetekben is megjelenhet. Számolni kell azzal is, hogy a következmények az akut szakasz után, szeronegatív állapotban - hónapokkal a fertőzés kezdete után - is felléphetnek. Kiemelten a szív (myocarditis, coronariaelégtelenség, ritmuszavar), a vese (akut veseelégtelenség, majd tartós GFR-csökkenés), a glükózanyagcsere zavara (diabetes romlása, új diabetes kialakulása, ketoacidosis) okozza a legnagyobb terápiás kihívást. A sokszervi károsodás hátterében a direkt vírus okozta sejtpusztulás, a vascularis rendszerben végbemenő endothelialis sejtkárosodás és thromboinflammatio microthrombusok kialakulásával, a RAAS szabályozórendszer egyensúlyzavara és korai és késleltetett kóros immunválasz (citokinvihar) áll.
1.
2.
3.
4.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről5.
1.
2.
Klinikai Onkológia
A rosszindulatú daganatok fenotípusának plaszticitása és az immunogén mimikri3.
Klinikai Onkológia
A szarkopénia mérése komputertomográfiával és jelentősége az onkológiai betegeknél4.
5.