Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 179
A petefészekrák kezelésének frontvonalában: a PARP-gátlók szerepének megújítása
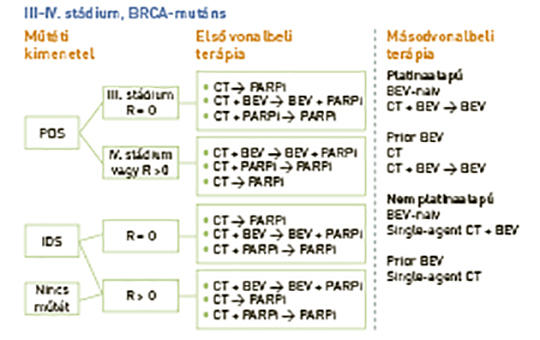
Kiújult petefészekrákban a poli(ADP-ribóz)polimeráz- (PARP-) gátlókkal történő kezelések megváltoztatták a platinaérzékeny daganatok kezelését. Az új adatok szerint a PARP-gátlókat a kezelési algoritmus korábbi szakaszában kell alkalmazni. A kutatók számba veszik azokat a fázis III vizsgálatokat, amelyekben a PARP-gátlók hatását értékelték újonnan diagnosztizált petefészekrákok primer, illetve fenntartó kezelésében. Megvitatják a gyógyszerek hatásosságát és biztonságosságát az összes daganat, illetve a biomarkerek szerint válogatott daganatok klinikai vizsgálataiban, és összevetik a különböző vizsgálatok előnyeit és korlátait. Fontolóra veszik a jövő kutatásainak prioritásait – különös tekintettel a betegek kiválasztására és a jövőben alkalmazandó, egyelőre hiányzó gyógyszeres regimenek megalkotására. Négy fázis III vizsgálatban (SOLO-1, PAOLA-1/ENGOT-OV25, PRIMA/ENGOT-OV26 és VELIA/GOG-3005) PARP-gátlók használatával (olaparib, niraparib vagy veliparib) a progressziómentes túlélés jelentős javulását figyelték meg petefészekrákos betegekben. A vizsgálatok eltérő kialakítása (kezelés vagy fenntartó kezelés, egy gyógyszeres vagy kombinációs kezelés, bevacizumabbal vagy bevacizumab nélkül), a betegek kiválasztása (műtéti eredmény, biomarkerek elérhetősége, prognózis szerint), a résztvevők eredeti megválasztása (intention-to-treat, BRCA-mutációs vagy homológ rekombinációdeficites pozitív) befolyásolták a vizsgálatokból levonható következtetéseket. A teljes túlélési adatok még függőben vannak, hosszú távú biztonságossági adatok is csak korlátozottan állnak rendelkezésre. A PARP-gátlók sarkalatos szerepet játszanak az újonnan kimutatott petefészekrák-ellátásban, és befolyásolják a további kezeléseket. Ki kell választani azokat a betegeket és gyógyszereket, akiknél az eddigi alkalmazott kezelések a PARP-gátlóknál kevesebb haszonnal járnának.
Tüdőrák harminc év távlatából. Gondolatok a küzdelmes múltról, a jelen eredményeiről és az ígéretes jövőről
Az elmúlt 30 évben a tüdőrák komplex kezelésében óriási fejlődés történt. Ez a fejlődés főként az utóbbi évtizedhez köthető. A tüdőrák kezelésével kapcsolatos nihilizmus már a múlté, realitássá vált az is, hogy az előrehaladott stádiumú betegek is megfelelő kezeléssel gyógyíthatóvá válhatnak, illetve betegségük folyamatos aktív daganatellenes terápia mellett krónikussá szelídíthető. Az előrehaladott stádiumban lévők harminc évvel ezelőtt elérhető 6-8 hónapos várható túlélési mutatói manapság már jelentősen növekedtek, bizonyos esetekben akár az 5 évet is meghaladhatják. Ehhez szükséges a megfelelő diagnosztikus háttér, amely lehetővé teszi a biomarkeralapú kezeléseket. Korai stádiumban alapvető a reszekciós tüdőműtét, beillesztve a komplex terápiás lehetőségeket neoadjuváns és adjuváns formában, illetőleg az új műtéti technikák is hozzájárulnak a terápiás eredmények javulásához. Elmondható ugyanez a sugárterápia vonatkozásában is. A gyógyszeres terápiás lehetőségek tekintetében is a komplex terápiás stratégia érvényesül, melyben alapvető szerepet játszanak a citotoxikus kemoterápiás, célzott kezelési és immunterápiás modalitások. A tüdőrák kezelési stratégiájának felállításában döntő szerepe van a tüdőrák-specifikus onkoteamek működésének. A jövő útját az újabb és újabb célzott terápiás lehetőségek megjelenése, az immunterápiás indikációk bővülése jelezheti a precíziós medicina alkalmazásával. Nem szabad azonban elfeledkeznünk a primer és szekunder prevencióról sem, mely a dohányzás elleni hatékony küzdelmet, illetőleg most már az evidenciává vált rizikócsoportos alacsony dózisú mellkasi CT-szűrés alkalmazását jelenti.
Az inváziós spektrum prognosztikai jelentősége glioblastomában
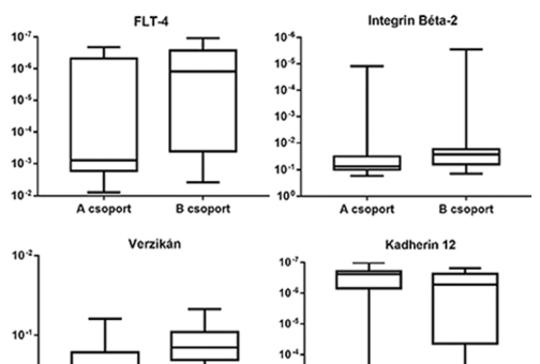
A glioblastoma a leggyakoribb központi idegrendszeri rosszindulatú daganat; sebészi kezelése a daganatok invazív jellegénél fogva nem lehetséges, onkoterápiája pedig csupán szerény eredményeket hoz – a betegek átlagos teljes túlélése (OS) 16–24 hónap. A betegek egy része alig reagál az alkalmazott kezelésre; a klinikumban jelenleg nincs olyan prognosztikai vagy prediktív marker, ami segítené a betegek túlélésében tapasztalható jelentős szórás érdemi feltérképezését és a kezelési algoritmus optimalizálását. Jelen kutatásban az invázióban szerepet játszó extracelluláris mátrix (ECM-) molekulák expressziójának prognosztikai jelentőségét kívántuk meghatározni. Eltérő prognózisú betegcsoportokat létrehozva (A csoport OS < 16 hónap, B csoport OS > 16 hónap) vizsgáltuk meg glioblastomás betegek gyorsfagyasztott tumormintáiban a szakirodalom által jelenleg elismert markerek (IDH1 mutációs és MGMT metilációs státusz) jelenlétét, továbbá 46 inváziós ECM-molekula mRNS-szintjét. A DE KK Idegsebészeti Klinikán operált és az Onkológiai Klinikán utókezelt betegek klinikai adatai nem mutattak jelentős különbségeket a túlélési adatokat (progressziómentes és teljes túlélés) és a reoperációs arányt leszámítva. Minden minta IDH vad típusú volt. Jelentős különbség volt a jobb és a rosszabb túlélésű betegek között az MGMT promoter hipermetiláció arányában (28,6% vs. 68,8%). Az inváziós ECM-molekulák expressziós mintázata, az inváziós spektrum szintén jelentős különbséget mutatott; szignifikáns különbség mutatkozott az integrin β2, kadherin-12, FLT4/VEGFR-3, verzikán molekulák expressziójában. Az inváziós spektrum megbízhatóságát statisztikai osztályozóval tesztelve a módszer a minták 83,3%-át sorolta a megfelelő prognosztikai csoportba (PPÉ: 0,93). A különböző túlélésű betegcsoportok összehasonlítása során a reoperációs arányban megfigyelhető különbség az irodalmi adatokkal összevágó tény. Az MGMT promoter metiláltságának vizsgálata hazai újdonság, az eredmény az eddigi ismereteket megerősítve sürgeti a vizsgálat rutinszerű bevezetését. Az inváziós spektrum vizsgálata többletinformációt ad a tumorról, prognosztikai markerként segíthet felismerni az agresszívabb tumorokat, továbbá felhívja a figyelmet az antiinvazív ágensek jövőbeni használatának szükségességére a GBM terápiájában.
Idegtudományok
2020. JÚLIUS 29.
A Homo sapiens és a pszichoaktív növények közötti kapcsolat
A pszichoaktív növények fogyasztásának az emberré válásban, az emberi kultúra kialakulásában játszott alapvető szerepét mutatják be az Akadémiai Kiadó gondozásában kiadott angol nyelvű folyóirat, a Journal of Psychedelic Studies 2019 végén megjelent különszámának tanulmányai.
A kemoterápia daganatkeltő hatása
Kemoterápia nélkül a felfedezett daganatos betegségek ötéves túlélési rátája – daganatfüggően – 0–15% között lenne, a jelenlegi terápia alkalmazásával 17-85%. Ugyanakkor számos figyelmeztetés hívja fel a figyelmet a kemoterápia által indukált nemkívánatos mellékhatások, legfőképpen a lehetséges tumorindukciós képesség veszélyeire, ami az öt éven túl gyógyult betegek 5-10%-át is érintheti. A szisztémás kemoterápiában használt egyes gyógyszerek (alkilálószerek, etopozid, arzén-trioxid) képesek a szervezet egészséges sejtjeiben mutációt okozni, amivel megnő a valószínűsége annak, hogy a mutációt szenvedett sejtek egy későbbi (szekunder) daganatképződést indítsanak el. A mutagén hatások mellett egyes kemoterapeutikumok a szervezet normális myeloid és epithelialis sejtjeire fejtenek ki olyan hatásokat, amelyek a szöveti mikrokörnyezet átalakításával megteremtik a malignus transzformáció lehetőségét. Ebben a folyamatban igen fontos szereplők a tumorokkal asszociáló makrofágok (TAM), amelyek a daganatsejt által szekretált faktorok és mikroszómák hatására megváltoztathatják génexpressziós mintázatukat, és prokarcinogén szignálokkal segítik a tumorsejtek megmaradását, invazivitását, csökkentik a citotoxikus T-sejtek aktivitását. Mindezen okok miatt kiemelten fontos az, hogy a daganatkeltő mutagénekkel dolgozó orvosok, gyógyszerészek, technikusok és nővérek ne kerüljenek közvetlen érintkezésbe ezekkel a veszélyes anyagokkal, hanem használjanak megfelelő védőfelszerelést.
Hogyan osztályozzuk az intenzív ellátásra szoruló betegeket?
Általánosságban megállapítható, hogy a kórházba érkezés sorrendjének elsődleges elve, amelyet Kínában Wuhan tartományban alkalmaztak, nem a legkedvezőbb stratégia a helyzet kezelésére, ráadásul a helyszíni tapasztalatok alapján jelentősen hozzájárult a járvány kezdeti nagyarányú halálozásához.
Húgyhólyagdaganat neoadjuváns és palliatív gyógyszeres ellátása
Az izominvazív, lokális hólyagtumoros betegek túlélése kedvezőbb, ha a cystectomiát neoadjuváns vagy adjuváns platinatartalmú kemoterápia egészíti ki. A neoadjuváns ciszplatinbázisú kemoterápia hatására, metaanalízisek alapján, 5-16%-os ötéves túlélési benefit érhető el. A neoadjuváns kemoterápiára jól reagáló betegeknél (patológiai komplett remisszió aránya 12-50%) még kedvezőbb a kimenetel. A cystectomia három hónapon túli késlekedésének nincs kedvezőtlen hatása a túlélésre, ha a műtét előtt kemoterápia történik. Az adjuváns fázis III vizsgálatok és metaanalízisek eredményei kevésbé egyértelműek, de összességükben kedvező trend észlelhető a kemoterápia hatására a túlélésben, különösen pT 3/4 és/ vagy N+ (valamint high grade vagy margin pozitív) esetekben. A platinabázisú kemoterápiás kezelés utáni progresszió esetén másod- és többed-, valamint ciszplatinra alkalmatlan betegeknél PD-L1-expresszió esetén első vonalban is alkalmazható immunterápia hatására a betegek túlélésének és a tumorválasz időtartamának eredményei igen biztatóak, hatékonyabbnak látszanak az adott stádiumokban eddig alkalmazott kemoterápiás szerek publikált adatainál. A legújabb irányokban az immunterápia neoadjuváns, adjuváns, valamint kemoterápiával kombinált alkalmazása is klinikai vizsgálatok értékelése alatt áll, amelyek korai adatai kiemelkedően perspektivikusnak tűnnek.
A lokalisan előrehaladott es a metasztatikus gyomorrak kezelese
A gyomorrák kezelésében az utóbbi időben ugyan jelentős előrelépés történt, de a túlélési eredmények még mindig meglehetősen szerények. Az összefoglaló közlemény célja áttekinteni a lokálisan előrehaladott és a metasztatikus gyomorrák kezelésének történetét és bemutatni a jelenlegi kezelési standardokat. Kiemelten foglalkozik a perioperatív kezelésben a közelmúltban bekövetkezett változásokkal, csakúgy, mint az áttétes betegek kezelésének átalakulásával. Részletesen elemzésre kerül a palliatív kemoterápiák többvonalbeli használata, és az elérhető célzott kezelések helye az áttétes daganatokban. Az immunellenőrzőpont- gátlók egyre szélesebb körben történő alkalmazásai és jövőbeni felhasználási lehetőségei is tárgyalásra kerülnek. A gyomorrák molekuláris altípusairól mint a terápiaválasztás lehetséges indikátorairól is szó esik. Végül pedig olyan terápiás javaslatokat kíván adni, ami
A cholangiocellularis carcinoma gyógyszeres kezelése
Az epeúti tumorok ritka daganatok, rossz prognózissal. Sok beteget előrehaladott stádiumban fedeznek fel, amikor műtét már nem jön szóba. Amennyiben műtétet végeznek is nagy a kiújulás rizikója, emiatt szükség van műtét után utókezelésre. Standard adjuváns kezelés a BILCAP study eredményei alapján a kapecitabin terápia, amely a túlélési mutatókat nagymértékben javította. A metasztatikus vagy előrehaladott stádiumú betegeknél első vonalban a standard terápia még mindig a gemcitabin és ciszplatin kombináció, van japán adat egyenértékű gemcitabin + S1-re is. A gemcitabin + ciszplatin kezelés utáni progresszió esetére 2019-ig nem volt evidencián alapuló kezelés, az ABC-O6 vizsgálat eredménye alapján az mFOLFOX protokoll javasolható most már. MSI-H/dMMR betegekben immunterápiát kell alkalmazni. A molekuláris célpontokra ható kezelések egyre inkább előtérbe kerülnek, az FGFR és IDH új targetek cholangiocellularis tumorokban, a kezdeti vizsgálati eredmények ígéretesek. A személyre szabott terápia molekuláris profi l alapján tekinthető a jövő útjának.
Az ANTI-PD-1-kezelés reumatikus mellékhatásai, valamint a kortikoszteroidok hatása
A PD-1/PD-L1 tengelyt célzó immunterápia (nivolumab, pembrolizumab, atezolizumab, avelumab) többféle daganatos betegségben példátlan túlélési előnnyel jár, viszont a betegek körülbelül 20%-ánál súlyos, immunfüggő mellékhatások (irAE-k) jelentkeznek. Ezek közül jól ismert a colitis, a pneumonitis…
1.
2.
3.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről4.
5.
1.
2.
Klinikai Onkológia
Hasnyálmirigyrák: az ESMO klinikai gyakorlati irányelve a diagnózishoz, kezeléshez, követéshez*3.
Klinikai Onkológia
Gyógyszerbiztonsági szemelvények – a múlt tanulságai és a jövő lehetőségei4.
5.