Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 69
Alemtuzumabterápiával kezelt sclerosis multiplexes betegek követéses vizsgálata a szegedi Sclerosis Multiplex Centrumban
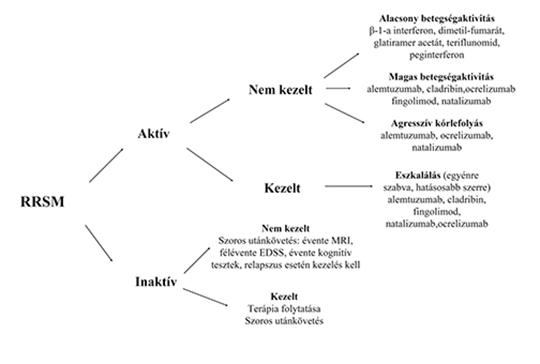
A relapszus-remisszió kórformájú sclerosis multiplex kezelési stratégiája az elmúlt évtizedben jelentősen megváltozott. Míg korábban az eszkalációs terápia volt az elfogadott terápiás módszer, napjainkban magas betegségaktivitás esetén lehetőségünk van indukciós kezelés indítására is.
Egészségpolitika
2022. JÚNIUS 30.
Az otthoni szabályok szerepe a dohányzás elleni küzdelemben
Számos országban hatékonynak bizonyult a dohányzás zárt nyilvános helyen és munkahelyeken történő betiltása. Ismert, hogy a dohányzásmentes környezet nem csak a másodlagos és harmadlagos dohányfüst káros hatásaitól óv meg, hanem a leszokott dohányzókat is segíti a leszokás fenntartásában. A munkahelyi mellett tehát az otthoni teljes dohányzásmentesség nem csak a nemdohányzókat védi, hanem dohányzás kipróbálásának valószínűségét is csökkenti, illetve már dohányzók esetében is szerencsés, mivel a leszokás, illetve a kisebb mértékű dohányzás irányába befolyásol.
Agresszív lefolyású akut sclerosis multiplexes beteg sikeres kombinált (plazmaferézis és alemtuzumab) kezelése
A sclerosis multiplex (SM) diagnosztikus és terápiás protokollja az utóbbi 3-4 évben jelentősen megváltozott. Az ECTRIMS 2020-ban közölt ajánlása meghatározta a magas betegségaktivitású SM -enotípus nomenklatúráját, diagnosztikus és terápiás protokollját. Ezt a fenotípust az ECTRIMS 2020 „agresszív SM”-ként definiálja, mely kórformát gyakori, súlyos relapszusok, rapid progresszió, magas gyulladásos és neurodegeneratív aktivitás jellemez.
A Covid-19-pandémia hatása az evészavarokra
A Covid-19-pandémia során több pszichiátriai kórkép vált gyakoribbá, a többi között az evészavarok esetében is. Növekedett az anorexia nervosa és a bulimia nervosa, valamint egyéb evészavartünetek incidenciája. Emellett súlyosbodtak a tünetek és nagyobb lett a relapszus aránya is. Mindezek hátterében a következő tényezők szerepelhetnek: megváltozott az étel elérhetősége; fokozódott a félelem az elhízástól, hangsúlyossá vált a közösségi média és egyes internetes oldalak szerepe az izoláció következtében, kifejezettebb lett a társas összehasonlítás; korlátozottak voltak a sportolási lehetőségek; növekedett a stresszkeltő életesemények hatása, például a családi feszültségeké. A pandémia mentális következményei a táplálkozási magatartás terén is a pszichoedukáció, az elsődleges és másodlagos prevenció fontosságára hívják fel a figyelmet.
B-sejt-depletio a sclerosis multiplex terápiájában: új szereplő az ofatumumab
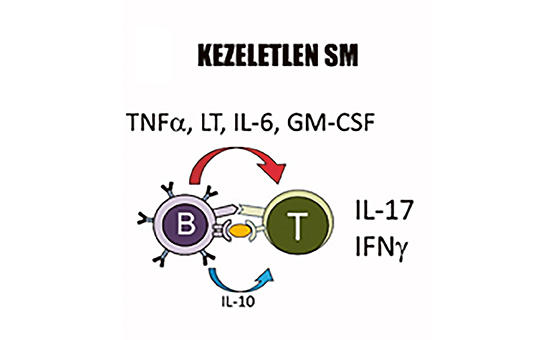
Az elmúlt évek kutatási eredményei bizonyították, hogy a B-lymphocyták döntő szerepet játszanak a sclerosis multiplex (SM) patogenezisében. A betegség folyamatának jobb megértése a B-sejteket célzó antitest-terápiák kifejlesztését eredményezte, amelyek potenciális gyógyszerek lehetnek mind a relapszusos, mind a progresszív SM formáiban. A B-sejt-depletiós terápiák ezért mindinkább előtérbe kerülnek, és meghatározóak a betegség progressziójának csökkentésében. Az első B-sejt-depletáló, anti-CD20 monoklonális antitest a rituximab volt, amit sclerosis multiplexben is vizsgáltak, és a kedvező eredményeket követően újabb gyógyszerek kerültek kifejlesztésre, hasonló támadásponttal. 2017-ben az FDA, 2018-ban az EMA is engedélyezte egy másik anti-CD20 monoklonális antitest, az ocrelizumab relapszáló-remittáló sclerosis multiplex (RRSM) és primer progresszív sclerosis multiplex (PPSM) terápiájában történő bevezetését. Ez különösen jelentős előrelépés volt a PPSM kezelésében, hiszen ez volt az első gyógyszer, ami bizonyítottan csökkentette a progressziót PPSM-ben. A B-sejt-depletiós terápia új szereplőjeként nemrégiben lépett színre az ofatumumab, ami egy teljesen humán anti-CD20 monoklonális antitest. A gyógyszer alkalmazását 2021 márciusában az EMA is engedélyezte a sclerosis multiplex relapszáló formáiban (RSM). Összefoglalónkban részletesen bemutatjuk a jelenleg SM-ben alkalmazott anti-CD20 monoklonális antitest-terápiák hatásmechanizmusát és hatékonyságát.
Idegtudományok
2021. DECEMBER 02.
Van-e összefüggés a krónikus gyulladásos demyelinisatiós polyneuropathia és a vakcináció között?
A krónikus gyulladásos demyelinisatiós polyneuropathia (chronic inflammatory demyelinating polyneuropathy, CIDP) a Guillain–Barré-szindrómához (GBS) hasonló betegség, amit a GBS-hez hasonlóan összefüggésbe hoznak a vakcinációval. Jelenleg az irányelvek mindkét betegpopuláció esetében javasolják az oltások felvételét, azonban keveset tudunk arról, hogy milyen hatással van a vakcináció a CIDP fellángolására. Jelen áttekintő közlemény annak próbált utánajárni, hogy milyen gyakorisággal jelentkezik CIDP vakcináció után, illetve milyen gyakori a kórkép vakcinációt követő fellángolása.
Idegtudományok
2021. NOVEMBER 11.
Klinikai döntéshozatal MOG antitest-asszociált betegségben
A szenzitív és specifikus sejtalapú esszék kifejlesztésével a humán myelin-oligodendrocyta glikoprotein (MOG) ellenes IgG-antitestek kimutatása lehetővé tette az anti-MOG antitest-asszociált betegség (anti-MOG antibody-associated disease, MOGAD) és az egyéb demyelinisatiós betegségek elkülönítését. A MOGAD, az aquaporin-4-asszociált neuromyelitis optica spektrum betegség (AQP4-NMOSD) és a sclerosis multiplex (SM) megkülönböztetését a betegségek különböző kórélettani háttere, klinikuma, terápiás és prognosztikus következményei egyaránt indokolják.
Magas aktivitású SM terhesség alatt – esetismertetés
33 éves, relapszáló-remittáló sclerosis multiplex miatt gondozott nőbetegünknél 4 éves Gilenya-kezelés után családtervezési szándék miatt gyógyszerváltást terveztünk, azonban a Gilenya leállításával szinte egy időben a beteg teherbe esett 2020 szeptemberében. A terhesség 14. hetében agytörzsi tünetekkel járó (szédülés, hányás, kettős látás, jobb arcfélzsibbadás, jobb alsó végtagi gyengeség), szteroid-lökéskezelést igénylő relapszusa zajlott, ami után Copaxone-t állítottunk be. A 26. héten azonban újabb, járásképtelenségig súlyosbodó, bal oldali hemiparesissel és dysarthriával járó relapszusa alakult ki. Tekintettel a terhesség alatt jelentkező, szokatlanul nagyfokú betegségaktivitásra, akut koponya-MRI-vizsgálatot kértünk, melyen az ismert SM határozott progressziója igazolódott, 9 új góccal, illetve jobb féltekei tumefaktív laesióval. A klinikai progresszió miatt a szteroid-kezelésen túl plazmaferézist is alkalmaztunk, ami mellett lassú javulás következett be. Az eset kapcsán is fontos hangsúlyozni a tudatos családtervezés és a megfelelő fogamzásgátlás jelentőségét minden fogamzóképes korú sclerosis multiplexes nőbetegnél. Páciensünk egészséges gyermeknek adott életet.
IVIG-en innen és túl – A CIDP kezelési lehetőségei kórházunk adatai alapján
A krónikus gyulladásos demyelinisatiós polyneuropathia (CIDP) a perifériás idegrendszer betegsége, ami kezelés nélkül maradandó rokkantságot okozhat. A kórházunkban gondozott betegek adatait tekintettük át az alkalmazott terápia típusának és hatékonyságának megítélése, a terápia okozta mellékhatások és azok gyakoriságának felmérése céljából. Az adatokat az országos CIDP-regiszterből, illetve a kórházi medikai rendszerből nyertük. A diagnosztikai kritériumok minden esetben teljesültek. A betegség típusos tünetekkel járt, 1-1 esetben észleltünk tisztán szenzoros formát, illetve DADS-variánst. Az átlagos életkor a betegség kezdetekor 52 év (medián) volt. 5 esetben először Guillain–Barré-szindróma, egy-egy esetben pedig polyneuropathia és kétoldali carpalis alagút szindróma volt a kezdeti diagnózis. A leggyakrabban alkalmazott kezelés az intravénás immungobulin (IVIG) volt, de több páciensnél végeztünk plazmaferézist, illetve néhány esetben tartós immunszuppresszív terápia is beállításra került. Két esetben autológőssejt-transzplantáció történt. A terápiák hatékonyságának megítélését nehezítette, hogy a mindennapi közkórházi gyakorlatnak nem része a pontozóskálák felvétele. Szteroidterápia egy esetben volt hatástalan, adekvát dózisú és időtartamú adagolás ellenére. Plazmaferézis vagy IVIG mellett a betegek többsége egyensúlyba került. Súlyosabb relapszusok esetén a beállított immunszuppresszív kezelés is hatékonynak bizonyult 1-1 esetben. A leggyakoribb mellékhatás az Imuran okozta hasi panaszok és laboreltérések voltak, két esetben fordult elő tartós szteroidkezelés következményeként osteoporosis kompressziós csigolyatörésekkel, egy esetben IVIG-kezeléshez társuló fejfájás. Összefoglalás: A krónikus gyulladásos demyelinisatiós polyneuropathia jól felimerhető és diagnosztizálható betegség, ami jól reagál adekvát dózisban és megfelelő ideig alkalmazott terápiára, így a tartós rokkantság megelőzhető. Kellő odafigyeléssel a kezelések mellékhatásai is kivédhetők.
Chorea minor
Az 5,5 éves gyermeknél egy hónappal lázas torokgyulladást követően polyarthritis zajlott, majd egy hónap múlva grimaszolás, vokális ticek jelentek meg. Később fokozódó figyelemzavar, bizarr végtagmozgások, fejrángás alakult ki. Törzsén, végtagjain számos hyperaemiás, gyűrű- szerű exanthema jelent meg. Pszichológiai, neurológiai vizsgálatai pszichés eredetet, vokális tic miatt kezdődő Tourette-szindrómát véleményeztek. Organikus ok tisztázása céljából vizsgáltuk, státuszában kifejezett hypotonia, jobb túlsúlyú ballisticus és choreiform mozgások, orofacialis dyskinesis, dysarthria, motoros imperzisztencia, nyelvfibrilláció volt észlelhető. Eszközfogáskészségét elvesztette, játszani, enni, rajzolni sem tudott. Koponya-MR negatív, a bal oldali nucleus caudatus tömegesebb volt. A liquor paraneoplasiás panel vizsgálata kétes volt (a Purkinje-sejtek citoplazmája, részben az elsődleges nyúlványokkal gyengén ábrázolódtak). Intrathecalis IgG-képzés nem igazolódott. A klinikai kép – lázas infekciót követő polyarthritis, erythema marginatum, viselkedés- és figyelemzavar, illetve cho- rea – alapján poststreptococcalis betegség merült fel. Torokváladék- tenyésztés negatív, AST jelzetten emelkedett volt. A szívultrahang eltérést nem talált. A major és minor kritériumok alapján betegségét reumás láz részeként jelentkező Sydenham-choreának tartottuk. Szteroid-, penicillin- és NSAID-terápia indult, mely mellett mind ízületi, mind neurológiai tünetei jelentősen regrediáltak. Másfél éves követése kapcsán két alkalommal észleltünk relapszust, interkurrens infekció, illetve tonsillectomia kapcsán. A tüneti szerek (haloperidol, tiapridal, carbamazepine) érdemi állapotjavulást nem eredményeztek, szteroid adására viszont mindkét alkalommal javultak a panaszai. Édesapjánál gyermekkorában zajlott poststreptococcalis polyarthritis miatt családi hajlam felmerül, HLA-vizsgálata folyamatban van. Konkluzió: Az antibiotikum-érában is felmerül chorea hátterében reumás láz, melynek diagnózisa a klinikai képen, valamint major és minor kritériumok jelenlétén alapul. A tüneti szerek és a tartós penicillinprevenció mellett immunterápiára is szükség lehet.
1.
2.
3.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről4.
5.
1.
2.
Klinikai Onkológia
Hasnyálmirigyrák: az ESMO klinikai gyakorlati irányelve a diagnózishoz, kezeléshez, követéshez*3.
Klinikai Onkológia
Gyógyszerbiztonsági szemelvények – a múlt tanulságai és a jövő lehetőségei4.
5.