Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 342
Új, innovatív prognóziskalkulátor áttétes gerinctumoros betegek számára
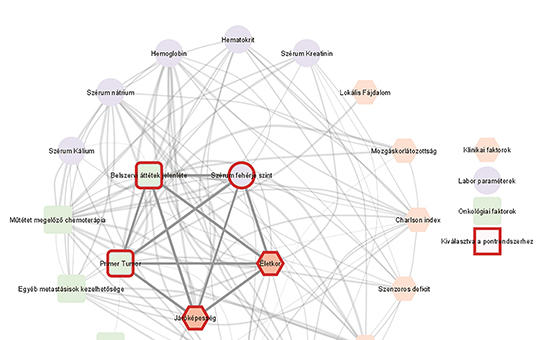
Kutatásunk célja volt egy prognózist jósló és terápiás opciót ajánló pontrendszer létrehozása a gerincmetasztázissal érintett betegek számára. Az egyre bővülő onkoterápiás lehetőségek és a prolongált túlélés miatt egyre gyakrabban foglalkozunk a primer tumor csontáttétei miatt kialakult klinikai tünetek megoldásával. A csigolyaáttétek az okozott neurológiai deficittünetek, illetve a fájdalom által szignifikáns életminőségbeni csökkenést okozhatnak, és a várható élettartamot is jelentősen befolyásolhatják. A prognózist megfelelő pontossággal jósló pontrendszer segítségünkre lehet a személyre szabott gyógyítás megvalósításában. Retrospektív klinikai vizsgálatot végeztünk az Országos Mentális, Ideggyógyászati és Idegsebészeti Intézetben a 2008 és 2018 között műtéti úton kezelt 18 év feletti gerincáttétes betegek adataiból. 454 beteg adatait elemeztük. Túlélési analízist (Kaplan–Meier-, log-rank-, Cox-modell) végeztünk, hálózati korrelációs vizsgálat segítségével választottuk ki pontrendszerünk prognosztikai faktorait úgy, hogy a vágópont-analízis során maximáljuk annak C értékét (predikciós képességi indexét). Multivariáns Cox-analízis eredményeként öt prognosztikai faktort azonosítottunk (a primer tumor típusa, életkor, járóképesség, belszervi áttétek, szérumfehérjeszint). Rendszerünk a 10 éves vizsgált periódusban átlagosan 70,6%-os pontossággal prognosztizált. Szimptómás, műtéten átesett, gerincmetasztázisban szenvedő betegek nagy esetszámú, egycentrumos, retrospektív műtéti adatait felhasználva létrehoztuk rizikóbecslő rendszerünket, ami segítheti a terápia megválasztását. Rizikókalkulátorunk online is elérhető az alábbi címen: https://emk.semmelweis.hu/gerincmet.
Minimálisan invazív és O-arm asszisztált en bloc gerincdaganat-reszekciók
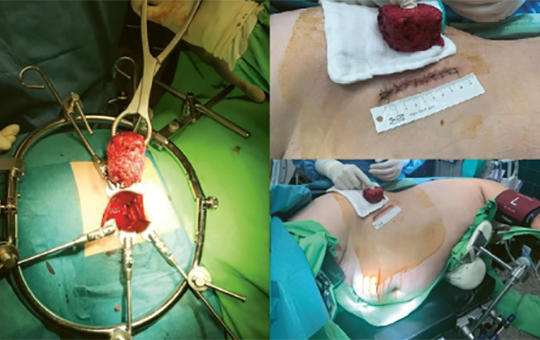
A gerincdaganatok en bloc eltávolítása szükséges primer gerincdaganatok, illetve metasztázisok válogatott eseteiben, amikor az alapbetegség jó prognózisú, onkológiailag jól kontrollált. Három esetet mutatunk be, amelyekben az en bloc reszekciót O-arm asszisztált navigációval vagy minimálisan invazív ventralis feltárással végeztük. O-arm navigáció segítségével végzett osteotomiákkal, az ép csigolyarészek megkímélésével egy emlődaganatos beteg szoliter Th.V. metasztázisát távolítottuk el en bloc. Egy chordomás (L.IV.) és egy carcinoid tumoros (L.V.) betegnél kétoldali minimálisan invazív retroperitonealis feltárásból corpectomiát végeztünk mikroszkóp segítségével. Az emlődaganatos betegnél morbiditás nem következett be, 1 évvel a műtét után lokális recidíva nem ábrázolódott, azonban több csigolyában is metasztázisok jelentek meg az aktív onkológiai kezelés ellenére. Az L.IV. chordomás betegnél a műtét után morbiditást tapasztaltunk, bal alsó végtagi paresis, járásnehezítettség jelentkezett. Másfél évvel a műtét után lokális recidíva nem ábrázolódott. A csak ventralis feltárásnak köszönhetően a gerinc dorsalis, ép struktúráit meg tudtuk őrizni. A carcinoid tumoros beteg esetében morbiditást nem tapasztaltunk. A kontrollvizsgálatokkal lokális recidíva 1 évvel a műtét után nem ábrázolódott. Mind az O-arm navigáció, mind a minimálisan invazív elülső gerincfeltárások segíthetnek a sebészi morbiditás csökkentésében és az ép, nem daganatos gerincstruktúrák megőrzésében. Ez utóbbi fontos szerepet játszhat a gerinc hosszú távú stabilitásának biztosításában. Az új módszerek alkalmazása csak akkor fogadható el, ha onkológiai szempontból, hosszú távon, legalább azonos eredményt tudnak elérni a hagyományos megközelítésekhez képest.
Nonproteinuriás diabeteses vesebetegség
A diabeteses nephropathia a krónikus vesebetegség egyik leggyakoribb oka. Az utóbbi években megfigyelték, hogy a klasszikus protein- uriával járó fenotípus mellett egyre gyakoribbá válik a betegség proteinuria nélkül, a vesefunkció progresszív beszűkülésével járó, úgynevezett nonproteinuriás formája. Ennek szövettani képe, kórélettani jellemzői és lefolyása is részben különbözik a proteinuriás fenotípustól. Az előbbi inkább az atheroscleroticus vesebetegség jegyeit mutatja mind szövettani, mind a társult cardiovascularis betegségek vonatkozásában, és progressziója lassabb, mint a proteinuriás formának. Mindez a szűrés, a terápia és a prognózis vonatkozásában is jelentőséggel bír. A nonproteinuriás diabeteses nephropathiáról relatíve kevés adat áll rendelkezésre, de mind a klinikumban, mind a tudományos kutatásban figyelmet érdemel.
Neuronalis sejtfelszíni autoantitest-mediált autoimmun encephalitis betegek klinikai jellemzőinek retrospektív multicentrikus vizsgálata Magyarországon
Bevezetés: A 2012–2018 közötti időszakban laboratóriumunk országos centrumként működött az autoimmun encephalitisre (AE) jellemző neuronalis sejtfelszíni ellenanyagok (anti-NMDAR, anti-LGI1, anti-GABABR, anti-Caspr2, anti-AMPAR1/2) tesztelésében. A vizsgált időszakban az antitestmérésekre érkezett szérum- és liquorminták retrospektív értékelése során a betegek 5,8%-ában (60 beteg) találtunk pozitivitást. Anyag és módszer: Saját fejlesztésű online kérdőívvel 30 sejtfelszíni ellenanyag-pozitív AE-beteg (19 NMDAR, 6 LGI1, 3 GABABR, 3 Caspr2) klinikai jellemzőinek retrospektív elemzését végeztük el négy fő klinikai központban neuroimmunológusok segítségével. Eredmények: A betegek 63%-a férfi, átlagos életkoruk 39 év volt. A leggyakoribb klinikai megjelenés a pszichiátriai tünet (83%), az epilepsziás rosszullét (73%) és a memóriazavar (50%) volt. Hyponatraemia (83%) és faciobrachialis dystoniás rohamok (50%) kizárólag az LGI1 encephalitis betegekben jelentkeztek. Egy esetben herpes simplex vírus- (HSV-) encephalitis előzte meg a szekunder NMDAR-encephalitis kialakulását. A betegek 27%-ában társuló tumor volt jelen. Az AE-betegek 37%- ánál nem volt gyulladást jelző eltérés a liquor- és a koponya- MRI-vizsgálatok során, azonban majdnem a betegek felében (48%) EEG-eltérést detektáltak. A betegek 80%-a első vonalbeli immunterápiában (szteroid, IVIG, plazmaferézis) részesült. Az esetek döntő többségében (83%) kedvező volt a betegség kimenetele, azonban a jelen lévő tumor kedvezőtlenebb betegségkimenetellel társult. Következtetések: Jelen tanulmányban elsőként vizsgáltuk a neuronalis sejtfelszíni autoantitest-mediált AEbetegek klinikai jellemzőit a magyar populációban. Eredményeink egybehangzóak a korábbi szakirodalmi adatokkal az AE klinikai jellemzőit és kimenetelét illetően, azonban az NMDAR-encephalitis elsősorban fiatal férfiakban jelentkezett, valamint egyik esetben sem társult ovariumteratomával. Az AE-betegek egyharmadában nem volt gyulladást jelző eltérés a liquor- és a koponya- MRI-vizsgálatok során, ami a klinikai tünettan és az ellenanyag-vizsgálatok jelentőségét hangsúlyozza az AE diagnózisának felállításában.
Egy igazi autoimmun kihívás – LGI1 autoimmun encephalitis sikeres kezelése Covid mellett
Bevezetés: Az LG1-encephalitis ritka, a feszültségfüggő kálium-csatorna elleni ellenanyag által mediált kórkép, ami leginkább epilepsziás rohamokkal, memóriazavarral, viselkedésváltozással társul. MR-képen a temporalis lebeny és a hippocampus intenzitásváltozása látszódhat. Akut szakaszban plazmaferézis, IVIG-, illetve hosszú távú immunszuppresszáns terápia mellett jó a prognózisa, Covid-19-infekció mellett azonban minden kórkép kezelése kihívásokkal teli, és prognózisa megjósolhatatlan. Esetleírás: 75 éves, diabeteses nőbetegünket zavartság, bizarr viselkedés és beszédzavar miatt vettük fel 2021. 03. 31-én. Neurológiai státuszában kifejezett agitáltság mellett szenzoros túlsúlyú kevert aphasiát észleltünk. Az elvégzett koponya-CT/CTA és -MR kórjelző eltérést nem igazolt. A láztalanság ellenére végzett lumbalpunctio során jelentősen emelkedett fehérjeértéket és mérsékelten emelkedett fehérvérsejtszámot találtunk. Az elvégzett vírus- és baktériumszerológiai, illetve PCR-vizsgálatok kórokozót nem igazoltak. A klinikum alapján felmerült autoimmun encephalitis lehetősége, emiatt empirikusan nagy dózisú szteroidterápiát (7 napig napi 500 mg Solu-Medoll) indítottunk. A kezdeti progressziót mutató globális aphasia fokozatosan szűnt, mérsékelt dezorientáció, kismértékű zavartság maradt vissza. Javuló neurológiai státusz mellett azonban tachy-dyspnoe, deszaturáció jelentkezett, és ugyanaznap igazolódott az LG1-ellenanyag jelenléte és a Covid-19-infekció. Ezt követően párhuzamosan kezeltük a beteg encephalitisét és Covidját Neurológiai Osztályunk Covid-részlegén. Többszörös szövődmények ellenére, a rendelkezésre álló terápiás lehetőségek teljes palettáját alkalmazva, a neurológiai osztály és a társszakmák teammunkája mellett a beteg neurológiai és belszervi állapotát is sikerült rendezni, majd a beteget rehabilitációs kezelést követően otthonába tudtuk bocsátani. A részletes esetismertetését előadásunk tartalmazza. Konklúzió: az LG1-encephalitis többnyire jó prognózisú, adekvát terápia mellett jól kezelhető kórkép. Covid- 19-fertőzés mellett kórházi kezelése rendkívül megnehezül, de jelentős terápiás, illetve emberi erőfeszítések mellett a betegek gyógyulása elősegíthető.
Paradigmaváltás a krónikus szívelégtelenség gyógyszeres terápiájában
A szívelégtelenség incidenciája, prevalenciája folyamatosan növekszik, a betegség morbiditása és a mortalitása továbbra is nagy, így a kórkép jelentősége óriási, megfelelő kezelése kiemelt jelentőségű. A betegség prognózisát javító érdemi evidenciák továbbra is csak csökkent balkamra-funkcióval járó krónikus szívelégtelenség (HFrEF) kezelése esetén állnak rendelkezésre. Az elmúlt évtizedekben számos „mérföldkővizsgálat” született, melyek eredményei a mai napig alapjaiban határozzák meg a betegség terápiáját. A HFrEF bázisterápiája sokáig három alappillérre épült: angiotenzinkonvertáló-enzim- (ACE-) gátló, β-blokkoló és mineralokortikoidreceptor-antagonista, melyek I/A ajánlási szinttel szerepelnek a különböző szívelégtelenség-ajánlásokban. 2014-ben publikálták az áttörő sikert hozó, nagy jelentőségű PARADIGM-HF (heart failure) vizsgálatot, amelyben egy teljesen új gyógyszercsoportot, az angiotenzinreceptor-blokkoló/ neprilysininhibitor (ARNI-) vegyületek csoportjába tartozó sacubitril/valsartant vizsgálták HFrEF-betegeken. A vizsgálat eredménye szerint a sacubitril/valsartan szignifikáns mértékben, 20%-kal csökkentette a cardiovascularis (CV) halálozás és a szívelégtelenség miatti hospitalizáció primer összetett végpontját, valamint 16%-kal csökkentette az összmortalitást egy aktív komparátorhoz, az HFrEF terápiájában a legnagyobb evidenciákkal rendelkező enalaprilhoz képest. Az Európai Kardiológusok Társasága (European Society of Cardiology, ESC) 2016-os szívelégtelenség-irányelve I/B evidenciaszinttel javasolja a sacubitril/ valsartan alkalmazását ACEI helyett a szívelégtelenség miatti hospitalizáció és halálozás csökkentése céljából olyan ambuláns HFrEF-betegek esetén, akik az optimális ACEI, β-blokkoló (BB) és mineralokortikoidreceptor-antagonista (MRA-) kezelés ellenére is panaszosak maradnak. A későbbiekben sacubitril/valsartannal több kisebb vizsgálatot is publikáltak kissé eltérő indikációkkal és más betegcsoportokon. A PIONEER-HF vizsgálat bizonyította, hogy a sacubitril/valsartan terápia korai, az akut szívelégtelenség stabilizációját követően történő megkezdése biztonságos és hatékony HFrEF-betegek esetén, gyorsabban csökkenti a szívelégtelenség prognózisával korreláló NT-proBNP-szintet, mint az enalapril. A TRANSITION és a TITRATION vizsgálat a sacubitril/valsartan terápia kezdetéről, a dózistitrálás módjáról adott hasznos információkat. A sacubitril/ valsartan megjelenése új korszak kezdetét jelentette néhány évvel ezelőtt a HFrEF terápiájában. Ez a korszak Magyarországon most zajlik. Elképzelhető, hogy az SGLT-2-inhibitoroknak köszönhetően egy újabb korszak kapujában állunk, és erre várhatóan választ ad majd az ESC idén megjelenő új szívelégtelenség-ajánlása.
Koronavírus-betegség reumatológiai betegek körében – a megfertőződés, a súlyos lefolyás és a hatásos vakcináció esélyei
A gyulladásos és reumatológiai betegségekben szenvedők koronavírus-fertőzöttségének gyakorisága nem tér el jelentősen a helyi népesség fertőzöttségi arányaitól. A nagyobb adagú kortikoszteroiddal kezeltek, elsősorban a súlyosabb szisztémás autoimmun betegek megfertőződésének nagyobb a valószínűsége. A hospitalizáció, illetve a mortalitás esélye sem tér el lényegesen a népességi Covid-fertőzöttekétől. E tekintetben is kivételnek számítanak a nagyobb mennyiségű kortikoszteroidokkal és citosztatikumokkal kezeltek. A Covid-prognózist illetően az általában kockázatot jelentő társuló betegségek (a Covid előtti reumatológiai felmérések szerint) ugyanazok a gyulladásos és a nem gyulladásos reumatológiai betegek körében. Ezért nem a reumatológiai betegség miatt súlyos a Covid-kimenetel kockázata, hanem az időskor és az ebben az életkori csoportban egyaránt fellelhető cardiopulmonalis és anyagcsere-betegségek következtében. A gyulladásos reumatológiai/autoimmun betegek kezelésének fegyvertárából hipotetikus alapon a súlyos Covid kezelésére kiválasztott készítmények közül a dexamethason hatásossága bizonyított egyértelműen. Speciális betegcsoportokban kedvező hatása lehet az interleukin-6-antagonistáknak és a JAK-gátlóknak. A reumatológiai és az autoimmun betegségek kezelésére alkalmazott betegségmódosító gyógyszerek, köztük az antimetabolitok, az anticitokin immunológiai készítmények és a JAK-gátlók nem jelentenek Covid-kockázatot, adásukat nem kell megszakítani. Kivétel ez alól a korai B-sejteket közvetlenül elpusztító rituximabkészítmény, amely a súlyos kimenetel esélyét növeli a kezeltekben, feltehetően aktív betegségük és a gátolt humorális immunvédekezés miatt. A Covid-vakcináció szintúgy nem jelent speciális akut kockázatot reumatológiai és autoimmun betegek számára. Hosszabb távon még vizsgálandó, hogy az immunválasz erősségét és tartósságát reumatológiai betegekben a vakcináció speciálisan befolyásolja-e.
A GLP-receptor-agonisták alkalmazásának potenciális előnyei Covid-19-járvány idején
Cukorbetegségben fokozott a SARS-CoV-2-fertőződés esélye, és a betegség lefolyása is súlyosabb. Az alapbetegséghez társuló elhízás és cardiovascularis betegség szintén súlyosbítja a fertőzés kimenetelének prognózisát. A 2-es típusú cukorbetegség kezelésére használt glükagonszerű peptid-1-receptor-agonisták (GLP1-RA) erőteljesen, a hypoglykaemia kockázatának jelentős növelése nélkül csökkentik a vércukorszintet, hozzásegítik a betegeket a fogyáshoz, és csökkentik a cardiovascularis betegségek kialakulásának, rosszabbodásának valószínűségét. Számos hatásuk révén mintegy felkészítik a cukorbetegeket arra, hogy SARS-CoV-2-fertőzés esetén kevesebb szövődménnyel vészeljék át a betegséget, és kedvező immunológiai hatásuk miatt a citokinvihar kifejlődését is mérsékelik. A szerzők összefoglalják a GLP1-RA-k potenciális kedvező hatását a SARS-CoV-2-fertőzésre.
A pancreascarcinoma preoperatív kezelésének átformálása a precíziós medicina korában
Ez az áttekintés összefoglalja a pancreascarcinoma preoperatív kezelési stratégiáira vonatkozó legújabb bizonyítékokat, és a nem metasztatizáló betegség esetén tárgyalja a személyre szabott terápiás módszer mielőbbi bevezetésének szükségességét és észszerű magyarázatát. A pancreascarcinoma molekuláris diverzitása, és annak a prognózisra és a terápiás válaszra gyakorolt hatása, kombinálva az „összes ígéretes új szerrel” végzett kezelések sikertelenségével, jelentős hatást gyakorol a betegség lefolyására, ami paradigmaváltást tesz szükségessé a genomika által irányított megközelítés felé. Ez különösen fontos a preoperatív, potenciálisan gyógyítható esetekben, ahol a személyre szabott kezelés megválasztásában jelentős potenciál rejlik, ami csökkenti a hasnyálmirigyrák mortalitását.
Rapidan progrediáló glomerulonephritis megtévesztő esete
Az egyre csökkenő incidenciájú poststreptococcalis glomerulonephritis (PSGN) helyett egyre gyakrabban találkozhatunk infekcióhoz társult glomerulonephritissel (IRGN). Mind a kórkép etiológiájában, mind lefolyásában és prognózisában jelentős különbségek mutatkoznak a PSGN-hez képest. Külön figyelmet érdemel az IRGN egy morfológiai variánsa, amely aktuálisan zajló Staphylococcus aureus-infekció mellett jelentkezik, alsó végtagi purpurás bőrelváltozásokkal, IgA-domináns glomerulonephritissel, amely kísértetiesen hasonlíthat Henoch–Schönlein-purpurára (HSP). Rendkívül fontos azonban megkülönböztetni a HSP-t és a Staphylococcus-fertőzés okozta IgA-domináns glomerulonephritist egymástól, mert a HSP immunszuppresszáns, míg a Staphylococcus-fertőzéssel összefüggő glomerulonephritis antibiotikus terápiát igényel. Esetünkkel erre a differenciáldiagnosztikai nehézségre szeretnénk felhívni a figyelmet.
1.
2.
3.
4.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről5.
1.
2.
Klinikai Onkológia
A rosszindulatú daganatok fenotípusának plaszticitása és az immunogén mimikri3.
Klinikai Onkológia
A szarkopénia mérése komputertomográfiával és jelentősége az onkológiai betegeknél4.
5.