Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 436
Európa összefogott a ritka betegségekkel élőkért
A kontinens döntéshozói, egészségpolitikusai, betegszervezetei, szakemberei, a digitális egészség úttörői közös platformra léptek a Biogen vállalat, a Reuters Events és az EU40 együttműködésével megrendezett virtuális konferencián, hogy kollektív tudásukkal még hatékonyabban lépjenek a ritka betegek érdekében, hogy mind a diagnózishoz, mind az ellátáshoz való hozzáférés Európa-szerte egységes legyen. Költséghatékonyságot célzó stratégiát, az ismeretek összegyűjtését és az információhoz való hozzáférés javítását, erősítését hirdették meg. Dr. Molnár Mária Judit, a Semmelweis Egyetem Genomikai Medicina és Ritka Betegségek Intézetének igazgatója értékelte az összefogás jelentőségét és mutatta be a hazai helyzetet.
Daganatos betegek rehabilitációja
Hazánkban a daganatos megbetegedések száma folyamatosan növekszik. A KSH adatai alapján 2017-ben már 376 709 fő szenvedett valamilyen daganatos megbetegedésben. A betegség hosszan tartó, idült folyamat, a kezelések okozta fizikai terhek pedig megnehezítik a betegek testi-lelki egyensúlyának megőrzését. A daganatos beteg életminősége megváltozik, csökken a munkaképessége, megváltozik a családban betöltött szerepe, testi és érzelmi erőnléte, megélhetési helyzete. Ezek a problémák rehabilitációs intervenciókkal orvosolhatók, de az onkológiai rehabilitáció hazánkban sok helyen, sajnos, még nem képezi az ellátás standard részét. Valójában az onkológiai rehabilitáció eltér a többi betegség rehabilitációs munkatervétől. Az onkológiai rehabilitációs tervezetet rugalmasabban, differenciáltabban kell kezelni, mindig figyelembe kell venni a betegségből és a kezelésekből származó változásokat. Emiatt pedig egyre nő az igény a bizonyítékon alapuló rehabilitációs intervenciókra, ezért a mi célunk, a nemzetközi szakirodalom alkalmazásával, a daganatos betegek, köztük az áttétes betegek rehabilitációs lehetőségeinek az áttekintése, amelyekkel csökkenteni lehet a kezelések mellékhatásaként kialakult fájdalmakat, mozgásszervi és tápláltsági problémákat, hogy ezáltal lehetőség nyíljon a betegek életminőségének jelentős mértékű javítására.
A méhnyakrák korszerű onkológiai kezelése
Világszerte évente több mint félmillió nőnél igazolódik méhnyakrák, és körülbelül 300 000 halálesetet okoz a betegség. A nyugati társadalmakban a cervixcarcinoma incidenciája és mortalitása csökken a humán papilloma vírus (HPV) elleni vakcinációnak és a populációs szintű szűrésnek köszönhetően. A fejlődő világ országaiban azonban továbbra is emelkedő a tendencia. A rákmegelőző állapotok és a korai méhnyakrák definitív onkológiai ellátása a stádiumfüggő kiterjesztéssel végzett műtétek révén lehetséges. A posztoperatív sugárkezelés vagy kemoradioterápia szükségessége a patológiai rizikófaktorok alapján határozható meg. Előrehaladott méhnyakrákban a definitív kemoradioterápia vagy a szisztémás kezelés a terápiás alternatívák. A fiatal betegek részéről gyakran felmerülő kívánság a fertilitásmegtartás, amely az onkológiai elvekkel csak jól definiált határok között egyeztethető össze, alapos felvilágosítást követően. A terhesség alatt felismert méhnyakrák becsült incidenciája 1,4-4,6 eset/100 000 szülés, amelynek ellátása során, az onkológiai szempontokon túl, a magzat biztonságát is szem előtt kell tartanunk az anya preferenciái alapján. A klasszikus kemoterápia mellett a biológiai szerek is megjelentek a közelmúltban a méhnyakrák szisztémás kezelési lehetőségei között: első vonalban bevacizumabbal egészíthető ki a ciszplatin-paclitaxel kombináció közel négy hónapos túlélési előnyt nyújtva a betegek számára; míg másodvonalban pembrolizumab adható mikroszatellita-instabil vagy PDL-1-et expresszáló (combined positive score [CPS] ≥1), illetve magas tumormutációs terheltséget (TMB ≥10) mutató daganatok esetén. A jelen munka egy rövid összefoglalót szolgáltat a méhnyakrák megelőzéséről, kivizsgálásáról és onkológiai ellátásáról.
Oncompass Medicine lett idén Európa legígéretesebb technológiai vállalkozása
Az Oncompass Medicine nyerte a Digitaleurope versenyét, így a Future Unicorn Award kitüntetést elnyerve idén egy magyar biotechnológiai cég lett a kontinens legígéretesebb vállalkozása.
Egészségpolitika
2021. FEBRUÁR 05.
Vége a TVK 16 éves uralmának – újraszabták a kórházi finanszírozást
A teljesítmény-volumenkorlát elve szerinti számolás tizenhét év után megszűnik a szakellátásban.Bevezetik az éves keretet a finanszírozásban, illetve szakmákra lesz kiosztva ez a pénz. Az idén életbe lépett változás megkérdezett szakértőink szerint leginkább átnevezés, de nem jelent átütő változást. Igaz, várhatóan megszűnik a kórházak mozgástere abban, hogy a jól és kevésbé jól fizetett területek között „játszanak”.
Covid-19 – a rákgyógyításban is nehézségeket okozott
A betegek, de még az orvosok is nehéz helyzetbe kerültek a világjárvány hozta egészségügyi átrendeződés kapcsán. Egyrészt volt, ahol hónapokig nem is fogadták a betegeket, a már megkezdett kezelések is abbamaradtak, másrészt maguk az érintettek is tartottak bemenni az intézményekbe. A kormányrendeletek ellenére tanácstalan volt gyógyító és páciens egyaránt.
A méh rosszindulatú daganatainak korszerű onkológiai kezelése
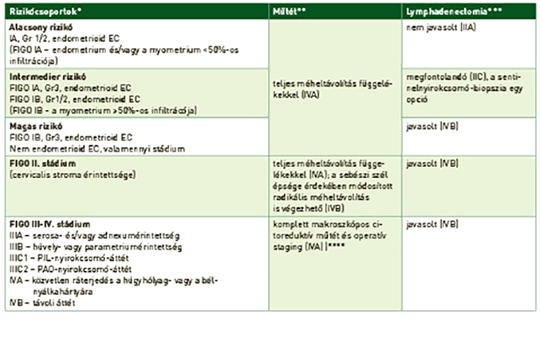
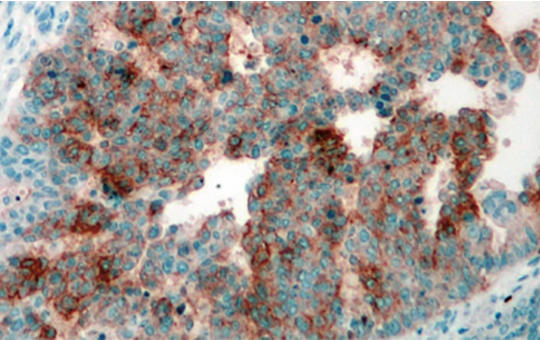
Világviszonylatban évente közel 400 000 nőnél igazolódik méhtestrák, amely 2018-ban körülbelül 90 000 nő halálát okozta. Az esetek túlnyomó részét a méhnyálkahártya hormonérzékeny hámjából kiinduló endometriumcarcinomák (EC) alkotják. A sarcomák a méhtestrákok alig 3%-át adják. Az EC-k 80-85%-a jó prognózisú, mivel alacsony gradusú és korai stádiumban kerül felismerésre, amikor a műtét és az esetleges posztoperatív kezelés révén a gyógyulás reális terápiás cél. Az előrehaladott stádiumban diagnosztizált EC és a nem endometrioid altípusok esetén a prognózis lényegesen rosszabb. A magas rizikójú EC optimális adjuváns kezelésére irányuló vizsgálatok egy része még folyamatban van, illetve a bővülő molekuláris ismeretek újabb vizsgálatokat generálnak. A méhtestsarcomák esetében is a sebészi eltávolítás jelenthet kuratív megoldást, az adjuváns kezelésre vonatkozó evidenciák bizonytalanok, egyéni mérlegelést igényelnek. A modern onkoterápia érájában már nemcsak a betegségmentes élet meghosszabbítására, hanem az élet minőségének minél teljesebb megőrzésére is törekszünk. A nőgyógyászati onkológiában ezt jelenti a fertilitás vagy a funkcionáló ováriumok lehetőség szerinti megőrzése; a magas morbiditással járó szisztémás lymphadenectomia indikációs körének szűkítése; a kedvezőbb mellékhatásprofilú brachytherapia alkalmazása a teljes kismedencei besugárzás helyett. A modern onkoterápia az úgynevezett biológiai kezelések által az előrehaladott betegségek ellátásának is a részévé vált: kemoterápia mellett/után progrediáló esetekben a pembrolizumab az EC és a sarcomák esetén is alkalmazható mikroszatellita-instabilitás vagy magas tumormutációs terheltség esetén, míg az NTRK fúziós gén jelenlétében larotrectinib vagy entrectinib mint célzott tirozinkináz-gátlók javasolhatók. Az EC-k 70-80%-át kitevő mikroszatellita-stabil esetekben (nem endometrioid altípusokban is!) a pembrolizumab lenvatinibbel kombinációban adható a kemoterápia után. Az EC területén gyarapodnak továbbá az egyéb célzott terápiás szerekkel szerzett tapasztalatok is (anti-HER2 serosus carcinomában, mTOR-gátló kezelés, endokrin terápia, más immun checkpoint inhibitorok, tirozinkináz-gátlók, PARP-gátlók és kombinációs kezelések). A jelen munka a méhtestrákok onkoterápiájáról kíván rövid összefoglalást nyújtani az aktuális szakmai ajánlások és a folyamatban lévő vizsgálatok bemutatásával.
Agnosztikus terápia onkológiai alkalmazása
A tumoragnosztikus terápia az onkológiai kezelés ígéretes lehetősége, azonban a potenciális célpontok klasszifikálása, validálása, azok egységes módszerek szerinti kimutatása elengedhetetlen. A tumoragnosztikus kezelések engedélyezése új típusú, biomarker-vezérelt klinikai vizsgálatok bevezetését tette szükségessé. Jelenleg három tumoragnosztikus molekuláris célpont ismert: a daganatok magas fokú mikroszatellita-instabilitása (MSI-H), a neurotrop-tirozinkináz-receptor (NTKR) gének fúziója, valamint a daganatok magas tumormutációs terhelése (TMB-H). A pembrolizumab (anti-PD-1 antitest) az első tumoragnosztikus indikációban is törzskönyvezett gyógyszer, amelyet először MSI-H daganatok kezelésére engedélyeztek, majd később a magas TMB is bekerült az indikációk közé. Az NTKR-fúziót hordozó daganatok kezelésére a larotrectinib és az entrectinib került engedélyezésre.
Hányáscsillapítás az onkológiai kezelések során
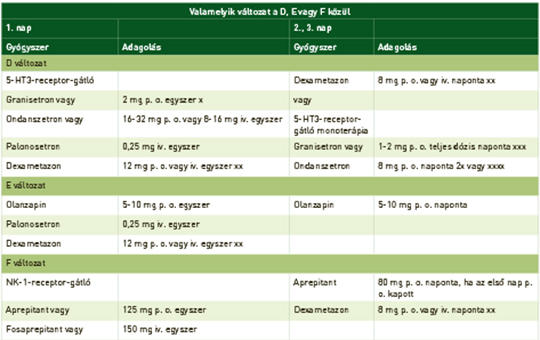
A hányinger és hányás egy többlépcsős folyamat, amely a központi idegrendszer irányítása alatt áll. A hányást kiváltó ingerek pszichés hatásra az agykéreg felől érkezhetnek vagy a nervus vaguson keresztül. A nyúltvelőben speciális magvak találhatók, amelyek a hányást kiváltják. Legfontosabb ingerületátvivő anyagok a szerotonin, a P-anyag és a dopaminok. A kemoterápiás szerek különböző arányban okoznak hányingert és hányást. Az 5-HT3- és NK-1-receptor-antagonisták a legjelentősebb hányinger-csillapítók. Szakmai ajánlások javasolják a gyógyszer-kombinációkat a különböző kemoterápiák okozta hányás csillapítására. A fix, szájon keresztül alkalmazható kombináció: netupitant és palonosetron (NEPA) növeli a betegek terápiahűségét. Az összefoglaló kitér a speciális hányingerek és hányások ismertetésére: áttöréses, többnapos kemoterápia okozta, sugárterápia során kialakult és a megelőlegezett hányásokra, valamint a gyermekkori hányáscsillapítás problematikájára is.
Az onkológiai gyógyszerész táguló szerepköre
A technológiai haladás felszabadította a gyógyszerészeket, akiknek ma már nem kell a gyógyszerkiadás biztonsági ellenőrzésére fókuszálniuk, és egyre több betegágy melletti feladatot is vállalhatnak, részt vehetnek akár az őssejttranszplantáció kivitelezésében vagy a farmakogenomikai eredmények értelmezésében is.
1.
2.
3.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről4.
5.
1.
2.
Klinikai Onkológia
A rosszindulatú daganatok fenotípusának plaszticitása és az immunogén mimikri3.
Klinikai Onkológia
A szarkopénia mérése komputertomográfiával és jelentősége az onkológiai betegeknél4.
5.