Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 245
A corticalis silent periódus klinikai alkalmazása
A primer motoros kéreg transcranialis mágneses stimulációja (TMS) a központi és a perifériás motoros pályák noninvazív vizsgálatára alkalmas eljárás. A célizom akaratlagos kontrakciója során végzett TMS hatására fiziológiásan átmenetileg megszűnik az elektromiográfiás tevékenység. Ezt a jelenséget corticalis silent periódusnak (CSP) nevezzük.
Modern idegsebészeti technikák a krónikus fájdalom kezelésében
A krónikus fájdalomszindrómák több mint 80 millió embert érintenek Európában. A gyógyszeres kezelésre nem reagáló deafferentációs fájdalmak csökkentésére már 1954-ben publikálta Heath a mély agyi stimulációs módszert. A célpontok a szenzoros thalamus, a septalis area és a nucleus caudatus voltak.
Migrénes stroke, migrén és stroke
A migrén és a stroke kapcsolata több szintű. Mivel mindkettő gyakori, így ischaemiás stroke más okból migrénben is szenvedő betegnél is kialakul. Az ischaemiás stroke tünetei hasonlíthatnak aurás migrénre, és valódi migrénes infarktus (MI) is kialakulhat. Ez utóbbiról akkor beszélünk, ha a migrénroham teljesíti az alábbiakat: Aurás migrénben szenvedő betegnél jelentkezik, megfelel a korábbi rohamoknak, kivéve, hogy egy vagy több auratünet tovább tart, mint 60 perc, képalkotó vizsgálat infarktust igazol a megfelelő területben és más ok kizárható. A migrénes infarktus incidenciája alacsony, az összes ischaemiás stroke 0,2–0,5%-a. Ez a fiatalok körében azonban 13% is lehet. Az MI gyakoribb nőkben, elsősorban a hátsó érterületet érinti (posterior: 70–80%), általában kisméretű (64,7%), többszörös laesio észlelhető az esetek 41,2%-ában.
Folyamatos EEG-monitorozás neurológiai szubintenzív osztályon
Kritikus állapotú betegnél az agyi funkciók károsodása akár órákkal is megelőzheti a neurológiai fizikális vizsgálattal észlelhető állapotromlást. A corticalis funkciók folyamatos tér- és időbeli követésére a tartós EEG- (continuous EEG, cEEG) monitorozás érzékeny vizsgálómódszer. Vizsgálatunk célja az OMIII Szubintenzív osztályán a cEEG-monitorozás klinikai alkalmazhatóságának vizsgálata súlyos idegrendszeri kórképekben.
Minor fizikális anomáliák epilepsziában
Az epilepszia etiológiájának vonatkozásában végzett újabb vizsgálatok rámutattak arra, hogy az epileptogenezisben az in utero, illetve a postnatalis kóros idegrendszeri fejlődés is szerepet játszik számos olyan epilepsziaszindróma esetében is, melyeket korábban egy specifikus anomáliának tulajdonítottak.
Idegtudományok
2022. ÁPRILIS 25.
Nagyérelzáródás detektálása akut ischaemiás stroke-ban gépi tanulásos módszerrel
Az akut ischaemiás stroke (AIS)-ok mintegy 30%-át nagyérelzáródás (large-vessel occlusion, LVO) okozza, mely a többi ischaemiás stroke-hoz képest súlyosabb tünetekkel és rosszabb kimenetelekkel jár, amennyiben kezelése nem sürgősen történik meg. A nagyérelzáródás intravénás thrombolysisen (IVT) túl endovascularis thrombectomiával (EVT) is kezelhető, melynek hatékonyságát a stroke kimenetele súlyosságának mérséklésében több vizsgálat is bizonyítja. Az EVT-k elvégzését ugyanakkor megnehezíti a korlátozottan elérhető, neurointervenciót végző stroke-centrumok (comprehensive stroke centers, CSC) száma, valamint az, hogy az LVO megléte csak képalkotó vizsgálatokkal igazolható, ami az esetek döntő többségében CT-angiográfiás vizsgálatot takar.
Idegtudományok
2022. JANUÁR 28.
Centrális és perifériás eredetű szédülés differenciáldiagnosztikája sürgősségi osztályos körülmények között
A szédülés, a bizonytalanság és az egyensúlyzavar a sürgősségi osztályos megjelenések mintegy 4%-ában szerepel vezető panaszként. Sürgősségi osztályos körülmények között a fő kihívást a jóindulatú vestibularis kórképek és a veszélyes, központi idegrendszeri kórképek differenciálása jelenti. A hátsó keringési stroke-ok mintegy 20%-ában a szédüléssel asszociáltan nincs jelen nyilvánvaló neurológiai tünet, sőt a klinikailag BPPV-ként diagnosztizált esetek mintegy 5%-ában, a neuritis vestibularisként diagnosztizált esetek 25%-ában valójában stroke áll a panaszok hátterében. Egy gyakran alkalmazott megközelítés a cardiovascularis rizikófaktorok felmérésén alapul, ugyanakkor ezt a stratégiát sok kritika éri a túlzottan gyakran indikált koponya-CT-vizsgálatok miatt, melynek szenzitivitása a hátsó keringés ischaemiás eltéréseire csupán 16–42%. A DWI MR-szekvencia ennél jóval érzékenyebb, ugyanakkor sokkal drágább és sokkal nehezebben hozzáférhető. Ezek a megfontolások kiemelik egy objektív, klinikai tüneteken alapuló diagnosztika fontosságát, melyek megfelelnek a költséghatékonyság kívánalmainak, mégis kellően magas a diagnosztikai pontosságuk. A HINTS vizsgálat (Head Impulse, Nystagmus, Test of Skew) az AVS differenciáldiagnoszikájában magas pontosságot mutat: neurooftalmológusok által validálva a stroke diagnosztikájában 100%-os szenzitivitást és 96%-os specificitást mutat. A szemmozgásvizsgálatokbban nem jártas sürgősségis orvosok körében ugyanakkor valószínűleg kevésbé kedvezően alakulnak ezek a mutatók. E célból alkották meg a STANDING diagnosztikus algoritmust, mely a nystagmus, a head impulse-teszt, a járásvizsgálat és pozicionális tesztek kiértékelésén alapszik. A tüneteken alapuló vizsgálatok mellett egy stroke rizikóbecslő skála, például az ABCD2 alkalmazása is hasznos lehet bizonyos körülmények között.
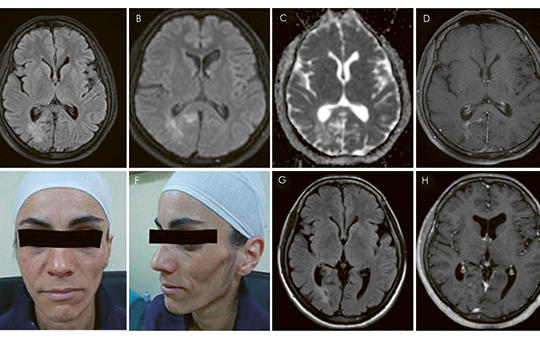
[Relapszáló-remittáló betegségnek tarthatjuk-e a Parry–Romberg-szindrómát?]
[A progresszív hemifacialis atrophia néven is ismert Parry– Romberg-szindróma ritka, lassan progrediáló betegség, amit az arcbőr és az arc bőr alatti kötőszöveteinek egyoldali, fájdalmatlan atrophiája jellemez. A kórkép viszonylag gyakran (az esetek 15–20%-ában) jár együtt neurológiai manifesztációkkal (epilepszia, migrén, trigeminusneuralgia). A lehetséges okok között a következő etiológiai tényezőket tartják számon: fertőzés, az embrionális fejlődés zavara, szimpatikus diszfunkció, autoimmun betegség. Esetismertetésünkben bemutatjuk egy 37 éves nő kórtörténetét, akinek betegsége kétéves periódusban relapszáló-remittáló betegséglefolyásra emlékeztető, dinamikus kontrasztfokozott fehérállomány-elváltozásokkal jelentkezett. Szisztémás gyulladásos aktivitást, gyulladásos jeleket a cerebrospinalis folyadékban, pozitív szérum-autoantitesteket mutattunk ki, ami a beteg korábban felfedezett autoimmun betegségével együtt az autoimmun-gyulladásos kóreredet hipotézisét támogatja.]
Idegtudományok
2021. NOVEMBER 11.
Klinikai döntéshozatal MOG antitest-asszociált betegségben
A szenzitív és specifikus sejtalapú esszék kifejlesztésével a humán myelin-oligodendrocyta glikoprotein (MOG) ellenes IgG-antitestek kimutatása lehetővé tette az anti-MOG antitest-asszociált betegség (anti-MOG antibody-associated disease, MOGAD) és az egyéb demyelinisatiós betegségek elkülönítését. A MOGAD, az aquaporin-4-asszociált neuromyelitis optica spektrum betegség (AQP4-NMOSD) és a sclerosis multiplex (SM) megkülönböztetését a betegségek különböző kórélettani háttere, klinikuma, terápiás és prognosztikus következményei egyaránt indokolják.
NMDAR-encephalitissel átfedő demyelinisatiós szindróma – diagnosztikai és terápiás kérdések
Az anti-N-metil-D-aszpartát-receptor (NMDAR-) encephalitis az NMDAR GluN1 alegysége elleni IgGantitestekkel társuló autoimmun kórkép. A tünetek súlyossága ellenére csak a betegek 35%-ánál mutatható ki koponya-MRI-vel károsodás, ami leggyakrabban monofázisos formában fordul elő. A legfrissebb adatok alapján azonban az anti-NMDAR encephalitisben szenvedők kis százalékánál további relapszusok jelentkezhetnek, melyek hátterében demyelinisatiós laesiók mutathatók ki. A szakirodalomban egyre több adat lelhető fel, miszerint az NMDAR-encephalitis átfedést mutathat más autoimmum, demyelinisatiós kórképpel, leggyakrabban neuromyelitis optica spektrum betegséggel (főként anti- MOG ellenanyag-pozitív estekben), ritkábban sclerosis multiplexszel. A felmerülő diagnosztikai nehézségeket egy eset kapcsán mutatjuk be. A 24 éves férfi pszichiátriai beutalást követően 2 hónapos tünetkezdetet követően először 2014 májusában került felvételre a Neurológiai Klinikára memóriazavar, bal oldali latens hemiparesis kivizsgálása céljából. Akkor készült koponya-MRI-n disszeminált, gócos agyi folyamat ábrázolódott, gyűrűszerű kontrasztanyag-halmozással, kétoldali hippocampus-érintettséggel. A látott kép leginkább ADEM-nek felelt meg. A liquorban oligoklonális gammopathia látszott. A virális és paraneoplasiás eredetet kizártuk. Intravénás szteroidterápiára átmeneti javulás jelentkezett, azonban a terápia leépítését követően ismételt állapotrosszabbodás következett be. A szteroidterápia ismétlése érdemi változást nem hozott, plazmaferézisben részesült, azathioprinterápiát kapott. A diagnosztikai vizsgálatok során az ellenanyag-vizsgálat alapján anti- NMDAR encephalitis diagnózist állítottuk fel. PET CTvel követtük 3 évig. Állapota stagnált, koponya-MRI-n sem jelent meg új laesio, kifejezett jobb oldali hippocampalis atrophia látszott. Imuran elhagyását követően 2 évvel kettős látása jelentkezett, koponya-MRI-vizsgálaton novum fehérállományi laesiók jelentek meg. A látott radiológiai kép és a korábbi liquorlelet, valamint a klinikum alapján felmerült sclerosis multiplex lehető- sége, intravénás nagy dózisú szteroidterápiát alkalmaztunk. Szérum-aquaporin-4, anti-MOG, anti-NMDAR ellenanyag- vizsgálat a szteroidterápiát követően készült, negatív eredményt adott. A szakirodalmat részletesen áttekintve az anti-MOG ellenanyag-pozitív NMO szövődik leggyakrabban az NMDA-R encephalitisszel átfedő demyelinisatiós szindrómával, a sclerosis multiplex ettől jóval ritkább. A közös hatékony terápiás opció a rituximab, aminek támogatását kérvényeztük.
1.
2.
3.
4.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről5.
1.
2.
Klinikai Onkológia
A rosszindulatú daganatok fenotípusának plaszticitása és az immunogén mimikri3.
Klinikai Onkológia
A szarkopénia mérése komputertomográfiával és jelentősége az onkológiai betegeknél4.
5.