Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 351
Újgenerációs e-anatómiaatlaszt fejlesztettek Szegeden
Szeged, 2021. szeptember 24., péntek (MTI) – Oktatásra is alkalmas, interaktív, háromdimenziós, VR-ban is megjeleníthető újgenerációs e-anatómiaatlaszt fejlesztettek a Mozaik Kiadó és a Szegedi Tudományegyetem (SZTE) Anatómiai és Fejlődéstani Intézetének munkatársai uniós támogatással – tájékoztatta a szegedi cég az MTI-t.
Anti-GAD cerebellaris ataxia terápiás nehézségei
Bevezetés: A GAD- (glutamát-dekarboxiláz-) ellenes antitestekkel asszociált cerebellaris ataxia ritka, többnyire lassú progressziót mutató kórkép. Jellemző tünetei a törzs- és végtagataxia, a dysarthria és a nystagmus. Normál liquorfehérje-érték és -sejtszám mellett a betegek egy részében oligoclonalis gammopathia mutatható ki. A koponya-MR-en a betegség fennállásának függvényében látható különösen a vermist érintő cerebellaris atrophia. Igen gyakori társulást mutat szisztémás autoimmun betegségekkel. A kimenetel a betegség kialakulásával (szubakut vs. krónikus) és a cerebellaris atrophia fokával mutat korrelációt. Enyhe fokú vagy hiányzó cerebellaris atrophia esetén a betegek várhatóan jobban reagálnak az immunterápiára. Az MR-en látható atrophia fokából valamelyest becsülhető a cerebellaris rezerv. Esetbemutatás: 35 éves férfi betegünk felvételére közel két éve induló, hosszabb tünetmentes periódusokat is mutató egyensúly-bizonytalanság kifejezett, szubakut rosszabbodása miatt került sor. Az immun cerebellaris ataxia diagnózisa a felvételét megelőző napokban igazolódott. Anamnéziséből vitiligo és Hashimoto-thyreoiditis emelhető ki. A korábbi koponya-MR-vizsgálaton kifejezett kisagyi atrophia ábrázolódott. Plazmaferézist és szteroid-lökésterápiát indítottunk érdemi effektus nélkül. A szteroidterápia folytatása mellett iv. immunglobulint alkalmaztunk, a tünetek jelzett javulását észleltük. Azatioprin beállítását kezdtük el, ezt mellékhatások miatt elhagytuk. Tekintettel a betegség kórlefolyásában észlelt időszakos relapszusokra, rituximab alkalmazása mellett döntöttünk, ami tünetstabilizálódást, enyhe állapotjavulást eredményezett. Megbeszélés: Bár a GAD-asszociált cerebellaris ataxia lassú lefolyást mutató, krónikus betegség, a mihamarabbi diagnózis kulcsfontosságú. A gravis cerebellaris atrophia megelőzése, a cerebellaris rezerv lehetőség szerinti megtartása időben elkezdett, adekvát immunterápiával lehetséges. A diagnózist segíti a képalkotó vizsgálaton látott cerebellaris atrophia, illetve a gyakran társuló autoimmun kórképek ismerete. Összefoglalás: Fiatal, autoimmun társbetegségekben is szenvedő, két éve tünetes, anti-GAD cerebellaris ataxia miatt gondozott férfi betegünk státusza plazmaferézis, bolus szteroid, azatioprin, IVIG mellett érdemi javulást nem mutatott. Rituximab hatására állapota stabilizálódott, enyhe javulást sikerült elérnünk. Radiológiai követését a cerebellaris rezerv megítélése céljából MR-spektroszkópiával tervezzük.
A neuromyelitis optica elektrofiziológiai jellegzetességei
Célkitűzés: A neuromyelitis optica (NMO) a központi idegrendszert érintő autoimmun, demyelinisatiós kórkép. A labor- és a képalkotó diagnosztika fejlődésével egyre több helyen el tudják különíteni a sclerosis multiplexben (SM) és a neuromyelitis opticában szenvedő betegeket. A két kórkép patomechanizmusa és terápiája eltérő. Bemutatjuk, hogy a hozzánk beküldött betegek esetében milyen segítséget nyújtanak az elektrofiziológiai vizsgálatok a két kórkép elkülönítésében és a kórlefolyás követésében. Betegek és módszerek: 2015 és 2021 között klinikánkon 56 beteget vizsgáltunk, életkoruk 24–61 év volt. Az NMO-diagnózis alapja főleg a nyaki gerincvelői és az agytörzsi MRI-felvételeken kimutatott demyelinisatiós góc, illetve a liquorvizsgálat volt. Az elektrofiziológiai vizsgálatokat a nemzetközi standard szerint végeztük, a betegek hozzájárulását és az etikai követelményeket figyelembe véve. Eredmények: A leggyakoribb eltérés a látókérgi kiváltott válaszban az N135 hullámkomponens kifejezett megnyúlása, valamint szabálytalan hullámforma jelentkezése volt, ami mindkét szemet érintette. Súlyos fokú PERG-eltérést az esetek 50%-ában láttunk. Összefoglalás: A szemészeti elektrofiziológiai vizsgálatok (VEP és PERG) eredménye az esetek nagy részében SM és NMO esetén különbözik. A VEP speciális eltérései mellett a laboratóriumunkban rutinszerűen, minden páciensnél elvégzett PERG-vizsgálatok is hozzásegíthetnek a két típusú demyelinisatiós kórkép korai elkülönítéséhez.
NMDAR-encephalitissel átfedő demyelinisatiós szindróma – diagnosztikai és terápiás kérdések
Az anti-N-metil-D-aszpartát-receptor (NMDAR-) encephalitis az NMDAR GluN1 alegysége elleni IgGantitestekkel társuló autoimmun kórkép. A tünetek súlyossága ellenére csak a betegek 35%-ánál mutatható ki koponya-MRI-vel károsodás, ami leggyakrabban monofázisos formában fordul elő. A legfrissebb adatok alapján azonban az anti-NMDAR encephalitisben szenvedők kis százalékánál további relapszusok jelentkezhetnek, melyek hátterében demyelinisatiós laesiók mutathatók ki. A szakirodalomban egyre több adat lelhető fel, miszerint az NMDAR-encephalitis átfedést mutathat más autoimmum, demyelinisatiós kórképpel, leggyakrabban neuromyelitis optica spektrum betegséggel (főként anti- MOG ellenanyag-pozitív estekben), ritkábban sclerosis multiplexszel. A felmerülő diagnosztikai nehézségeket egy eset kapcsán mutatjuk be. A 24 éves férfi pszichiátriai beutalást követően 2 hónapos tünetkezdetet követően először 2014 májusában került felvételre a Neurológiai Klinikára memóriazavar, bal oldali latens hemiparesis kivizsgálása céljából. Akkor készült koponya-MRI-n disszeminált, gócos agyi folyamat ábrázolódott, gyűrűszerű kontrasztanyag-halmozással, kétoldali hippocampus-érintettséggel. A látott kép leginkább ADEM-nek felelt meg. A liquorban oligoklonális gammopathia látszott. A virális és paraneoplasiás eredetet kizártuk. Intravénás szteroidterápiára átmeneti javulás jelentkezett, azonban a terápia leépítését követően ismételt állapotrosszabbodás következett be. A szteroidterápia ismétlése érdemi változást nem hozott, plazmaferézisben részesült, azathioprinterápiát kapott. A diagnosztikai vizsgálatok során az ellenanyag-vizsgálat alapján anti- NMDAR encephalitis diagnózist állítottuk fel. PET CTvel követtük 3 évig. Állapota stagnált, koponya-MRI-n sem jelent meg új laesio, kifejezett jobb oldali hippocampalis atrophia látszott. Imuran elhagyását követően 2 évvel kettős látása jelentkezett, koponya-MRI-vizsgálaton novum fehérállományi laesiók jelentek meg. A látott radiológiai kép és a korábbi liquorlelet, valamint a klinikum alapján felmerült sclerosis multiplex lehető- sége, intravénás nagy dózisú szteroidterápiát alkalmaztunk. Szérum-aquaporin-4, anti-MOG, anti-NMDAR ellenanyag- vizsgálat a szteroidterápiát követően készült, negatív eredményt adott. A szakirodalmat részletesen áttekintve az anti-MOG ellenanyag-pozitív NMO szövődik leggyakrabban az NMDA-R encephalitisszel átfedő demyelinisatiós szindrómával, a sclerosis multiplex ettől jóval ritkább. A közös hatékony terápiás opció a rituximab, aminek támogatását kérvényeztük.
Központi idegrendszeri vasculitis gyanújával vizsgált betegek vizsgálati eredményeinek retrospektív feldolgozása (OMIII, 2016–2021)
Bevezetés: A központi idegrendszeri (KIR) közép- és nagyérvasculitisek az intracranialis és nyaki artériák gyulladásával járó betegségek, melyek az érfal megvastagodása miatt az artériák szűkületét vagy elzáródását okozhatják. Ezen vasculitisek leggyakoribb tünete az agyi infarktus, az átmeneti agyi keringési zavar és a fejfájás. A primer KIR-vasculitis kizárólag az intracranialis ereket érinti, eredete ismeretlen. A szekunder KIR-vasculitisben az intracranialis erek gyulladása szisztémás kórkép (például SLE, HSV-fertőzés) részeként alakul ki. Célkitűzés: Az OMIII (korábban OKITI) Neurológiai Osztályán KIR-vasculitis iránydiagnózissal kezelt betegek vizsgálati eredményeinek feldolgozása a differenciáldiagnosztikai algoritmus pontosítása céljából. Módszerek: Az intézetünkben 2016. január és 2021. július között KIR-vasculitis gyanújával vizsgált 46 beteg vizsgálati eredményeinek statisztikai feldolgozása. Eredmények: Az akut stroke-ellátás során végzett CTA- és DSA-vizsgálat számos esetben felhívja a figyelmet KIR-i vasculitis lehetőségére. A pontos diagnózis felállításában segít a vasculitisprotokollal végzett koponya- MR- és MRA-vizsgálat. A megadott időszakban összesen 46 betegnél készült vasculitisprotokoll szerint MR- és MRA-vizsgálat. Az UH-val kimutatható halo-jel hasznos noninvazív kiegészítője a képalkotó vizsgálatoknak, ugyanakkor hiánya nem zárja ki a vasculitis lehetőségét. Pozitív halo-jel esetén végzett a. temporalis biopszia az esetek nagy részében alátámasztja a diagnózist. Hat betegnél (13%) láttunk egy vagy két oldali pozitív halo-jelet, ezek közül 3 betegnél lett pozitív a temporalis biopszia. Szérum- és liquorszerológiai vizsgálatok (szérum: HIV, HCV, HBV, VZV, HSV, Treponema pallidum, Borellia burgdorferi, liquor: HSV, VZV, Borellia) szükségesek a szekunder vasculitis kizárásához. A radiológiai vizsgálatok, a rutin labor- és a szerológiai vizsgálatok eredménye alapján 17 betegnél (37%) igazoltunk KIR-vasculitist; minden diagnosztizált beteg szteroid- vagy speciális immunterápiában (rituximab, MTX, cyclophosphamid) részesült. Összefoglalás: A központi idegrendszeri vasculitis lehetséges tünetei a stroke és a TIA-események. A betegség diagnosztizálása fontos, mert ezen betegek esetében a szekunder prevenciós módszerek (thrombocytaaggregáció- gátlás, antikoaguláció, lipidcsökkentés) nem elégségesek, a sikeres kezeléshez immunmoduláns terápia szükséges. A központi idegrendszeri vasculitisek diagnózisához körültekintő klinikai szemlélet szükséges, speciális eszközös vizsgálati módszerek és protokollok alkalmazásával.
Terápiás megközelítés és új evidenciák a neuromyelitis optica spektrum kezelésében
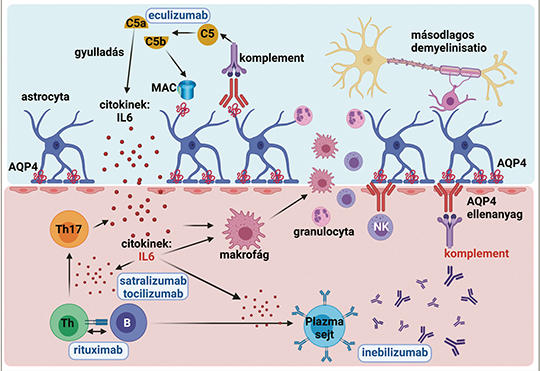
A neuromyelitis optica spektrum betegség (NMOSD) az esetek körülbelül 80%-ában AQP4-ellenanyaggal társul. A szeronegatív betegek körülbelül negyedében a központi idegrendszeri myelin oligodendrocyta glikoprotein (MOG) ellen mutatható ki ellenanyag, és ez a kórkép a MOG-ellenanyag-asszociált betegség (MOGAD) elnevezést kapta. Jelen közlemény áttekinti az off-label azathioprin és mycophenolat mofetil, valamint az evidenciákon alapuló B- és plazmasejt-depletio, az IL-6-jelátvitel és a komplement útvonal antagonizálás klinikai aspektusait NMOSD-ben. Az összefoglaló tárgyalja az NMOSD-terápia terhességi vonatkozásait, és a MOGAD – NMOSD-től eltérő – kezelési megközelítését. Az NMOSD kezelése kapcsán az utóbbi két évben több, III. fázisú klinikai tanulmányon alapuló I. osztályú evidencia jelent meg. A monoklonális ellenanyagokkal végzett vizsgálatok a rituximab (anti-CD20), az inebilizumab (anti-CD19), a tocilizumab (anti-IL6R), a satralizumab (anti-IL6R) és az eculizumab (anti-C5) hatékonyságát és biztonságosságát jelzik egyéb immunterápiákkal kombinálva vagy monoterápiában. A MOGAD kezelését bonyolítja, hogy az esetek körülbelül fele monofázisos, és a MOG ellenanyag a betegség lefolyása során spontán vagy kezelés hatására eltűnhet. A tartós immunszuppresszió igényét MOGAD-ban a relapsusterápiát követő, leépített orális szteroidkezelés után célszerű eldönteni. NMOSD-ben a fenntartó terápia folytatása javasolt terhesség és szoptatás alatt is, és ezt az optimális kezelés kiválasztásánál fertilis nőbetegeknél figyelembe kell venni. Az új evidenciák terápiarezisztens NMOSD-ben is több lehetőséget kínálnak, és a MOGAD kezelési stratégiája is körvonalazódik.
Paradigmaváltás a krónikus szívelégtelenség gyógyszeres terápiájában
A szívelégtelenség incidenciája, prevalenciája folyamatosan növekszik, a betegség morbiditása és a mortalitása továbbra is nagy, így a kórkép jelentősége óriási, megfelelő kezelése kiemelt jelentőségű. A betegség prognózisát javító érdemi evidenciák továbbra is csak csökkent balkamra-funkcióval járó krónikus szívelégtelenség (HFrEF) kezelése esetén állnak rendelkezésre. Az elmúlt évtizedekben számos „mérföldkővizsgálat” született, melyek eredményei a mai napig alapjaiban határozzák meg a betegség terápiáját. A HFrEF bázisterápiája sokáig három alappillérre épült: angiotenzinkonvertáló-enzim- (ACE-) gátló, β-blokkoló és mineralokortikoidreceptor-antagonista, melyek I/A ajánlási szinttel szerepelnek a különböző szívelégtelenség-ajánlásokban. 2014-ben publikálták az áttörő sikert hozó, nagy jelentőségű PARADIGM-HF (heart failure) vizsgálatot, amelyben egy teljesen új gyógyszercsoportot, az angiotenzinreceptor-blokkoló/ neprilysininhibitor (ARNI-) vegyületek csoportjába tartozó sacubitril/valsartant vizsgálták HFrEF-betegeken. A vizsgálat eredménye szerint a sacubitril/valsartan szignifikáns mértékben, 20%-kal csökkentette a cardiovascularis (CV) halálozás és a szívelégtelenség miatti hospitalizáció primer összetett végpontját, valamint 16%-kal csökkentette az összmortalitást egy aktív komparátorhoz, az HFrEF terápiájában a legnagyobb evidenciákkal rendelkező enalaprilhoz képest. Az Európai Kardiológusok Társasága (European Society of Cardiology, ESC) 2016-os szívelégtelenség-irányelve I/B evidenciaszinttel javasolja a sacubitril/ valsartan alkalmazását ACEI helyett a szívelégtelenség miatti hospitalizáció és halálozás csökkentése céljából olyan ambuláns HFrEF-betegek esetén, akik az optimális ACEI, β-blokkoló (BB) és mineralokortikoidreceptor-antagonista (MRA-) kezelés ellenére is panaszosak maradnak. A későbbiekben sacubitril/valsartannal több kisebb vizsgálatot is publikáltak kissé eltérő indikációkkal és más betegcsoportokon. A PIONEER-HF vizsgálat bizonyította, hogy a sacubitril/valsartan terápia korai, az akut szívelégtelenség stabilizációját követően történő megkezdése biztonságos és hatékony HFrEF-betegek esetén, gyorsabban csökkenti a szívelégtelenség prognózisával korreláló NT-proBNP-szintet, mint az enalapril. A TRANSITION és a TITRATION vizsgálat a sacubitril/valsartan terápia kezdetéről, a dózistitrálás módjáról adott hasznos információkat. A sacubitril/ valsartan megjelenése új korszak kezdetét jelentette néhány évvel ezelőtt a HFrEF terápiájában. Ez a korszak Magyarországon most zajlik. Elképzelhető, hogy az SGLT-2-inhibitoroknak köszönhetően egy újabb korszak kapujában állunk, és erre várhatóan választ ad majd az ESC idén megjelenő új szívelégtelenség-ajánlása.
Az Európai Hypertonia Társaság 2021. évi irányelvei a rendelői, illetve rendelőn kívüli vérnyomásmérésről
A hypertonia (magasvérnyomás-betegség) világszerte a legfőbb morbiditásért, valamint mortalitásért felelős módosítható rizikófaktor. A hypertonia diagnózisának, valamint kezelésének alapja a vérnyomás mérése, melyet a további költséges vizsgálatok, valamint hosszútávú terápiás módszerek indikációjának megerősítéséhez vagy kizárásához rutinszerűen alkalmaznak. A nem megfelelő mérési módszer vagy pontatlan vérnyomásmérő használata potenciálisan a kórkép túldiagnosztizáláshoz és szükségtelen kezeléséhez vagy a diagnózis elmaradása esetén megelőzhető kardiovaszkuláris (szív-érrendszeri) betegségek kialakulásához vezethet.
Ellentmondások a neurológiában: A sclerosis multiplex diagnózisának, követésének és terápiájának aktuális kérdései a patomechanizmus megközelítésével
A sclerosis multiplex relapszáló-remittáló és progresszív formái közötti határvonal sokszor nehezen megállapítható. A kórkép különböző klinikai megjelenései (fenotípusai) ellenére nincs egyértelmű biológiai oka az egyes formák elkülönítésének. Mind a primer progresszív, mind pedig a szekunder eseteknél ugyanis hasonló patológiai eltérések észlelhetők a gyulladásos infiltráció, az axonalis károsodás és a corticalis demyelinisatio vonatkozásában. Felmerül a kérdés, hogy a primer progresszív sclerosis multiplexet megelőzheti egy aszimptomatikus (fel nem ismert) relapszáló-remittáló fázis. A szekunder progresszív sclerosis multiplex meghatározásához a betegnek 4-es EDSS-értéke kell, hogy legyen. Következésképpen a klinikai progresszió a korai fázisban kevéssé követett a betegeknél. Ismert továbbá a relapszusoktól függetlenül előrehaladó progresszió, ami észlelhető a betegség relapszáló-remittáló fázisában. A háttérben zajló lappangó, parázsló celluláris/molekuláris folyamatok meghatározzák a klinikai történést, amik a gyógyszeres terápia fontos célpontjai lehetnek. Ugyanakkor a proinflammatorikus citokinek összefüggésbe hozhatók a rosszabbodó kognícióval. Ez a gyulladásos környezet igen komolyan közrejátszhat a relapszus alatt megfigyelt mentális állapot kialakulásában. A betegeknél a motoros (fizikai) rosszabbodást jóval megelőzően rejtett kognitív teljesítménycsökkenés észlelhető. A relapszáló-remittáló fázisban észlelt silent progression pedig kapcsolatban lehet az agyi atrophia előrehaladásával. Levonható tehát az a következetés, hogy a szekunder progresszív fázisban észlelt folyamat jóval előbb elkezdődhet. Ezek az adatok a sclerosis multiplex egységes szemléletét erősítik, és felvetik a lehetőséget, hogy a betegség valójában egy primer progresszív kórkép, amire relapszusok rakódnak.
Idegtudományok
2021. JÚLIUS 14.
S1P-szint és a Parkinson-kór
Schwedhelm és munkatársai a Movement Disorders-ben megjelent cikkükben a szérum S1P-szint és a Parkinson-kórban megjelenő fenotípusok közti összefüggést tanulmányozták. 196, on-fázisban lévő Parkinson-kóros beteg motoros és kognitív tüneteit az UPDRS III, H&Y, valamint a MoCA-skálák szerint értékelték, majd 64 beteg követéses vizsgálatát végezték el. A motoros hanyatlást legalább 5 pontnyi MDS-UPDRS III-skála szerinti csökkenéssel, míg a kognitív hanyatlást legalább 3 pontnyi MoCA-skála szerinti csökkenéssel definiálták. A kezdetben, valamint a követéses időszakban mért szérum-S1P-értékeket a kontrollcsoport megfelelően párosított betegeinek S1P-szintjével hasonlították össze.
1.
2.
3.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről4.
5.
1.
2.
Klinikai Onkológia
A rosszindulatú daganatok fenotípusának plaszticitása és az immunogén mimikri3.
Klinikai Onkológia
A szarkopénia mérése komputertomográfiával és jelentősége az onkológiai betegeknél4.
5.