Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 81
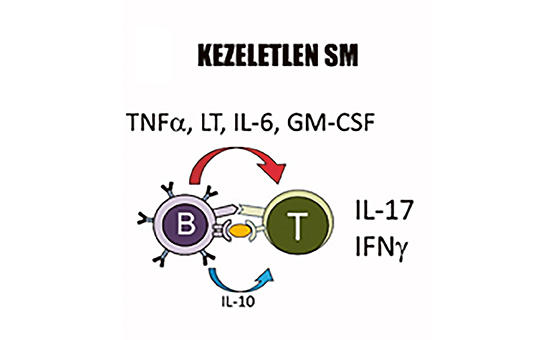
B-sejt-depletio a sclerosis multiplex terápiájában: új szereplő az ofatumumab
Az elmúlt évek kutatási eredményei bizonyították, hogy a B-lymphocyták döntő szerepet játszanak a sclerosis multiplex (SM) patogenezisében. A betegség folyamatának jobb megértése a B-sejteket célzó antitest-terápiák kifejlesztését eredményezte, amelyek potenciális gyógyszerek lehetnek mind a relapszusos, mind a progresszív SM formáiban. A B-sejt-depletiós terápiák ezért mindinkább előtérbe kerülnek, és meghatározóak a betegség progressziójának csökkentésében. Az első B-sejt-depletáló, anti-CD20 monoklonális antitest a rituximab volt, amit sclerosis multiplexben is vizsgáltak, és a kedvező eredményeket követően újabb gyógyszerek kerültek kifejlesztésre, hasonló támadásponttal. 2017-ben az FDA, 2018-ban az EMA is engedélyezte egy másik anti-CD20 monoklonális antitest, az ocrelizumab relapszáló-remittáló sclerosis multiplex (RRSM) és primer progresszív sclerosis multiplex (PPSM) terápiájában történő bevezetését. Ez különösen jelentős előrelépés volt a PPSM kezelésében, hiszen ez volt az első gyógyszer, ami bizonyítottan csökkentette a progressziót PPSM-ben. A B-sejt-depletiós terápia új szereplőjeként nemrégiben lépett színre az ofatumumab, ami egy teljesen humán anti-CD20 monoklonális antitest. A gyógyszer alkalmazását 2021 márciusában az EMA is engedélyezte a sclerosis multiplex relapszáló formáiban (RSM). Összefoglalónkban részletesen bemutatjuk a jelenleg SM-ben alkalmazott anti-CD20 monoklonális antitest-terápiák hatásmechanizmusát és hatékonyságát.
Idegtudományok
2022. ÁPRILIS 29.
Az Epstein–Barr-vírus és a sclerosis multiplex
Régi feltételezés, hogy az Epstein–Barr-vírussal (EBV) történő megfertőződés indítja el a sclerosis multiplexet (SM) eredményező kórfolyamatot. Korábbi vizsgálatok az SM-es betegek 99,5%-ában emelkedett EBV-ellenes antitestszinteket mutattak ki, mely magasabb az egészséges populációban mért 94%-os értékhez képest. Egy mostanában publikált eredmény több mint 10 millió, az USA hadseregében 1993 és 2013 között szolgáló katonákból álló kohorszba tartozó 801 SM-es beteget vizsgált. A 801 beteg közül 35 kezdetben EBV-szeronegatív volt, az SM kezdete előtt közülük 34 beteg szeropozitívvá vált. A 801 SM-es beteg közül mindössze egy beteg volt EBV-szeronegatív az SM kezdetekor, mely meggyőző érv amellett, hogy az EBV valóban képes lehet elindítani az SM-hez vezető folyamatot.
Átmeneti monoocularis látászavar a Covid-19-betegség kezdeti tüneteként sclerosis multiplexben szenvedő, teriflunomiddal kezelt betegnél
A SARS-CoV-2 virus elsődlegesen a legutakat celba vevő virus, ugyanakkor neuroinvaziv kepessegeket is mutat, igy kozponti idegrendszeri tuneteket is okozhat. Noha a Covid-19 altalaban laz, kohoges es altalanos gyengeseg kepeben jelentkezik, kepes neurologiai erintettseg tuneteit, ugymint fejfajast, tudatzavart, ischaemias es verzeses stroke-ot, myelitist, myositist es encephalitist is okozni. Mind klinikai, mind pedig allatkiserletek kimutattak, hogy a koronavirusok kepesek atjutni a ver-agy gaton. Ennek mechanizmusa nem pontosan tisztazott, elsősorban a nervus olfactorius, a virussal fertőzott lymphocytak es monocytak, a microvascularis endothelium es a periferias idegeken keresztuli transzszinaptikus utvonal szerepe merul fel fertőzesi utvonalkent.
Cuprizonnal kiváltott demyelinisatio: Nem minden (auto)immunitás, és nem mindegy, hogy mi van abban, amit megeszünk...
A diétában adott cuprizon (biscyclohexanon-oxaldihydrazon) egy rézkelátor, ami egerekben az oligodendrogliák (OG) mitochondriumainak ismeretlen mechanizmussal történő szeletív károsítását okozza. Ennek következtében OG-apoptózis, következményes, több agyi régióban kialakuló, „plakkszerű” demyelinisatio alakul ki. A tartós cuprizonexpozíció axonkárosodást is okoz. A cuprizon indukálta demyelinisatiós folyamat során nem figyelhetők meg sem aktivált T-, B-lymphocyták, sem vér-agy gát zavar. A celluláris immunrendszert („csupán”) a károsodott myelint eltakarító macrophagok képviselik. A cuprizon kihagyását követően remyelinisatio alakul ki. A cuprizonmodellben látható morfológiai elváltozások hasonlóak a III–IV-es típusú SM-ben leírtakhoz (Lucchinetti, et al. Ann Neurol 2000), illetve a cuprizonmodellben látható morfológiai eltérések számos analógiát mutatnak n = 12, shub után rövid idővel elhunyt SM-beteg agyának neuropatológiai feldolgozása során leírtakkal (Barnett & Prineas. (Ann Neurol 2004). A cuprizon egy környezeti ártalom (tudniillik az állatok tápjába keverjük), ami genetikailag fogékony állatokban, azok „serdülőkorában” (ez egerekben az anyatejes táplálás megszűnésének időszaka) alkalmazva okoz multifokális központi idegrendszeri demyelinisatiót, axonkárosodást. Az SM kialakulásában szerepet játszó környezeti tényezők között a táplálkozást fontos tényezőnek tartják (Altowaijri G, et al. 2017). Érdekes lenne annak tisztázása, hogy a cuprizon intakt molekulaként váltja-e ki toxikus hatásait vagy „prodrug”-ként, azaz metabolizálódik-e és a metabolitjai a toxikusak. Az SM szempontjából is érdekes lehet az említett kérdések tisztázása, mert ez hipotetikusan lehetőséget nyitna „cuprizonszerű” vagy „cuprizonmetabolit(ok)-szerű” anyagok felkutatására. Ezen felvetéstől függetlenül is indokolható kutatási program lehetne a potenciálisan mitochondriumfunkciót károsító adalékok (például színezők, ízfokozók, tartósítók stb.) felkutatása az ipari méretekben előállított élelmiszerekben.
Klinikum
2021. JÚNIUS 09.
A vérplazma összetevői, azok élettani szerepe, és gyógyászati felhasználása
A vér folyékony kötőszövetünk komplex bonyolult és összetett funkcióval. Alkotórészei a sejtes elemek (vörösvérsejtek, fehérvérsejtek, vérlemezkék), és az in vivo működésükhöz szükséges közeg a vér 55%-át kitevő plazma. Ebben a sejtek szabadon áramlanak, lehetővé teszi, hogy azok minden szervhez eljuthassanak az érpályán keresztül és kifejthessék élettani hatásukat.
Tüdőrák harminc év távlatából. Gondolatok a küzdelmes múltról, a jelen eredményeiről és az ígéretes jövőről
Az elmúlt 30 évben a tüdőrák komplex kezelésében óriási fejlődés történt. Ez a fejlődés főként az utóbbi évtizedhez köthető. A tüdőrák kezelésével kapcsolatos nihilizmus már a múlté, realitássá vált az is, hogy az előrehaladott stádiumú betegek is megfelelő kezeléssel gyógyíthatóvá válhatnak, illetve betegségük folyamatos aktív daganatellenes terápia mellett krónikussá szelídíthető. Az előrehaladott stádiumban lévők harminc évvel ezelőtt elérhető 6-8 hónapos várható túlélési mutatói manapság már jelentősen növekedtek, bizonyos esetekben akár az 5 évet is meghaladhatják. Ehhez szükséges a megfelelő diagnosztikus háttér, amely lehetővé teszi a biomarkeralapú kezeléseket. Korai stádiumban alapvető a reszekciós tüdőműtét, beillesztve a komplex terápiás lehetőségeket neoadjuváns és adjuváns formában, illetőleg az új műtéti technikák is hozzájárulnak a terápiás eredmények javulásához. Elmondható ugyanez a sugárterápia vonatkozásában is. A gyógyszeres terápiás lehetőségek tekintetében is a komplex terápiás stratégia érvényesül, melyben alapvető szerepet játszanak a citotoxikus kemoterápiás, célzott kezelési és immunterápiás modalitások. A tüdőrák kezelési stratégiájának felállításában döntő szerepe van a tüdőrák-specifikus onkoteamek működésének. A jövő útját az újabb és újabb célzott terápiás lehetőségek megjelenése, az immunterápiás indikációk bővülése jelezheti a precíziós medicina alkalmazásával. Nem szabad azonban elfeledkeznünk a primer és szekunder prevencióról sem, mely a dohányzás elleni hatékony küzdelmet, illetőleg most már az evidenciává vált rizikócsoportos alacsony dózisú mellkasi CT-szűrés alkalmazását jelenti.
Pszichózis mint az antibiotikumok mellékhatása
Direkt kapcsolat van az antibiotikum-expozíció és az akut pszichózis között, állapította meg a Brain, Behavior, & Immunity – Health című szaklap tanulmánya. Az egyesült államokbeli kutatók cikke az első olyan tanulmány, ami az egyes antibiotikumok pszichiátriai mellékhatásainak (insomnia, hallucináció, delúzió, delírium, katatónia, paranoia, érzelmi elszíntelenedés, pszichózis) gyakoriságát értékeli.
A humán immunrendszer rendszerelvű megközelítése
A nukleotidpolimorfizmusok kutatása révén kiderült, hogy az autoimmun betegségek kialakulásában nagyon kis hatáserősséggel nagyon sok genetikai lokusz közreműködik, és itt is kiderült, hogy egy-egy kórkép molekuláris heterogenitása – pl. SLE esetén – milyen óriási. E betegségek kezelését forradalmasította a biologikumok rendszerimmunológiának köszönhető bevezetése.
Táplálkozási ajánlások a CoVID-19 miatti karantén idején
A karanténhoz társuló stressz alvászavarokat is okozhat, ami tovább fokozhatja a stresszt és ezáltal a táplálékbevitelt, ami egy ördögi kör kialakulásához vezethet. Fontos, hogy vacsorára olyan ételeket fogyasszunk, amelyek szerotonint vagy melatonint tartalmaznak vagy elősegítik ezeknek a szintézisét.
A kemoterápia daganatkeltő hatása
Kemoterápia nélkül a felfedezett daganatos betegségek ötéves túlélési rátája – daganatfüggően – 0–15% között lenne, a jelenlegi terápia alkalmazásával 17-85%. Ugyanakkor számos figyelmeztetés hívja fel a figyelmet a kemoterápia által indukált nemkívánatos mellékhatások, legfőképpen a lehetséges tumorindukciós képesség veszélyeire, ami az öt éven túl gyógyult betegek 5-10%-át is érintheti. A szisztémás kemoterápiában használt egyes gyógyszerek (alkilálószerek, etopozid, arzén-trioxid) képesek a szervezet egészséges sejtjeiben mutációt okozni, amivel megnő a valószínűsége annak, hogy a mutációt szenvedett sejtek egy későbbi (szekunder) daganatképződést indítsanak el. A mutagén hatások mellett egyes kemoterapeutikumok a szervezet normális myeloid és epithelialis sejtjeire fejtenek ki olyan hatásokat, amelyek a szöveti mikrokörnyezet átalakításával megteremtik a malignus transzformáció lehetőségét. Ebben a folyamatban igen fontos szereplők a tumorokkal asszociáló makrofágok (TAM), amelyek a daganatsejt által szekretált faktorok és mikroszómák hatására megváltoztathatják génexpressziós mintázatukat, és prokarcinogén szignálokkal segítik a tumorsejtek megmaradását, invazivitását, csökkentik a citotoxikus T-sejtek aktivitását. Mindezen okok miatt kiemelten fontos az, hogy a daganatkeltő mutagénekkel dolgozó orvosok, gyógyszerészek, technikusok és nővérek ne kerüljenek közvetlen érintkezésbe ezekkel a veszélyes anyagokkal, hanem használjanak megfelelő védőfelszerelést.
1.
2.
3.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről4.
5.
1.
2.
Klinikai Onkológia
A rosszindulatú daganatok fenotípusának plaszticitása és az immunogén mimikri3.
Klinikai Onkológia
A szarkopénia mérése komputertomográfiával és jelentősége az onkológiai betegeknél4.
5.