Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 129
Hírek a világból
2022. március 11-én az Egyesült Államok Élelmiszer- és Gyógyszerügyi Hatósága (FDA) jóváhagyta az olaparib (Lynparza) -kezelést BRCA-mutált, HER-2-negatív, magas kockázatú korai emlőrákos betegek adjuváns kezelésére, akik neoadjuváns vagy adjuváns kemoterápiában részesültek. A betegeket az olaparib FDA által jóváhagyott diagnosztikája alapján kell kiválasztani a terápiára, és március 11-én a Myriad BRACAnalysis CDx tesztjét is jóváhagyták ilyen felhasználásra.
Gondolatok a gyomorrákos betegek nem sebészi kezeléséről
A gyomorrákos betegek oki és tüneti kezelése az oncoteam javaslatán alapuló, interdiszciplináris feladat, amelynek során a beteg állapotára kiemelt figyelmet kell fordítani. Hazánkban a perioperatív (neoadjuváns és adjuváns) kemoterápia, még inkább a radiokemoterápia várható előnyeikhez képest kevésbé elterjedt módszerek. Az áttétes betegség kezelésében legjobb eredmény az első vonalban várható, HER2-pozitív esetben trasztuzumab, HER2-negatív (és PD-L1 pozitív) daganatban a nivolumab és pembrolizumab citosztatikus kezeléshez adásával. A kemoterápia szerei a ciszplatin, kapecitabin, az indikáción túli oxaplatin és a fluoropirimidinek, valamint taxánok különböző kombinációi. Másodvonalban a ramucirumab, harmadvonalban a trifluridin-tipiracil jelentenek újabb lehetőséget. A szerzők hangsúlyozzák a molekuláris célpontalapú terápia, az ezt biztosító (racionális indikációval végzett) új generációs szekvenálás fontosságát, s kitérnek a tumoragnosztikus kezelésre is. Speciális klinikai helyzetek (tumoros vérzés, peritonealis áttétek, idősek, rossz általános állapotúak) ellátására is adnak javaslatot. Hangsúlyozzák, hogy a gondos tüneti terápiát nemcsak terminálisan, hanem a diagnózis felállításától kell szorgalmazni, s hangsúlyozzák, hogy a szomatikus tünetek ellátása mellett a pszichés és szociális tényezők figyelembevétele is szükséges, valamint a beteggel, családdal történő, megfelelő kommunikáció a későbbiekben a különbözőképpen jelentkező elégedetlenség megelőzését is szolgálja.
Sugárterápia indukálta másodlagos daganatok
Az onkológiai kezelések szerves részét képezi a sugárterápia, amiben a betegek közel fele részesül. A modern onkológiai kezeléseknek köszönhetően a túlélés egyre hosszabb, így a betegek körülbelül egyötöde megéli azt is, hogy egy második tumor kialakuljon. Több tanulmány szerint maga az onkológiai kezelés is összefüggésbe hozható a másodlagos primer tumor kialakulásával, ami egyes becslések szerint az esetek 5-8%-ában lehet a sugárterápia következménye. Nagy kihívást jelent, hogy megértsük a sugárterápia okozta hatásokat az esetlegesen túlélő daganatsejtekben, a daganatot körülölelő egészséges szövetekben, az alacsony dózisban részesült területekben, illetve az egyáltalán nem irradiált szövetekben, ahol abszkopális hatások érvényesülhetnek. Ezek együttes hatása tehető felelőssé az úgynevezett radiokarcinogenezis kialakulásáért. Manapság számos tanulmány foglalkozik a sugárterápia daganatindukáló hatásaival. Ez az összefoglaló arra hivatott, hogy áttekintse a témával kapcsolatos ismereteinket a patogenezis, radiogenomikai, sugárfizikai és sugárbiológiai szempontok alapján, továbbá tárgyalja a megelőzés és a szűrés lehetőségeit. A sugárterápia kétélű fegyver, amely egyrészt nagyon jól alkalmazható a daganatos betegségek kuratív kezelésében, másrészt azonban potencionálisan másodlagos daganatot indukálhat, amely évekkel később jelentkezik. Emiatt a jövőben a maximálisan optimalizált, személyre szabott sugárterápiának lehet csak létjogosultsága.
Hírvilág
2021. ÁPRILIS 08.
Nemzeti Rákellenes Nap – Covid idején se álljunk meg!
Április 10-én immár 29. alkalommal tartják meg a Nemzeti Rákellenes Napot. A szervező Magyar Rákellenes Liga ismét emlékeztet arra, hogy a daganatos betegségek megelőzése jórészt a saját kezünkben van, és számos programot is kínál ehhez. Mindemellett arra is felhívják a figyelmet, hogy a legfrissebb nemzetközi adatok szerint a 2020-as lezárások alatt 40%-kal csökkent a diagnosztizált rákos esetek száma!
A méh rosszindulatú daganatainak korszerű onkológiai kezelése
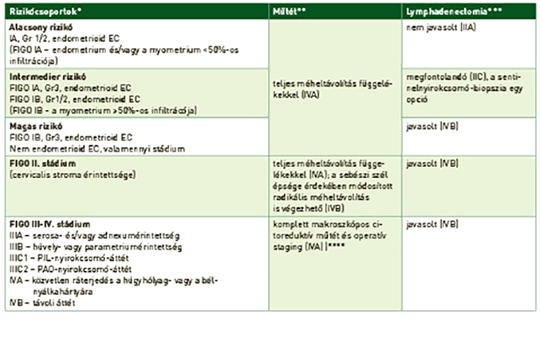
Világviszonylatban évente közel 400 000 nőnél igazolódik méhtestrák, amely 2018-ban körülbelül 90 000 nő halálát okozta. Az esetek túlnyomó részét a méhnyálkahártya hormonérzékeny hámjából kiinduló endometriumcarcinomák (EC) alkotják. A sarcomák a méhtestrákok alig 3%-át adják. Az EC-k 80-85%-a jó prognózisú, mivel alacsony gradusú és korai stádiumban kerül felismerésre, amikor a műtét és az esetleges posztoperatív kezelés révén a gyógyulás reális terápiás cél. Az előrehaladott stádiumban diagnosztizált EC és a nem endometrioid altípusok esetén a prognózis lényegesen rosszabb. A magas rizikójú EC optimális adjuváns kezelésére irányuló vizsgálatok egy része még folyamatban van, illetve a bővülő molekuláris ismeretek újabb vizsgálatokat generálnak. A méhtestsarcomák esetében is a sebészi eltávolítás jelenthet kuratív megoldást, az adjuváns kezelésre vonatkozó evidenciák bizonytalanok, egyéni mérlegelést igényelnek. A modern onkoterápia érájában már nemcsak a betegségmentes élet meghosszabbítására, hanem az élet minőségének minél teljesebb megőrzésére is törekszünk. A nőgyógyászati onkológiában ezt jelenti a fertilitás vagy a funkcionáló ováriumok lehetőség szerinti megőrzése; a magas morbiditással járó szisztémás lymphadenectomia indikációs körének szűkítése; a kedvezőbb mellékhatásprofilú brachytherapia alkalmazása a teljes kismedencei besugárzás helyett. A modern onkoterápia az úgynevezett biológiai kezelések által az előrehaladott betegségek ellátásának is a részévé vált: kemoterápia mellett/után progrediáló esetekben a pembrolizumab az EC és a sarcomák esetén is alkalmazható mikroszatellita-instabilitás vagy magas tumormutációs terheltség esetén, míg az NTRK fúziós gén jelenlétében larotrectinib vagy entrectinib mint célzott tirozinkináz-gátlók javasolhatók. Az EC-k 70-80%-át kitevő mikroszatellita-stabil esetekben (nem endometrioid altípusokban is!) a pembrolizumab lenvatinibbel kombinációban adható a kemoterápia után. Az EC területén gyarapodnak továbbá az egyéb célzott terápiás szerekkel szerzett tapasztalatok is (anti-HER2 serosus carcinomában, mTOR-gátló kezelés, endokrin terápia, más immun checkpoint inhibitorok, tirozinkináz-gátlók, PARP-gátlók és kombinációs kezelések). A jelen munka a méhtestrákok onkoterápiájáról kíván rövid összefoglalást nyújtani az aktuális szakmai ajánlások és a folyamatban lévő vizsgálatok bemutatásával.
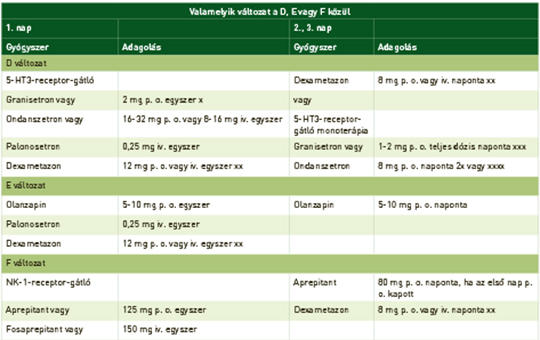
Hányáscsillapítás az onkológiai kezelések során
A hányinger és hányás egy többlépcsős folyamat, amely a központi idegrendszer irányítása alatt áll. A hányást kiváltó ingerek pszichés hatásra az agykéreg felől érkezhetnek vagy a nervus vaguson keresztül. A nyúltvelőben speciális magvak találhatók, amelyek a hányást kiváltják. Legfontosabb ingerületátvivő anyagok a szerotonin, a P-anyag és a dopaminok. A kemoterápiás szerek különböző arányban okoznak hányingert és hányást. Az 5-HT3- és NK-1-receptor-antagonisták a legjelentősebb hányinger-csillapítók. Szakmai ajánlások javasolják a gyógyszer-kombinációkat a különböző kemoterápiák okozta hányás csillapítására. A fix, szájon keresztül alkalmazható kombináció: netupitant és palonosetron (NEPA) növeli a betegek terápiahűségét. Az összefoglaló kitér a speciális hányingerek és hányások ismertetésére: áttöréses, többnapos kemoterápia okozta, sugárterápia során kialakult és a megelőlegezett hányásokra, valamint a gyermekkori hányáscsillapítás problematikájára is.
Tüdőrák harminc év távlatából. Gondolatok a küzdelmes múltról, a jelen eredményeiről és az ígéretes jövőről
Az elmúlt 30 évben a tüdőrák komplex kezelésében óriási fejlődés történt. Ez a fejlődés főként az utóbbi évtizedhez köthető. A tüdőrák kezelésével kapcsolatos nihilizmus már a múlté, realitássá vált az is, hogy az előrehaladott stádiumú betegek is megfelelő kezeléssel gyógyíthatóvá válhatnak, illetve betegségük folyamatos aktív daganatellenes terápia mellett krónikussá szelídíthető. Az előrehaladott stádiumban lévők harminc évvel ezelőtt elérhető 6-8 hónapos várható túlélési mutatói manapság már jelentősen növekedtek, bizonyos esetekben akár az 5 évet is meghaladhatják. Ehhez szükséges a megfelelő diagnosztikus háttér, amely lehetővé teszi a biomarkeralapú kezeléseket. Korai stádiumban alapvető a reszekciós tüdőműtét, beillesztve a komplex terápiás lehetőségeket neoadjuváns és adjuváns formában, illetőleg az új műtéti technikák is hozzájárulnak a terápiás eredmények javulásához. Elmondható ugyanez a sugárterápia vonatkozásában is. A gyógyszeres terápiás lehetőségek tekintetében is a komplex terápiás stratégia érvényesül, melyben alapvető szerepet játszanak a citotoxikus kemoterápiás, célzott kezelési és immunterápiás modalitások. A tüdőrák kezelési stratégiájának felállításában döntő szerepe van a tüdőrák-specifikus onkoteamek működésének. A jövő útját az újabb és újabb célzott terápiás lehetőségek megjelenése, az immunterápiás indikációk bővülése jelezheti a precíziós medicina alkalmazásával. Nem szabad azonban elfeledkeznünk a primer és szekunder prevencióról sem, mely a dohányzás elleni hatékony küzdelmet, illetőleg most már az evidenciává vált rizikócsoportos alacsony dózisú mellkasi CT-szűrés alkalmazását jelenti.
Az emlőrák hormonkezelése
A fejlett országokban a nők 12%-ának lesz emlőrákja az élete folyamán. Ez az áttekintés az emlőrák szisztémás endokrin kezelésének jelenlegi lehetőségeivel foglalkozik. Az emlőrákokat három nagy alcsoportba lehet osztani a szövettani vizsgálat során értékelt három marker (ER, PR, HER2-receptorok) jelenléte és hiánya alapján. A nem áttétes betegeknél a kezelés célja a lokoregionális és a távoli kiújulás megelőzése. Az adjuváns hormonterápia alkalmazásának időtartama fontos kérdés a mindennapi onkológiai gyakorlatban. Áttétes betegeknél a terápia célja az élet meghosszabbítása, az életminőség megőrzése és a daganatos betegséggel kapcsolatos tünetek palliálása. A HR+ emlőrákos betegek monoterápiában és kombinált kezelések részeként is kaphatnak endokrin ellátást. Az új terápiás megközelítések és a nemzetközi gyógyszerfejlesztési erőfeszítések eredményeként egyre több terápiás lehetőség áll rendelkezésre mind a korai emlőrákos betegek, mind az áttétes betegek számára.
Húgyhólyagdaganat neoadjuváns és palliatív gyógyszeres ellátása
Az izominvazív, lokális hólyagtumoros betegek túlélése kedvezőbb, ha a cystectomiát neoadjuváns vagy adjuváns platinatartalmú kemoterápia egészíti ki. A neoadjuváns ciszplatinbázisú kemoterápia hatására, metaanalízisek alapján, 5-16%-os ötéves túlélési benefit érhető el. A neoadjuváns kemoterápiára jól reagáló betegeknél (patológiai komplett remisszió aránya 12-50%) még kedvezőbb a kimenetel. A cystectomia három hónapon túli késlekedésének nincs kedvezőtlen hatása a túlélésre, ha a műtét előtt kemoterápia történik. Az adjuváns fázis III vizsgálatok és metaanalízisek eredményei kevésbé egyértelműek, de összességükben kedvező trend észlelhető a kemoterápia hatására a túlélésben, különösen pT 3/4 és/ vagy N+ (valamint high grade vagy margin pozitív) esetekben. A platinabázisú kemoterápiás kezelés utáni progresszió esetén másod- és többed-, valamint ciszplatinra alkalmatlan betegeknél PD-L1-expresszió esetén első vonalban is alkalmazható immunterápia hatására a betegek túlélésének és a tumorválasz időtartamának eredményei igen biztatóak, hatékonyabbnak látszanak az adott stádiumokban eddig alkalmazott kemoterápiás szerek publikált adatainál. A legújabb irányokban az immunterápia neoadjuváns, adjuváns, valamint kemoterápiával kombinált alkalmazása is klinikai vizsgálatok értékelése alatt áll, amelyek korai adatai kiemelkedően perspektivikusnak tűnnek.
Petefészekrákban szenvedő betegek nem sebészi kezelése
A petefészekrákban szenvedő betegek kezelésében alapvető a kellően radikális műtét, amely az egyéb módszerek eredményességét is meghatározza. Az ezt követően, egy ülésben végzett hyperthermiás intraperitonealis kemoterápia 40,5–42,5 Celsius-fokos citosztatikus oldat perfúziójával történik. A szisztémás kezelések megválasztásában a hat hónapos progressziómentesség a mérföldkő, ezentúl platinaszenzitív, ezen belül -refrakter vagy -rezisztens betegségről van szó. A citosztatikus kezelés fejlődése az alkilálószerektől a platinaszármazékokon át a paklitaxel alkalmazásáig terjed, különféle kombinációkkal, egyre jobb eredményekkel és mind kevesebb mellékhatással. A célzott terápiában az érújdonképződés-gátlók (főleg a bevacizumab) és a DNS-hibák javítását megakadályozó, PARP-gátlók a legjelentősebbek; ez utóbbiak esetében általában a platinaérzékenység feltétel, míg a BRCA-mutáció már nem mindig követelmény. Az utóbbi időben az immunterápiával kapcsolatban is ígéretes vizsgálatok folynak. A hormonkezelés fő előnye a jó tolerálhatóság. A gyógyszerek alkalmazásának sikerei mellett visszaszorulni látszik a sugárterápia, pedig a teljes peritonealis felszín ellátása – különösen a korszerű besugárzási technikák alkalmazása mellett – a kemoterápia alternatívája lehet, a palliatív irradiáció pedig a tünetek csökkentése mellett a gyógyszermentes időszakot is megnyújthatja, s a kombinálás lehetőségei további távlatokat nyitnak meg.
1.
2.
3.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről4.
5.
1.
2.
Klinikai Onkológia
A rosszindulatú daganatok fenotípusának plaszticitása és az immunogén mimikri3.
Klinikai Onkológia
A szarkopénia mérése komputertomográfiával és jelentősége az onkológiai betegeknél4.
5.