Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 322
Agnosztikus terápia onkológiai alkalmazása
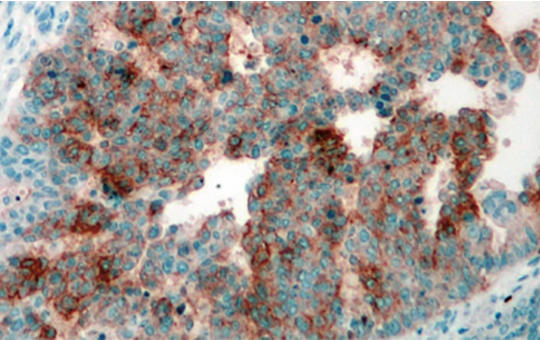
A tumoragnosztikus terápia az onkológiai kezelés ígéretes lehetősége, azonban a potenciális célpontok klasszifikálása, validálása, azok egységes módszerek szerinti kimutatása elengedhetetlen. A tumoragnosztikus kezelések engedélyezése új típusú, biomarker-vezérelt klinikai vizsgálatok bevezetését tette szükségessé. Jelenleg három tumoragnosztikus molekuláris célpont ismert: a daganatok magas fokú mikroszatellita-instabilitása (MSI-H), a neurotrop-tirozinkináz-receptor (NTKR) gének fúziója, valamint a daganatok magas tumormutációs terhelése (TMB-H). A pembrolizumab (anti-PD-1 antitest) az első tumoragnosztikus indikációban is törzskönyvezett gyógyszer, amelyet először MSI-H daganatok kezelésére engedélyeztek, majd később a magas TMB is bekerült az indikációk közé. Az NTKR-fúziót hordozó daganatok kezelésére a larotrectinib és az entrectinib került engedélyezésre.
Hányáscsillapítás az onkológiai kezelések során
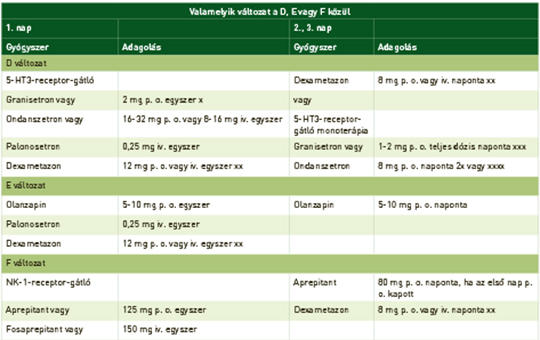
A hányinger és hányás egy többlépcsős folyamat, amely a központi idegrendszer irányítása alatt áll. A hányást kiváltó ingerek pszichés hatásra az agykéreg felől érkezhetnek vagy a nervus vaguson keresztül. A nyúltvelőben speciális magvak találhatók, amelyek a hányást kiváltják. Legfontosabb ingerületátvivő anyagok a szerotonin, a P-anyag és a dopaminok. A kemoterápiás szerek különböző arányban okoznak hányingert és hányást. Az 5-HT3- és NK-1-receptor-antagonisták a legjelentősebb hányinger-csillapítók. Szakmai ajánlások javasolják a gyógyszer-kombinációkat a különböző kemoterápiák okozta hányás csillapítására. A fix, szájon keresztül alkalmazható kombináció: netupitant és palonosetron (NEPA) növeli a betegek terápiahűségét. Az összefoglaló kitér a speciális hányingerek és hányások ismertetésére: áttöréses, többnapos kemoterápia okozta, sugárterápia során kialakult és a megelőlegezett hányásokra, valamint a gyermekkori hányáscsillapítás problematikájára is.
A méh rosszindulatú daganatainak korszerű onkológiai kezelése
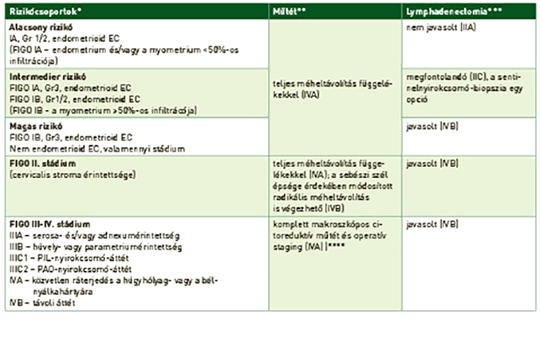
Világviszonylatban évente közel 400 000 nőnél igazolódik méhtestrák, amely 2018-ban körülbelül 90 000 nő halálát okozta. Az esetek túlnyomó részét a méhnyálkahártya hormonérzékeny hámjából kiinduló endometriumcarcinomák (EC) alkotják. A sarcomák a méhtestrákok alig 3%-át adják. Az EC-k 80-85%-a jó prognózisú, mivel alacsony gradusú és korai stádiumban kerül felismerésre, amikor a műtét és az esetleges posztoperatív kezelés révén a gyógyulás reális terápiás cél. Az előrehaladott stádiumban diagnosztizált EC és a nem endometrioid altípusok esetén a prognózis lényegesen rosszabb. A magas rizikójú EC optimális adjuváns kezelésére irányuló vizsgálatok egy része még folyamatban van, illetve a bővülő molekuláris ismeretek újabb vizsgálatokat generálnak. A méhtestsarcomák esetében is a sebészi eltávolítás jelenthet kuratív megoldást, az adjuváns kezelésre vonatkozó evidenciák bizonytalanok, egyéni mérlegelést igényelnek. A modern onkoterápia érájában már nemcsak a betegségmentes élet meghosszabbítására, hanem az élet minőségének minél teljesebb megőrzésére is törekszünk. A nőgyógyászati onkológiában ezt jelenti a fertilitás vagy a funkcionáló ováriumok lehetőség szerinti megőrzése; a magas morbiditással járó szisztémás lymphadenectomia indikációs körének szűkítése; a kedvezőbb mellékhatásprofilú brachytherapia alkalmazása a teljes kismedencei besugárzás helyett. A modern onkoterápia az úgynevezett biológiai kezelések által az előrehaladott betegségek ellátásának is a részévé vált: kemoterápia mellett/után progrediáló esetekben a pembrolizumab az EC és a sarcomák esetén is alkalmazható mikroszatellita-instabilitás vagy magas tumormutációs terheltség esetén, míg az NTRK fúziós gén jelenlétében larotrectinib vagy entrectinib mint célzott tirozinkináz-gátlók javasolhatók. Az EC-k 70-80%-át kitevő mikroszatellita-stabil esetekben (nem endometrioid altípusokban is!) a pembrolizumab lenvatinibbel kombinációban adható a kemoterápia után. Az EC területén gyarapodnak továbbá az egyéb célzott terápiás szerekkel szerzett tapasztalatok is (anti-HER2 serosus carcinomában, mTOR-gátló kezelés, endokrin terápia, más immun checkpoint inhibitorok, tirozinkináz-gátlók, PARP-gátlók és kombinációs kezelések). A jelen munka a méhtestrákok onkoterápiájáról kíván rövid összefoglalást nyújtani az aktuális szakmai ajánlások és a folyamatban lévő vizsgálatok bemutatásával.
Az onkológiai gyógyszerész táguló szerepköre
A technológiai haladás felszabadította a gyógyszerészeket, akiknek ma már nem kell a gyógyszerkiadás biztonsági ellenőrzésére fókuszálniuk, és egyre több betegágy melletti feladatot is vállalhatnak, részt vehetnek akár az őssejttranszplantáció kivitelezésében vagy a farmakogenomikai eredmények értelmezésében is.
Génmódosított immunsejtek: új fegyverek nem csak daganatok ellen
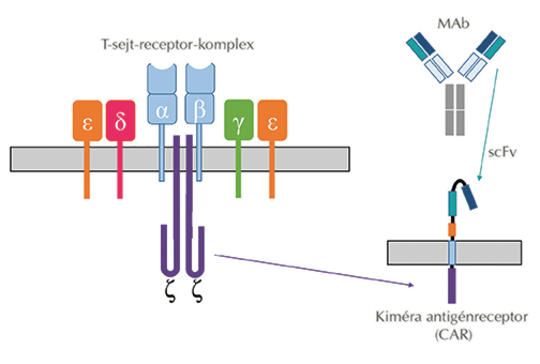
Az elmúlt évtized onkológiai áttörése minden bizonnyal a CD19-specifikus CAR T-sejtek alkalmazása volt a különböző hematológiai kórképek kezelésében. A klinikai vizsgálatokban szerzett tapasztalatok, párosulva a magánszektor és gyógyszeripar befektetéseivel, a meglévő CAR T-sejt-készítmények kereskedelmi forgalmazásával, sok kutató figyelmét irányította rá az új típusú immunsejtekben rejlő lehetőségekre, és azok nem onkológiai célú felhasználására. A közlemény célkitűzése, hogy röviden bemutassa azokat a preklinikai alkalmazásokat, ahol a CAR T-sejteket sikerrel próbálták ki autoimmun és infektológiai kórképekben.
Hírvilág
2020. OKTÓBER 04.
Szeptember 15-e a Limfóma Világnapja
Minden év szeptember 15-e a Limfóma Világnapja. Ennek alkalmából a Magyar Rákellenes Liga ismét biciklis felvonulással kívánja felhívni a figyelmet a betegségre, annak tüneteire és a korai diagnosztizálásra.
Az inváziós spektrum prognosztikai jelentősége glioblastomában
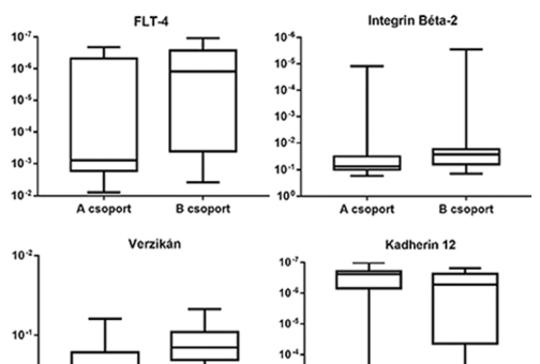
A glioblastoma a leggyakoribb központi idegrendszeri rosszindulatú daganat; sebészi kezelése a daganatok invazív jellegénél fogva nem lehetséges, onkoterápiája pedig csupán szerény eredményeket hoz – a betegek átlagos teljes túlélése (OS) 16–24 hónap. A betegek egy része alig reagál az alkalmazott kezelésre; a klinikumban jelenleg nincs olyan prognosztikai vagy prediktív marker, ami segítené a betegek túlélésében tapasztalható jelentős szórás érdemi feltérképezését és a kezelési algoritmus optimalizálását. Jelen kutatásban az invázióban szerepet játszó extracelluláris mátrix (ECM-) molekulák expressziójának prognosztikai jelentőségét kívántuk meghatározni. Eltérő prognózisú betegcsoportokat létrehozva (A csoport OS < 16 hónap, B csoport OS > 16 hónap) vizsgáltuk meg glioblastomás betegek gyorsfagyasztott tumormintáiban a szakirodalom által jelenleg elismert markerek (IDH1 mutációs és MGMT metilációs státusz) jelenlétét, továbbá 46 inváziós ECM-molekula mRNS-szintjét. A DE KK Idegsebészeti Klinikán operált és az Onkológiai Klinikán utókezelt betegek klinikai adatai nem mutattak jelentős különbségeket a túlélési adatokat (progressziómentes és teljes túlélés) és a reoperációs arányt leszámítva. Minden minta IDH vad típusú volt. Jelentős különbség volt a jobb és a rosszabb túlélésű betegek között az MGMT promoter hipermetiláció arányában (28,6% vs. 68,8%). Az inváziós ECM-molekulák expressziós mintázata, az inváziós spektrum szintén jelentős különbséget mutatott; szignifikáns különbség mutatkozott az integrin β2, kadherin-12, FLT4/VEGFR-3, verzikán molekulák expressziójában. Az inváziós spektrum megbízhatóságát statisztikai osztályozóval tesztelve a módszer a minták 83,3%-át sorolta a megfelelő prognosztikai csoportba (PPÉ: 0,93). A különböző túlélésű betegcsoportok összehasonlítása során a reoperációs arányban megfigyelhető különbség az irodalmi adatokkal összevágó tény. Az MGMT promoter metiláltságának vizsgálata hazai újdonság, az eredmény az eddigi ismereteket megerősítve sürgeti a vizsgálat rutinszerű bevezetését. Az inváziós spektrum vizsgálata többletinformációt ad a tumorról, prognosztikai markerként segíthet felismerni az agresszívabb tumorokat, továbbá felhívja a figyelmet az antiinvazív ágensek jövőbeni használatának szükségességére a GBM terápiájában.
A fej-nyaki daganatok komplex kezelése – áttekintés
A fej-nyaki laphámsejtes daganatok (head and neck squamous cell carcinoma – HNSCC) kezelése rendkívül komplex feladat, amely megkívánja a fej-nyak sebész, sugárterápiás szakember és klinikai onkológus szoros együttműködését. Elsődleges célnak a jó tumorkontrollt kell tekintenünk, de a terápia megválasztásánál szem előtt kell tartanunk az onkológiai radikalitás mellett az elfogadható életminőséget, ismervén, hogy a legtöbb lokális terápia nagyban befolyásolja a betegek légzés-, nyelés- és/vagy beszédfunkcióját. A megfelelő diagnosztikus vizsgálatok alapján a betegséget besorolhatjuk korai stádiumba, lokálisan/regionálisan előrehaladott stádiumba, illetve távoli áttétes és/vagy kiújult stádiumba. Kategóriánként eltérő terápiás modalitások jönnek szóba, amelyeket tovább bonyolít a primer tumor, az áttétek elhelyezkedése, a beteg állapota, társbetegségei, a daganat biológiai viselkedése. Jelen áttekintő közleményben a szerzők összefoglalják a fej-nyaki laphámrákok terápiájának alapelveit.
A vitaminok és nyomelemek onkológiai alkalmazása
A táplálkozás és a daganatos megbetegedések kialakulása, valamint a daganatkontroll összefüggéseit már hosszú ideje tanulmányozzák, mivel a táplálkozásnak alapvető szerepe van a daganatos betegek kezelésében. A vitaminok és nyomelemek megfelelő onkológiai alkalmazásához több szakmát átölelő multidiszciplináris munkacsoportot javasolt felállítani, hogy a felméréstől a gyakorlati kivitelezésig biztosított legyen a több tudományterületen dolgozó szakember (mint például onkológus, dietetikus, laboratóriumi aszszisztens) szakmai felügyelete. Ezzel jobban kiegyensúlyozható az egyén állapotához igazított szükséglet. A megfelelő állapotfelmérés (labor-, bélmikrobiom- és nutrigenetikai vizsgálatok), illetve célmeghatározás segíti a dietetikus szakembert a vitaminok és nyomelemek pontosabb meghatározásában, azok mennyiségének és beviteli módjának (táplálékkal szájon át vagy étrend-kiegészítő formájában) a kialakításában. A dietetikus szakember segít az egyénnek jelenlegi táplálékkal bevitt tápanyagbevitelét elemezni, aktuális állapotához igazított szükségletei értékeit meghatározni és a gyakorlatban kivitelezni.
A másodlagos májáttét eltávolításának indikációja – új terápiás megközelítések
A májsebészetben jelentős fejlődés volt megfi gyelhető az utóbbi évtizedekben: a műtét mortalitása rendkívüli mértékben csökkent, és az új technikák alkalmazásával a korábban technikailag nem műthető esetek váltak operálhatóvá. A máj a daganatok áttéteinek leggyakoribb helye, így a modernizáció a metasztázisok sebészetében is változásokat hozott. A műtéti mortalitás jelentős csökkenésével olyan szervek esetében is felmerült a májáttétek eltávolításának lehetősége, amelyeknél korábban nem tartottak műtétet indokoltnak (gyomor, pancreas). Az új technikák (laparoszkópia, portaembolisatio) alkalmazása óta eltelt idő alatt megjelent tanulmányok már lehetőséget adnak arra, hogy felmérjük onkológiai szempontból is az eredményeket. A laparoszkópos technika már nemcsak a primer tumorok, hanem a májáttétek kezelésében is teret nyert: a rövid és hosszú távú hatások, illetve az onkológiai eredmények szintén megfelelnek a nyitott műtétekének. Bár erre nagy esetszámú közlések nincsenek, a colorectalis daganatok szimultán májáttéteinek egy ülésben végzett reszekciójának növekedése várható a laparoszkópos technika alkalmazásától. A kiterjedt májáttétek esetében az érreszekcióval végzett májműtétek, elégtelen posztoperatív residualis májfunkció miatt végzett portaocclusio után végzett májreszekciókkal is jobb eredmény érhető el, mint az onkológiai kezeléssel. A májáttétek esetében az onkológus és a sebész közös döntése szükséges a megfelelő terápiás terv felállításához.
1.
2.
3.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről4.
5.
1.
2.
Klinikai Onkológia
A rosszindulatú daganatok fenotípusának plaszticitása és az immunogén mimikri3.
Klinikai Onkológia
A szarkopénia mérése komputertomográfiával és jelentősége az onkológiai betegeknél4.
5.