Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 276
Az avalgükozidáz-α-val végzett, 3. fázisú COMET vizsgálat hatásossági és biztonságossági eredményei késői kezdetű Pompe-kórban szenvedő betegeknél
Az α-avalglükozidáz (neoGAA) humán, rekombináns, savanyú α-glükozidáz enzimpótló terápia; fejlesztésének célja az enzim mannóz-6-foszfát-receptorhoz való kötődésének fokozása, ezáltal az enzim felvételének javítása. Mindez a glikogén clearance-t fokozva az α-alglükozidázhoz (GAA) képest javítja a klinikai hatásosságot. A kezelésben még nem részesült, késői kezdetű Pompe-kóros betegek neoGAA- (n = 51) és GAA- (n = 49) kezelését összehasonlító, 3. fázisú, kettős vak COMET vizsgálat (NCT02782741/Sanofi Genzyme) eredményeiről számolunk be (a kiindulástól a 49. hétig bezárólag).
A lokálisan előrehaladott NSCLC konszolidációs immunterápiája
A lokoregionálisan előrehaladott, inoperábilis, III-as stádiumú nem kissejtes tüdőrákok (NSCLC) „standard of care” ellátása a konkurens radiokemoterápia. Bár a szekvenciális kezeléshez képest a konkurens kezelés közel 50% aránnyal növeli az ötéves túlélés esélyét (10,6% versus 15,1%), így is, sajnos, kedvezőtlen prognózisú folyamatként tekintünk a kórképre. Az új immunterápiás lehetőségek megjelenése az áttétes tüdőrák kezelésében komoly előrelépést hozott. Ezen eredmények alapján koraibb, még potenciálisan gyógyítható stádiumban vizsgálják az immunellenőrzőpont-gátlás hatékonyságát. A PACIFIC trial eredményei alapján ma már magas evidencia támasztja alá a konkurens kemoradioterápiát követő konszolidációs immunterápia túlélésre gyakorolt jelentős hatását. Számos jelenleg is futó klinikai vizsgálat teszteli az immunterápiák hatékonyságát ebben az indikációban.
A krónikus stressz szerepe az essentialis hypertonia kialakulásában. A rilmenidin helye a stressz által kiváltott hypertonia kezelésében
A hypertonia a cardiovascularis betegségek egyik önálló rizikótényezője. Kialakulásában számos tényező játszik szerepet. Ezek közül a krónikus stressz a szimpatikus aktivitás fokozásán keresztül eredményezheti a magasvérnyomás-betegség kialakulását. A szimpatikus idegrendszeri aktivitás emelkedésének jeleit elsősorban a hypertonia kezdeti – perctérfogat-fokozódással járó – szakaszában észlelhetjük. A szimpatikus aktivitás fokozódása a hemodinamikai következményeken (perctérfogat-emelkedés, tachycardia, coronariavasoconstrictio, proarrhythmia) túl számos kedvezőtlen következménnyel járhat. A metabolikus (inzulinrezisztencia, dyslipidaemia), strukturális és trofikus hatásokon túl (endotheldiszfunkció, vascularis hypertrophia, myocardium-hypertrophia), thromboticus és humorális (prokoaguláció, thrombocytaaggregáció-fokozódás, nátriumretenció, renin-angiotenzin-aldoszteron tengely aktivációja) folyamatok indulhatnak el, amelyek több támadásponton károsíthatják a szervezet működését. A fokozott szimpatikus aktivitás kedvező befolyásolására számos antihypertensiv gyógyszercsoport áll rendelkezésünkre. Idetartoznak a perifériásan ható alfa- és béta-blokkolók, továbbá a centrálisan ható vegyületek. Ez utóbbiak első generációját (például clonidin, guanfacin, alfa-metildopa) – jelentős mellékhatásprofiljuk miatt – jelenleg ritkán, egyáltalán nem vagy csak szűk indikációs körben alkalmazzuk. A második generációs, centrálisan ható vegyületek közül a rilmenidin, az imidazolin-I1-receptorok stimulációjának útján fejti ki kedvező hatásait, amelyeket kihasználhatunk a szimpatikus idegrendszer fokozott aktivitásával járó enyhe vagy mérsékelt hypertoniában.
[Késői kezdetű Sandhoff-betegség atípusos jelentkezése: esetismertetés]
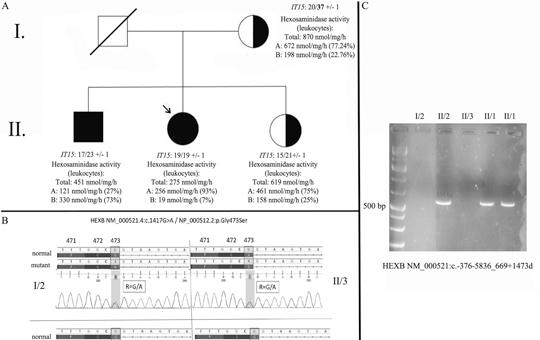
[Bevezetés – A Sandhoff-betegség egy olyan ritka, hereditaer GM2-gangliosidosis (autoszomális recesszív), amit a HEXB gén mutációja okoz. A hexózaminidáz (Hex) enzim β-alegységének károsodása miatt mind a Hex-A, mind a Hex-B izoformák működése zavart szenved. A betegség súlyossága, valamint a tünetek kezdete (infantilis vagy klasszikus, juvenilis, felnőttkori) a residualis enzimaktivitás függvénye. A késői kezdetű formát szerteágazó tünettan jellemzi. Jelen lehetnek többek között motoneuronbetegségre utaló eltérések, ataxia, tremor, dystonia, valamint pszichiátriai és neuropathiára utaló jegyek is. A 36 éves nőbeteg 9 éve tartó, progresszív, szimmetrikus alsó végtagi gyengeség miatt jelentkezett klinikánkon. A részletes neurológiai szakvizsgálat enyhe fokú szimmetrikus gyengeséget igazolt a csípőflexorokban, a többi izomcsoport megkíméltsége mellett. Mindkét oldalon a Patella-reflex renyhe volt. A laboratóriumi vizsgálatok releváns eltérést nem mutattak. A rutin elektro-encefalográfiás, valamint a koponya-MR-vizsgálatok a beteg panaszait magyarázó eltérést nem detektáltak. Az elektroneuronográfiás, valamint az elektromiográfiás vizsgálatokon szenzoros neuropathiának megfelelő eltérések látszottak. Az izombiopsziás minta elemzése kapcsán enyhe fokú neurogén károsodásra derült fény. A beteg öccse (32 éves) hasonló tüneteket mutat. Páciensünk részletes genetikai vizsgálata során két ismert patogén eltérést találtunk a HEXB génben, egy missense mutációt, valamint egy 15 008 bázispár hosszúságú deletiót (NM_000521.4:c.1417G>A; NM_000521:c.-376-5836_669+1473del; kettős heterozigóta állapot). A szegregációanalízis, valamint a családtagok hexózaminidáz-vizsgálata a késői kezdetű Sandhoff-betegség diagnózisát megerősítették. A jelen esetismertetés célja, hogy felhívja a figyelmet a késői kezdetű Sandhoff-betegség differenciáldiagnosztikai jelentőségére felnőttkorban kezdődő, proximális predominanciát mutató szimmetrikus alsó végtagi gyengeség esetén.]
Magas vérnyomás, kognitív funkció és demencia. A magas vérnyomást csökkentő kezelés jelentősége
A hypertensio jelentősége a szív- és érrendszeri történések egyik fő kockázati tényezőjeként megkérdőjelezhetetlen. Az életkor és társbetegségek szerint differenciált célvérnyomásértékek elérésével a cardiovascularis történések rizikója szignifikánsan csökkenthető. Korántsem közömbös azonban, hogy az így megszerzett többletéletéveket a beteg milyen életminőségben tölti el. Ez számos társdiszciplína területét érintő komplex kérdéskör, de ezek egyik legfontosabbika a szellemi egészség, a kognitív funkciók megőrzése, a demencia elkerülése. A magas vérnyomás az artériák simaizomzatának károsításával, az érelmeszesedés gyorsításával rontja a célszervek, így az agy vérellátását is, amely a tenzió mértékével arányosan növeli a mentális hanyatlás kockázatát, gyakoriságát, súlyosságát. Ennek mind az egyén, mind a család, mind a társadalom egésze szempontjából komoly jelentősége van. Sajátos ellentmondás, hogy a vérnyomás céltartományba kezelése nem jelenti automatikusan a kognitív funkciók megőrzését, a demencia kockázatának elkerülését. Nagy vizsgálatok metaanalízisei kimutatták, hogy az egyes antihypertensivum hatástani csoportok között e tekintetben is különbségek igazolódtak. Úgy tűnik, hogy a renin-angiotenzin rendszer gátlóinak és a dihidropiridin-kalcium antagonistáknak e vonatkozásban prioritása van. A szerzők áttekintést adnak a hypertensio és a mentális képességek kapcsolatáról, az irodalom áttekintésével a vérnyomáscsökkentő kezelés hatásairól, különös tekintettel a kognitív funkciókra és a demenciára kifejtett hatásokra.
Idegtudományok
2021. OKTÓBER 25.
PFO-zárás kriptogén stroke-ban
Az ischaemiás stroke-ok 20-30%-a kriptogén, azaz az infarktus nem köthető definitív emboliaforráshoz, nagyér-atherosclerosishoz vagy kisérbetegséghez. A kriptogén stroke-ok egy részében nyitott foramen ovale (patent foramen ovale, PFO) van jelen, ami felveti annak lehetőségét, hogy az agyi infarktus egy PFO-n keresztüli paradox embolisatio következtében alakul ki. Ismert, hogy a PFO mechanikus zárása alkalmasan megválasztott betegcsoportban csökkenti az ismétlődő stroke kockázatát. Kasner és munkatársai a The New England Journal of Medicine-ben megjelent cikkükben a Gore REDUCE prospektív, randomizált, open-label vizsgálat 5 éves kimeneteli eredményeit közlik, melyben két PFO-záró eszközös eljárás hatékonyságát és biztonságosságát hasonlítják össze a kizárólagos konzervatív terápiával (thrombocytaaggregáció-gátlás, TAG).
Központi idegrendszeri vasculitis gyanújával vizsgált betegek vizsgálati eredményeinek retrospektív feldolgozása (OMIII, 2016–2021)
Bevezetés: A központi idegrendszeri (KIR) közép- és nagyérvasculitisek az intracranialis és nyaki artériák gyulladásával járó betegségek, melyek az érfal megvastagodása miatt az artériák szűkületét vagy elzáródását okozhatják. Ezen vasculitisek leggyakoribb tünete az agyi infarktus, az átmeneti agyi keringési zavar és a fejfájás. A primer KIR-vasculitis kizárólag az intracranialis ereket érinti, eredete ismeretlen. A szekunder KIR-vasculitisben az intracranialis erek gyulladása szisztémás kórkép (például SLE, HSV-fertőzés) részeként alakul ki. Célkitűzés: Az OMIII (korábban OKITI) Neurológiai Osztályán KIR-vasculitis iránydiagnózissal kezelt betegek vizsgálati eredményeinek feldolgozása a differenciáldiagnosztikai algoritmus pontosítása céljából. Módszerek: Az intézetünkben 2016. január és 2021. július között KIR-vasculitis gyanújával vizsgált 46 beteg vizsgálati eredményeinek statisztikai feldolgozása. Eredmények: Az akut stroke-ellátás során végzett CTA- és DSA-vizsgálat számos esetben felhívja a figyelmet KIR-i vasculitis lehetőségére. A pontos diagnózis felállításában segít a vasculitisprotokollal végzett koponya- MR- és MRA-vizsgálat. A megadott időszakban összesen 46 betegnél készült vasculitisprotokoll szerint MR- és MRA-vizsgálat. Az UH-val kimutatható halo-jel hasznos noninvazív kiegészítője a képalkotó vizsgálatoknak, ugyanakkor hiánya nem zárja ki a vasculitis lehetőségét. Pozitív halo-jel esetén végzett a. temporalis biopszia az esetek nagy részében alátámasztja a diagnózist. Hat betegnél (13%) láttunk egy vagy két oldali pozitív halo-jelet, ezek közül 3 betegnél lett pozitív a temporalis biopszia. Szérum- és liquorszerológiai vizsgálatok (szérum: HIV, HCV, HBV, VZV, HSV, Treponema pallidum, Borellia burgdorferi, liquor: HSV, VZV, Borellia) szükségesek a szekunder vasculitis kizárásához. A radiológiai vizsgálatok, a rutin labor- és a szerológiai vizsgálatok eredménye alapján 17 betegnél (37%) igazoltunk KIR-vasculitist; minden diagnosztizált beteg szteroid- vagy speciális immunterápiában (rituximab, MTX, cyclophosphamid) részesült. Összefoglalás: A központi idegrendszeri vasculitis lehetséges tünetei a stroke és a TIA-események. A betegség diagnosztizálása fontos, mert ezen betegek esetében a szekunder prevenciós módszerek (thrombocytaaggregáció- gátlás, antikoaguláció, lipidcsökkentés) nem elégségesek, a sikeres kezeléshez immunmoduláns terápia szükséges. A központi idegrendszeri vasculitisek diagnózisához körültekintő klinikai szemlélet szükséges, speciális eszközös vizsgálati módszerek és protokollok alkalmazásával.
Paradigmaváltás a krónikus szívelégtelenség gyógyszeres terápiájában
A szívelégtelenség incidenciája, prevalenciája folyamatosan növekszik, a betegség morbiditása és a mortalitása továbbra is nagy, így a kórkép jelentősége óriási, megfelelő kezelése kiemelt jelentőségű. A betegség prognózisát javító érdemi evidenciák továbbra is csak csökkent balkamra-funkcióval járó krónikus szívelégtelenség (HFrEF) kezelése esetén állnak rendelkezésre. Az elmúlt évtizedekben számos „mérföldkővizsgálat” született, melyek eredményei a mai napig alapjaiban határozzák meg a betegség terápiáját. A HFrEF bázisterápiája sokáig három alappillérre épült: angiotenzinkonvertáló-enzim- (ACE-) gátló, β-blokkoló és mineralokortikoidreceptor-antagonista, melyek I/A ajánlási szinttel szerepelnek a különböző szívelégtelenség-ajánlásokban. 2014-ben publikálták az áttörő sikert hozó, nagy jelentőségű PARADIGM-HF (heart failure) vizsgálatot, amelyben egy teljesen új gyógyszercsoportot, az angiotenzinreceptor-blokkoló/ neprilysininhibitor (ARNI-) vegyületek csoportjába tartozó sacubitril/valsartant vizsgálták HFrEF-betegeken. A vizsgálat eredménye szerint a sacubitril/valsartan szignifikáns mértékben, 20%-kal csökkentette a cardiovascularis (CV) halálozás és a szívelégtelenség miatti hospitalizáció primer összetett végpontját, valamint 16%-kal csökkentette az összmortalitást egy aktív komparátorhoz, az HFrEF terápiájában a legnagyobb evidenciákkal rendelkező enalaprilhoz képest. Az Európai Kardiológusok Társasága (European Society of Cardiology, ESC) 2016-os szívelégtelenség-irányelve I/B evidenciaszinttel javasolja a sacubitril/ valsartan alkalmazását ACEI helyett a szívelégtelenség miatti hospitalizáció és halálozás csökkentése céljából olyan ambuláns HFrEF-betegek esetén, akik az optimális ACEI, β-blokkoló (BB) és mineralokortikoidreceptor-antagonista (MRA-) kezelés ellenére is panaszosak maradnak. A későbbiekben sacubitril/valsartannal több kisebb vizsgálatot is publikáltak kissé eltérő indikációkkal és más betegcsoportokon. A PIONEER-HF vizsgálat bizonyította, hogy a sacubitril/valsartan terápia korai, az akut szívelégtelenség stabilizációját követően történő megkezdése biztonságos és hatékony HFrEF-betegek esetén, gyorsabban csökkenti a szívelégtelenség prognózisával korreláló NT-proBNP-szintet, mint az enalapril. A TRANSITION és a TITRATION vizsgálat a sacubitril/valsartan terápia kezdetéről, a dózistitrálás módjáról adott hasznos információkat. A sacubitril/ valsartan megjelenése új korszak kezdetét jelentette néhány évvel ezelőtt a HFrEF terápiájában. Ez a korszak Magyarországon most zajlik. Elképzelhető, hogy az SGLT-2-inhibitoroknak köszönhetően egy újabb korszak kapujában állunk, és erre várhatóan választ ad majd az ESC idén megjelenő új szívelégtelenség-ajánlása.
Bradikinin-citokin vihar és patomechanizmusa igen súlyos Covid-19-fertőzésben
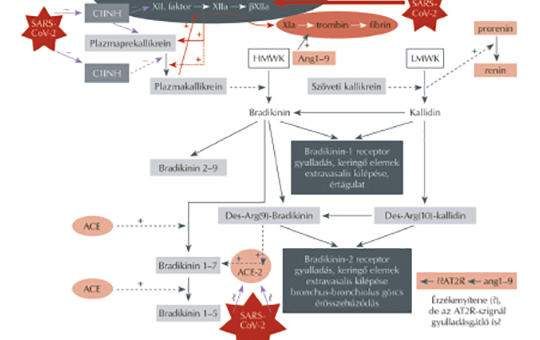
A szerzők a súlyos, fékezhetetlen szisztémás gyulladásba, thromboticus folyamatokba torkolló Covid-19 patomechanizmusának hátterét, a fertőző koronavírus, a lokális celluláris-szöveti kontakt rendszer, a kinin-kallikrein és renin-angiotenzin rendszerek rendkívül komplex interakcióit tekintik át közleményükben. Kritikusan értékelik a súlyos Covid-19 hátterében a domináns bradikinin-citokin vihart fékező, lehetséges terápiás beavatkozásokat, amelyek támadáspontja a bradikininképződés mérséklése, bontásának elősegítése, a B2-receptor, vagy az indukált citokinválasz blokkolása.
RAAS-gátló kezelés – Covid-pandémia
A SARS-CoV-2 okozta különböző méretű és lefolyású akut légzési szindróma ma az egészségügyi rendszerek legnagyobb kihívása világszerte. A Covid-19 klinikai képének kialakulásában döntő szerepe van a renin-angiotenzin-aldoszteron, valamint a kinin-kallikrein rendszernek, illetve ezen rendszereken belül két endopeptidáznak, az ACE és ACE-2 enzimeknek. Az ACE által stimulált Ang II/AT1R tengely káros hatásait (oxidáns, gyulladáskeltő hatás, vasoconstrictio) az ACE-2 által indukált AT2R- és MasR-aktivitás (antioxidáns, gyulladáscsökkentő hatás, vasodilatatio) ellensúlyozza. A SARS-CoV-2 azért okoz ilyen súlyos tüdő- és szisztémás gyulladást, mert az ACE-2-t, mint a tüdő fontos védelmi tényezőjét, károsítja a SARS-CoV-2 fehérjetüskéje az ACE-2-höz kötődéssel, ami az ACE-2-szint csökkenéséhez vezet. Ezzel párhuzamosan fokozott a bradikinintermelődés, amely a BKB1- és BKB2-receptorok révén ugyancsak erősíti a SARS-CoV-2 gerjesztette citokinvihart. Mivel a RAAS-gátló szerek (ACEI, ARB) különböző támadási helyeken és különböző mértékben befolyásolják a két említett szabályozó rendszert és enzimeket, sürgős volt szerepük tisztázása a Covid-fertőzés során, hiszen alkalmazásuk igen kiterjedt és nélkülözhetetlen pillére számos népbetegségnek (hypertonia, cardiorenalis anyagcsere-betegségek). A patofiziológiai és kísérletes adatok alapján jogosan feltételezhető, hogy Covid-fertőzésben a társbetegségekkel járó esetekben – kifejezetten az idős egyéneknél – a csökkent ACE-2-expressziót a RAAS-gátlók helyreállíthatják, és újra érvényesülni tud az elmaradt, vagy csökkent védőhatás. Ez a védőhatás mindkét RAAS-gátlóra érvényes. A klinikai vizsgálatok egyértelműen alátámasztják a különböző nemzetközi társaságok deklarált véleményét, miszerint a RAAS-gátlók alkalmazása nem növeli a Covid-19-előfordulást, illetve a súlyos, kritikus Covid-betegek megjelenésének kockázatát. Ennek értelmében az elindított RAAS-gátló kezelést folytatni lehet és szükséges a Covid-19 betegség kialakulása folyamán.
1.
2.
3.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről4.
5.
1.
2.
Klinikai Onkológia
Hasnyálmirigyrák: az ESMO klinikai gyakorlati irányelve a diagnózishoz, kezeléshez, követéshez*3.
Klinikai Onkológia
Gyógyszerbiztonsági szemelvények – a múlt tanulságai és a jövő lehetőségei4.
5.