Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 317
Az angiotenzinkonvertálóenzim-gátló/kalciumcsatornablokkoló fix gyógyszer-kombinációk egyéves perzisztenciája hypertoniában
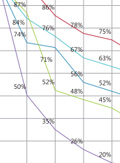
A legfrissebb európai hypertoniaajánlás a magas vérnyomás kezelésére első terápiás lehetőségnek javasolja a renin-angiotenzin-aldoszteron rendszer antagonistáknak (RAAS-gátlók) a kalciumcsatorna-blokkolókkal (CCB) vagy diuretikumokkal alkotott fix kombinációit (FDC). Az antihipertenzív terápia során a terápiahűség az egyik jelentős tényező a nemkívánatos cardiovascularis események csökkentésében. Célkitűzés: A szerzők célja a hypertonia indikációjában indított angiotenzinkonvertálóenzim-gátlók (ACE-gátlók)/CCB FDC-k egyéves perzisztenciájának összehasonlítása volt. Módszer: A retrospektív vizsgálatban a szerzők a 2012. október 1. és 2013. szeptember 30. közötti időszakban első alkalommal, bár - mely ACE-gátló/CCB FDC-k receptjeit kiváltó betegeket választották ki, akik a megelőző 12 hónapban hasonló készítményekkel nem részesültek antihipertenzív terápiában. A vénykiváltási adatokat az Országos Egészség biztosítási Pénztár vényforgalmi adatbázisa szolgáltatta. A perzisztencia modellezésére a túlélésanalízis klasszikus eszköztárát alkalmazták, ahol a „túlélési” idő a gyógyszer szedésének abbahagyásáig eltelt idő volt. Eredmények: A bevonási követelményeknek 124388 beteg felelt meg. A ramipril/amlodipin FDC egyéves perzisztenciája 54% volt, amelyet a perindopril/amlodipin FDC 47%-os, a lizinopril/amlodipin 36%-os, a ramipril/felodipin 26%-os és a trandolapril/verapamil 12%-os eredménye követett. A ramipril/amlodipin FDC-hez képest (referencia) a perindopril/amlodipin FDC elhagyásának kockázata 30%-kal (HR = 1,30, p < 0,0001), a lizinopril/amlodipin FDC-é 79%-kal (HR = 1,79, p < 0,0001) volt magasabb, míg a ramipril/felodipin FDC-é (HR = 2,28, p < 0,0001) mintegy kétszeres, a trandolapril/verapamil FDC-é (HR = 4,13, p < 0,0001) pedig több mint négyszeres volt. A 360 napra korlátozott átlagos gyógyszerszedési idő 270,2 nap volt a ramipril/amlodipin FDC, 242,7 nap a perindopril/amlodipin FDC, 211,2 nap a lizinopril/amlodipin FDC, 186,3 nap a ramipril/felodipin FDC, míg 125,7 nap a trandolapril/verapamil FDC esetén. Következtetések: A szerzők igazolták, hogy a hypertonia indikációjában alkalmazott ACE-gátló/CCB FDC-k egyéves perzisztenciája jelentősen különbözött. A betegadherencia szempontjából a legelőnyösebbnek a ramipril/amlodipin FDC bizonyult.
Új lehetőségek a tüdőrák kezelésében
Az utóbbi években az onkológia területén hatalmas kutatás folyik és ennek eredményeként lényegesen hosszabb túlélést láthatunk az orvoslás ezen területén. A tüdőrák, ha nem is vált gyógyítható betegséggé, kezd a krónikus betegségek családjába tartozni. Mind a sebészeti bravúrok, mind a sztereotaxiás radioterápia és a gyógyszeres kezelésben bekövetkezett változások eredményeként ma már az áttétes tüdődaganatos betegcsoportban sem ritka az ötéves túlélés, relatíve hosszú progresszióig eltelt idő mellett. Nagy túlélési előnyt jelentett a korábbi, harmadik generációs citotoxikus kombinációk után a hozzáadott, érnövekedés- gátló (VEGF-gátló) maintenance kezelés vagy a folyamatos pemetrexed citotoxikus kemoterápia. Az első igazi áttörést, a hosszú progressziómentes túlélést a célzott kezelés hozta, amely ismert driver mutációk mellett bizonyult hatékonynak. A másik nagy eredményt, különösen az éveken át „mostoha” laphámsejtes karcinómánál, az immunterápia, az immunellenőrző pontok gátlása jelentette, amelynek hatékonysága adenocarcinomában is igazolódott. Számos kutatás folyik az immunterápia adjuváns, neoadjuváns, valamint kombinált alkalmazásával (akár sugárterápiával, akár citotoxikus kemoterápiával kombinálva).
A stroma szerepe a rosszindulatú daganatok viselkedésében
A daganatok stromáját hosszú időn át úgy tekintették, mint ártatlan mellékszereplőt, ami nem befolyásolja a tumorok biológiai viselkedését. Ez a nézet az elmúlt 20 évben jelentősen megváltozott. Ismereteink gazdagodásával bebizonyosodott, hogy a stroma minden egyes sejtes eleme és alapállománya is aktív résztvevő a daganat kialakulásában és progressziójában. A kezdetben védőszerepet is játszó stromát a daganatsejtek gyorsan saját szolgálatukba állítják. Gyakorlatilag nincs olyan stromalis komponens, amely ne befolyásolná a rosszindulatú daganatok viselkedését. Ez lehet a daganatsejtek proliferációjának, inváziójának serkentése a stroma merevségének növelésével, energiatermelés a tumorsejtek számára, citokinek, növekedési faktorok előállítása és prezentációja, a daganatok vérellátása. Ez a felismerés vezetett új típusú, a daganatos neostroma komponenseinek gátlását célzó terápiák tervezéséhez. Ezek közül a legsikeresebb az immun- és az angiogenezist gátló terápia, de számos más target gátlására is folyamatos próbálkozások tanúi lehetünk.
Hogyan javítható a vérnyomáscsökkentő terápia hatékonysága diabeteses hypertoniás betegeknél?
A hypertonia, az első számú „néma gyilkos” évente 10 millió halálesetért felelős világszerte. Igen gyakran társul egyéb metabolikus rizikófaktorokkal, a 2-es típusú diabetes mellitusszal és a dyslipidaemiával, jelentősen fokozva ezen betegek globális cardiovascularis kockázatát. Kezelésük, a szigorú célérték elérése igazi kihívás a gyakorló orvosok számára.
Hogyan befolyásolja a BRCA-státusz az emlőrák ellátását 2019-ben?
A germinalis BRCA-státusz korai vagy előrehaladott/áttétes emlőrákban egyaránt befolyásolja az ellátás menetét. Így ideális esetben a beteg informáltan dönthet a műtét típusáról, a sugárkezelés elkerüléséről; a BRCA-státusz a legújabb eredmények alapján befolyásolja a neoadjuváns, adjuváns, palliatív kemoterápia megválasztását, továbbá új, hatékony célzott (target) terápia alkalmazását vetheti fel. Specifikus terápiának számítanak a DNS-támadáspontú citosztatikumok, mindenekelőtt a platinakészítmények és a szintetikus letalitás elve alapján ható PARP-inhibitorok. E speciális gyógyszercsoportok optimális helye és sorrendje egyelőre nem ismert. A nemzetközi ajánlások valamennyi HER2-negatív (NCCN) vagy legalább a mutatók alapján valószínű BRCA-mutációt hordozó (ESMO) előrehaladott/áttétes emlőrákos esetben sürgetik a BRCA-státusz-vizsgálatot a megfelelő terápiás stratégia meghatározása érdekében. Az elmúlt időszakban a BRCA-státusz meghatározására szolgáló módszerek óriási fejlődésen mentek át, és egyre szélesebb körben elérhetőek különféle szolgáltatók kínálatában. A mutáció azonosításához a teljes gének szekvenálása szükséges, amelyre a korábbi módszereknél gyorsabb és költséghatékonyabb megoldást nyújt az új generációs szekvenálóplatformok (next generation sequencing - NGS) alkalmazása. A kezelőorvos felelőssége, hogy amennyiben a részletes családi anamnézis, a beteg életkora, esetleges megelőző daganatos betegsége és nem utolsósorban a daganatjellemzők alapján felmerül, gondoljon patogén BRCA-mutáció jelenlétére, mérlegelje a teszt indokoltságát, illetve vesse fel a beteg számára a lehetőséget.
Előremutató terápiák kasztrációrezisztens áttétes prosztatarákban
Bevezetés: A prosztatarák világszerte a második leggyakoribb daganatos betegség, és az Európai Unióban az 50 fölötti férfi ak leggyakrabban diagnosztizált daganata. Változatlanul az androgéndeprivációs terápia a kiújult vagy áttétes betegség kezelésének alapja. Szerencsétlen módon viszont csaknem az összes beteg rezisztenssé válik az androgénblokáddal szemben, és kialakul a „kasztrációrezisztens prosztatarák” (CRPC) képe. Az utóbbi 10 évben az új kezelési lehetőségeknek köszönhetően drámaian javult az áttétes CRPC-ben (mCRPC) szenvedő férfi ak túlélése. A legmodernebb terápiák az AR-axis-gátlók és a taxánalapú kemoterápiák, valamint a radiofarmakonok és a sipuleucel T. Az érintett területek: A szerzők az áttétes CRPC legújabb szisztémás kezelési lehetőségeit tárgyalják. Ezután a legújabb kezelések részletes analízise következik, és tárgyalják az új terápiák alapját képező biológiai okokat. Szakértői vélemény: Mivel számos vizsgálat igazolta, hogy a docetaxel és az új hormonális szerek meghosszabbítják az áttétes CRPC-ben szenvedők, valamint a nem áttétes CRPC-ben szenvedők élettartamát, várható, hogy a betegek egyre növekvő alcsoportjában korán lehet kemoterápiát és az AR-t célzó anyagokkal végzett kezeléseket elindítani. Alapvető, hogy találjunk új stratégiákat a gyógyszer-rezisztencia legyőzésére, amellyel tovább javulhat a betegek túlélése.
Thrombocytaaggregáció-gátló kezelés perifériás érbetegségben - Paradigmaváltás a gyakorlatban?
A perifériás verőérbetegség (PAD) a társuló multilocularis atheroscleroticus betegségek következtében igen nagy mortalitású betegség. Tünetes PAD esetén a jól megválasztott antithromboticus kezelés nemcsak az alsó végtagi vascularis események, hanem a cardiovascularis halálozás, stroke és myocardialis infarctus kompozit végpont előfordulási arányának csökkentése szempontjából is kulcsfontosságú. Ezen a területen a thrombocytaaggregáció-gátló acetilszalicilátnál jobb eredményt lehetett elérni clopidogrellel, de a két szer kombinációja már nem jár a cardiovascularis major események számának csökkenésével. Az elmúlt évek vizsgálatai alapján számos, egyéb hatóanyagról bizonyosodott be, hogy a PADbetegek csoportjában nem előnyösebb alkalmazásuk a hagyományos thrombocytaaggregáció-gátló szereknél. Terápiás gyakorlatunkban változást jelenthet azonban a Xa-faktor-gátló rivaroxaban kis dózisának és az acetilszalicilátnak a fix kombinációja, amely a monoterápiánál jobb eredményeket tudott felmutatni a kombinált cardiovascularis végpontot illetően, elfogadható vérzéses kockázatnövekedés mellett.
Intenzív (clopidogrel + aszpirin + dipiridamol) és irányelv (aszpirin + dipiridamol vagy clopidogrel) szerinti thrombocytaaggregáció-gátló terápia összehasonlítása akut cerebralis, nem cardioemboliás ischaemiás beteg
Ischaemiás stroke és tranziens ischaemiás attak (TIA) esetén az ismétlődés veszélye legnagyobb az esemény után közvetlenül és hétről hétre csökken. Az aszpirin csökkenti a korai ismétlődés kockázatát (IST, CAST vizsgálatok), de a kettős gátlás még hatékonyabb. A CHANCE vizsgálatban magas kockázatú betegeknél az aszpirin (ASA) + clopidogrel kombináció hatékonyabbnak bizonyult, mint az ASA önmagában. Felmerült a kérdés, hogy ha a kettős kombináció hatékonyabb, akkor a rövid idejű hármas támadáspontú thrombocytaaggregáció-gátló (TAG) kombináció [ASA: ciklooxigenáz irreverzibilis gátlás, clopidogrel: ADP (adenozin-difoszfát)-receptor irreverzibilis blokkolás, dipiridamol: tct. cAMP (ciklikus anonozonmonofoszfát)- és/vagy cGMP (ciklikus guanozinmonofoszfát)- szintet növeli] hozhat-e még előnyt ennek a betegcsoportnak a kezelésében. Ezt in vitro TAG-vizsgálatok, thrombocyta-leukocyta konjugációs, leukocytaaktivációs vizsgálatok, illetve egészséges önkénteseknél és korábban stroke-on átesett betegeknél végzett kisebb létszámú vizsgálatok, esettanulmányok kettős kombináció ellenére is visszatérő epizód esetén hosszú távon alkalmazott effektív hármas kombináció mellett is bizonyítják.
A tüdőrák immunterápiája az újabb eredmények tükrében
Tíz évvel ezelőtt az előrehaladott stádiumú tüdőrák esetén, mind a kissejtes (SCLC), mind pedig a nem kissejtes (NSCLC) csoportban, a várható átlagos túlélés egy év körüli volt. Ez, sajnos, az SCLC esetén lényegileg mára sem változott. Az NSCLC kezelésében igazi forradalmi időszakot élünk át. A patológiai alcsoportokra specifikált kombinált citotoxikus kemoterápia mellett igen hosszú túléléssel kecsegtet a célzott terápia (EGFR-mutáció, ALK, ROS1, BRAF-pozitivitás esetén). Az SCLC vonatkozásában a klinikai gyakorlat tekintetében jelentős előrelépés a gyógyszeres kezelésben az utóbbi harminc évben nem történt. Az újabb terápiás lehetőség NSCLC fennállásakor előrehaladott stádiumban az immunellenőrzőpont-gátló terápia, amely három éve már a klinikumban is a komplex kezelés része, hazánkban is. A PD1, a PDL1 és a CTLA4-gátló vegyületek beépítése a terápiás gyakorlatba igazi, új kihívás. Előrehaladott stádiumú NSCLC fennállásakor, magas PDL1-expresszió esetén, első vonalban új standard a pembrolizumab-monoterápia. Második vonalban mind a pembrolizumab, mind a nivolumab, mind pedig az atezolizumab evidenciaalapon adható. Az NSCLC-betegek mintegy harmadát kitevő lokálisan kiterjedt esetekben a radiokemoterápia után alkalmazott konszolidációs fenntartó durvalumab terápia új hatékony lehetőség. Az eddigi gyógyszeres terápiás nihilizmus az SCLC esetén oldódni látszik. Az antitestgyógyszerkonjugátummal végzett terápia alkalmazásának lehetősége már a közeljövőben a klinikumban is várható. A nivolumab, illetőleg a nivolumab + ipilimumab kombináció szintén ígéretes eredményekkel kecsegtet SCLC másod-, illetőleg többedvonalbeli kezeléseként. A biomarker-szelekción alapuló kezelési terv mind NSCLC, mind pedig SCLC esetén részben gyakorlat, részben kutatási irány (például PDL1-expresszió, szomatikus mutációs arány [TMB], DLL3, cMyc stb.). A különböző gyógyszeres kezelési modalitások egyedi alkalmazása helyett az okos, biomarker-szelekción alapuló komplex terápiás stratégia segíthet e betegség eddigi szerény terápiás eredményeinek javításában, krónikus betegséggé való formálásában.
Malignus daganatos megbetegedések okozta neurológiai kórképek
Az onkológiai betegségek okozta neurológiai tünetek, tünetegyüttesek egy szerteágazó etiológiájú heterogén klinikai entitás, amely érintheti a központi és perifériás idegrendszert, lehet primer vagy szekunder, de létrejöhet akár immunmediált folyamatok útján is. Összefoglaló cikkünkben áttekintjük az onkológiai gyakorlatban előforduló neurológiai kórképeket és vezető tüneteket. Kiemelten tárgyaljuk a háttérben álló leggyakoribb daganatként az agyi metasztázisokat, amelyek jelenleg az új célzott és immunterápiák fókuszpontjába kerültek, s napjainkban is egyre bővül azon szerek köre, amelyek intracranialis aktivitást mutatnak. Részletezzük a daganatok okozta paraneoplasiás neurológiai szindrómákat, mert bár ritkák, de egyre jobban diagnosztizálhatók, és gyors felismerésük elengedhetetlen a háttérben álló daganatos folyamat detektálásában. Végül a tumorok kezelésének mellékhatásaként újabban megfi gyelhető neurológiai tüneteket ismertetjük, mint a PD1-gátló immunterápiák következtében közel 3%-ban fellépő neurológiai szövődmények. Nem megfeledkezve a kemoterápiák okozta polyneuropathiákról és a tüneti terápiaként alkalmazott antikonvulzív terápiás indikációkról.
1.
2.
3.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről4.
5.
1.
2.
Klinikai Onkológia
A rosszindulatú daganatok fenotípusának plaszticitása és az immunogén mimikri3.
Klinikai Onkológia
A szarkopénia mérése komputertomográfiával és jelentősége az onkológiai betegeknél4.
5.