Előrehaladott Parkinson-kór esetén a szájon át adható gyógyszeres kezelés gyakran nem éri el a kellő terápiás sikert. Az eszköztámogatott terápiás módszerek egyike, a levodopa intrajejunalis adagolása, értékes alternatívának bizonyult. A jól ismert intestinalis levodopapumpa egy modern változata lehetővé teszi a levodopa, karbidopa és entakapon orális hármas kombinációjának további alkalmazását, amellyel sok beteg már előzőleg kezelve volt. Ez, az entakapont is tartalmazó, modern kezelési lehetőség 2021. február óta érhető el Ausztriában és Németországban és a levodopadózis csökkentését is eredményezheti az intestinalis levodopadózishoz (LCIG) viszonyítva. A közeljövőben számos más országban, köztük Magyarországon is egyedi támogatással igényelhető. A pumpa és az intestinalis gélt tartalmazó patron lényegesen kisebb és könnyebb, mint az LCIG-pumpa, ami javítja a terápia elfogadottságát. Egy Svédországban végzett tanulmány a kisebb pumpa magasabb elfogadottsági arányról és felhasználóbarátabb kezelésről számolt be a betegek körében. Az entakapon esetlegesen fellépő nemkívánt mellékhatásait nem szabad a figyelmen kívül hagyni.
A levodopa intrajejunalis alkalmazása pumpával (levodopa-karbidopa intestinalis gél, LCIG) bevett kezelési lehetőség1, amennyiben a szájon át szedett gyógyszerekkel már nem lehet kellően egyenletes hatást elérni. Hosszú ideig csak egyfajta pumpa volt kereskedelmi forgalomban (LCIG/Duodopa®). Az LCIG levodopából és karbidopából (20 mg/5 mg/ml) álló gél, amelyet kazettában (100 ml) tárolnak, és gastrostomán keresztül a jejunumba fecskendeznek2. Ez az eljárás minimálisan invazív, melynek hatékonysága nasojejunalis szondával előzetesen tesztelhető3. A levodopadózis általában jelentősen magasabb az LCIG-pumpával, mint szájon át történő beadás esetén2, 4. Az LCIG hátránya, hogy a már levodopa/DDI/COMT-inhibitor kombinációval kezelt betegeket levodopa/DDI-re kell visszaállítani.
Az intrajejunalis levodopa (LCIG) alkalmazására vonatkozó evidenciák gyarapodtak az elmúlt években, egyrészt a hosszú távú tapasztalatoknak, másrészt egy kontrollált vizsgálatnak köszönhetően5, 6, 9. Az MDS (Movement Disorder Society) jelenlegi értékelése szerint az LCIG-t az előrehaladott stádiumú motoros szövődmények kezelésére ajánlják4. Ez a terápia azonban gastrointestinalis és helyi szövődményekkel, valamint ritka, de lehetséges axonalis neuropathiákkal és Guillain–Barré-szerű szindrómával járhat2, 6.
A levodopa intestinalis adagolása újabb, entakapont tartalmazó készítményben
A levodopa-entakapon-karbidopa intestinalis gél (LECIG) számos előnyt kínál az orális terápiákkal vagy az entakapon nélküli intestinalis terápiával szemben. A levodopa továbbra is a leghatékonyabb és legjobb gyógyszer a Parkinson-kór (PD) kezelésére. A levodopa toxicitásával kapcsolatos korábbi aggodalmakat nem sikerült kontrollált vizsgálatokban kimutatni. Az adatok azt mutatják, hogy a magas koncentrációjú levodopa az UPDRS-pontszám jelentős javulását eredményezi 40 hetes kezelés, majd egy ezt követő 2 hetes kimosási időszak után, az alacsonyabb dózisokhoz vagy a placebóhoz viszonyítva7. Ha közvetlenül a bélrendszerbe adagoljuk a levodopát, az előrehaladott parkinsonos betegnél elkerülhetők az orális adagolás tipikus problémái, így például a nyelési zavar, a késleltetett gyomorürülés és a levodopa felszívódási zavara fehérjében gazdag étrend miatt. A cél az állandó levodopaellátás biztosítása, ezáltal a megfelelő mobilitás elérése, valamint a dyskinesia elkerülése.
Egy randomizált kettős vak vizsgálat megerősíti az intestinalis adagolás nagyobb hatékonyságát az orális terápiához képest, lényegesen hosszabb on- és rövidebb off-fázisokkal8. Az entakaponnal való kombináció növeli a biológiai hozzáférhetőséget, ami lehetővé teszi a levodopa alacsonyabb dózisainak alkalmazását az entakapon nélküli LCIG-terápiához képest.
Figyelem: Azok a betegek, akiknél entakapon vagy tolkapon hatására hasmenés alakult ki, nem kezelhetők LECIG-gel. Ha a beteg korábban nem kapott entakapont vagy tolkapont, a hasmenés kialakulásának lehetőségével számolni kell. Az 1. táblázat bemutatja az LCIG- és a LECIG-pumpák és -patronok összehasonlítását.
1. táblázat. A pumpák és a patronok összehasonlítása

A LECIG alkalmazásával kapcsolatos tanulmányok áttekintése
Egy randomizált, nyílt, kétnapos keresztezett vizsgálatban 11, előrehaladott Parkinson-kórban szenvedő beteg kapott 14 órás infúziót LECIG-ből, illetve standard levodopa-karbidopa gélből (LCIG)9. Az LCIG szokásos reggeli adagja 80%-ának (n = 5) vagy 90%-ának (n = 6) megfelelő LECIG-dózisokat, illetve az LCIG fenntartó adagjának 80%-át és a kiegészítő adagok 80%-át alkalmazták. A levodopa biohasznosulása 14 órás infúzión keresztül a LECIG esetében körülbelül egyharmaddal volt magasabb, mint az LCIG esetében9, 10. A vizsgálat tehát azt mutatta, hogy csökkentett levodopadózissal összehasonlíthatóan hatékony stabil levodopa-plazmaszint érhető el. E tanulmány9 szerint az LCIG és a LECIG közvetlen összehasonlítása a levodopa adagjának 34%-os csökkentését eredményezi hasonló klinikai hatékonyság mellett, amelyet a hétlépcsős kezelési válasz skálával (Treatment Response Scale, TRS) értékeltek.
A 2017-es crossover vizsgálat9 adatai alapján további elemzéseket végeztek egy farmakokinetikai modell segítségével11. A kutatás célja az volt, hogy kiderítsék, melyik adagolási séma a legjobb, mivel a crossover vizsgálatban választott beállítások nem vezettek optimális eredményre. Az adagolási modellezésbe különböző tényezőket vontak be, például a felszívódási sebességet, a relatív biológiai hozzáférhetőséget, a centrális és perifériás megoszlási térfogatot, a látszólagos és a kompartmentek közötti clearance-t, valamint a testsúlyt és a táplálékbevitelt. Az 1000 adatsor/szimuláció elemzése alapján az LCIG-adag 100%-os reggeli adagja + az LCIG-adag 65%-ának megfelelő folyamatos fenntartó adag az LCIG-adag LECIG-re való átszámolásának lehető legoptimálisabb módja11.
Ezen túlmenően a levodopát lebontó enzimek genetikai enzimvariabilitásának hatását is vizsgálták, hogy kiderítsék, miért nem emelkedett minden betegnél ugyanolyan mértékben a levodopa plazmakoncentrációja. A katechol-O-metiltranszferáz és a dopa-dekarboxiláz vizsgált polimorfizmusai elméletileg magasabb és alacsonyabb enzimaktivitáshoz vezethetnek. Az értékelés azonban nem mutatott egyértelmű kapcsolatot a betegek genetikai változatai és a farmakokinetika között. A szerzők a korlátozott adathalmaz alapján azt feltételezték, hogy az enzimstátusz nem játszik szerepet a LECIG-re való beállításban, különösen azért, mert minden egyes betegnél egyénileg titrálják ki a szükséges dózist11.
A Lecigon® svédországi engedélyezését követően Dag Nyholm kutatócsoportja megfigyeléses vizsgálatot végzett12. A vizsgálat középpontjában a terápia hatékonysága és biztonságossága, valamint a pumpa felhasználóbarát volta állt. Huszonnégy beteg (köztük 11 nő) 72 éves medián életkorral és 16 éves medián betegségtartammal átlagosan 7,0 ml (140 mg) levodopát kapott reggeli adagként, 2,5 ml/h folyamatos dózissal (50 mg/h) és 1,0 ml (20 mg) extra adagot egy 305 napos medián megfigyelési időszak alatt. A betegek felét közvetlenül LCIG-ről LECIG-kezelésre váltották; a korábbi LCIG-dózis alapján a reggeli adag 100%-át, a fenntartó adag 76%-át és az extra adag átlagosan 92%-át adták be. Öt beteg hagyta abba a LECIG-t, három hasmenés miatt (valószínűleg entakapon okozta). A többi beteg elégedett volt; a legtöbbjük örült a LECIG-pumpa méretének és súlyának. A szerzők arra a következtetésre jutottak, hogy a LECIG alkalmas hosszú távú terápiára, az LCIG-hez hasonló hatékonysággal és az orális levodopa/karbidopa/entakaponhoz hasonló biztonságossággal rendelkezik12.
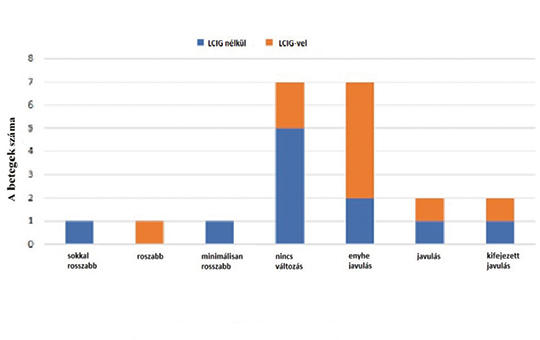
A klinikai globális javulás kérdőívben a korábban pumpás kezelésben nem részesült betegek 70%-a (n = 10) számolt be a Parkinson-kór tüneteinek javulásáról.
1. ábra. A betegek értékelése a LECIG-terápia általi parkinsontünetek javulására vonatkozóan
(n=21)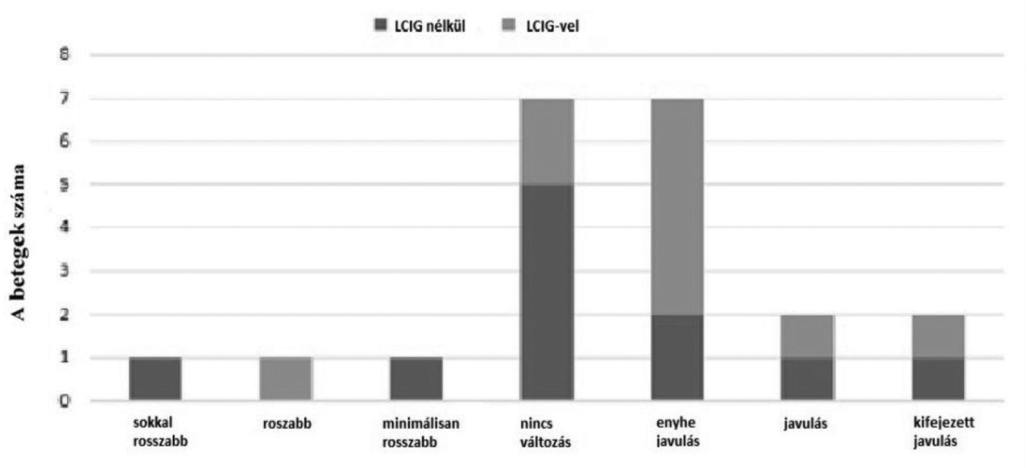
A korábban LCIG-terápiával rendelkező betegek többsége javulást tapasztalt a felhasználóbarát kezelés és a patroncsere tekintetében. Minden beteg jelentős javulást észlelt a pumpa méretét illetően.
2. ábra. Az LCIG-ről LECIG-re váltott betegek pumpajellemzőinek összehasonlítása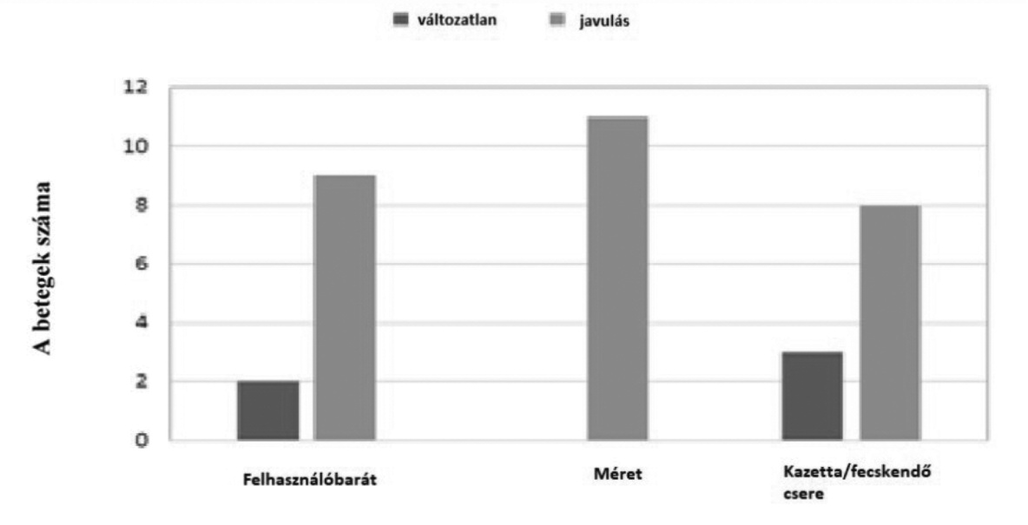
3. ábra. Pumpaalkalmazás
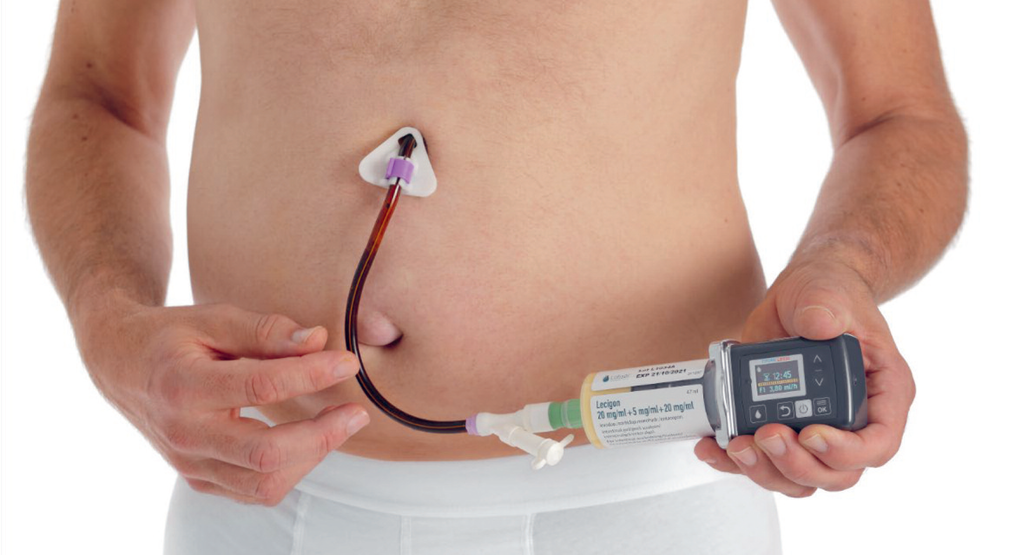
A LECIG még a hosszabb kezelési időszak alatt is általában jól tolerálható. A teljes időszak alatt hét betegnél jelentkeztek mellékhatások, amelyek négy betegnél a terápia megszakításához vezettek (három betegnél hasmenés, egy betegnél hallucinációk miatt). A vizsgálócsoport úgy döntött, hogy megengedik az esetlegesen entakaponnal összefüggően jelentkező hasmenéssel küzdő betegeknek a LECIG-pumpa kipróbálását, hogy lássák, számít-e az adagolás módja. Úgy tűnik, hogy az entakapon szájon át vagy bélrendszeri úton történő alkalmazástól függetlenül hasmenést okoz. Összesen három beteg hunyt el (egy beteg Covid-19, egy beteg szívroham következtében, egy beteg a használat abbahagyása után).
A szerzők arra a következtetésre jutottak, hogy a LECIG-terápia általában jól tolerálható, és hosszú távon is alkalmazható. Ezen túlmenően a betegek által jelzett hatékonysága is jó. Az új módszer jó felhasználóbarátságot mutat, és a betegek általában elégedettek a pumpa méretével, bár indokolt a szoftver további technikai fejlesztése12.
Következtetések
A levodopa intrajejunalis beadása hasznos kezelési lehetőség előrehaladott Parkinson-kórban. Eddig csak egy szolgáltató kínált levodopagélt, amelyet PEG-J-n keresztül pumpa segítségével juttattak a jejunumba. Ez folyamatos levodopaadagolást tesz lehetővé közvetlenül a jejunumba, ami állandó levodopaszintet tart fenn a szérumban. 2021 februárja óta Németországban és néhány más európai országban egy másik, eltérő típusú pumpával működő készítmény is elérhető. Ez az eljárás körülbelül egyharmadával csökkentheti a levodopa szükséges adagját. A pumpa kisebb, könnyebb és csendesebb. Az entakapon hozzáadásával hasmenés léphet fel, amire mindenképpen figyelni kell.









HOZZÁSZÓLÁSOK
0 hozzászólás