Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 125
Hírvilág
2021. AUGUSZTUS 24.
hirdetés
A TAGRISSO TM ▼ megkapta az Európai Gyógyszerügynökség (EMA) jóváhagyását a korai stádiumú, EGFR-mutációt hordozó, nem kissejtes tüdőrákban szenvedő betegek adjuváns kezelésére
A jóváhagyás a III. fázisú ADAURA vizsgálat eredményei alapján történt, ahol a TAGRISSO-kezelés 80%-kal csökkentette a halálozás, illetve a betegség kiújulásának relatív kockázatát.
Az onkológiai biológiai kezelések és a magas vérnyomás kapcsolatának elemzése
A biológiai gyógyszerekkel kombinált kemoterápia valódi áttörést jelent a lokálisan előrehaladott és metasztatikus daganatos betegek hatékony kezelésében. Az angiogenezis-gátlás egyik leggyakoribb és klinikailag jelentős mellékhatása a magas vérnyomás kialakulása. Az összefoglaló cikknek az a célja, hogy elemezze a vascularis endothelialis növekedési faktor jelátviteli útvonal gátlói és a magas vérnyomás közötti kapcsolatot. Áttekintjük a VEGF/VEGFR gátlók által kiváltott magas vérnyomás előfordulását, kialakulásának mechanizmusait, a vérnyomásértékek rendszeres ellenőrzésének fontosságát, a lehetséges kezelési stratégiákat és a profilaktikus vérnyomáscsökkentő kezelés hatékonyságát. Összehasonlítjuk a klinikai vizsgálatok eredményeit, hogy tisztázzuk az antiangiogén-kezelés során bekövetkező vérnyomás-emelkedés prognosztikai és prediktív jelentőségét. A biológiai kezelés és a magas vérnyomás közötti kapcsolat további kutatása hatékonyabb, hosszabb túléléssel és jobb életminőséggel járó kezelést eredményezhet az előrehaladott daganatos betegekben.
Nivolumab+kemoterápia vagy nivolumab+ipilimumab kombináció gastrooesophagealis rákban
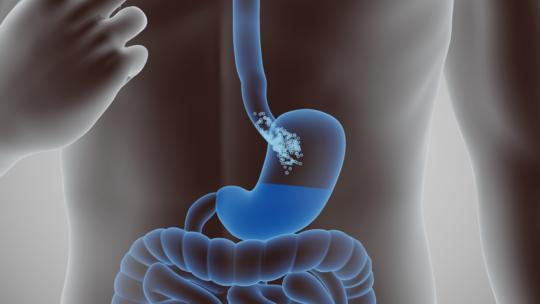
A standard első vonalbeli kemoterápia a humán epidermalis növekedési faktor receptor 2 negatív (HER2)-vel nem rendelkező gastrooesophagealis adenocarcinomában szenvedő betegek többségénél egy éven belül a betegség progressziójához és halálhoz vezet. A nivolumab+kemoterápia a 12 hónapos követés során a kemoterápiához képest jobb általános túlélést mutatott.
Ökológia
2022. JÚLIUS 21.
Ehető vadon élő gombák: egészséges táplálékforrások és ígéretes gyógyászati lehetőségek
Számos, gombákból izolált vegyület kiemelkedően kedvező gyógyászati hatásokkal bír. Ezek az összetevők, köztük lektinek, poliszacharidok, poliszacharid-peptinek és poliszacharid-fehérje komplexek igen hatásosnak bizonyultak: immunmoduláns, daganatellenes, gyulladáscsökkentő és antioxidáns hatásokat is kiváltanak, és csökkentik a vér koleszterinszintet. A gombák szárazanyag-tartalma meglehetősen alacsony, pontos mértékét a gomba faja, a betakarítási, növekedési és tárolási körülmények mind befolyásolják. Általában a szárazanyag-tartalom legnagyobb részét szénhidrátok teszik ki, de jelentős mennyiségű fehérjét is tartalmaz, valamint ásványi anyagokat és kevés zsírt. Szénhidrátok közül a keményítő nincs jelen, a poliszacharid-raktárként a gombák egy részénél glikogén funkcionál. Jellemző a glükóz, mannitol és trehalóz. A gombák sejtfalát körülbelül 80%-ban kitevő kitin korlátozza más gomba-összetevők elérhetőségét, és emészthetetlen számunkra. Az élelmi rostok szintén jelentős mennyiségben vannak jelen. A β-glükánok fontos funkcionális összetevők, képesek immunszabályozó hatást kiváltani, befolyásolják a humorális és celluláris immunitást.
Gondolat
2022. JÚNIUS 23.
Lehet-e tudatos a micélium?
A Fungal Biology folyóiratban megjelent Hyphal and mycelial consciousness: the concept of the fungal mind című közlemény szerzője rávilágít, tudományos berkekben mennyire égető szükségünk van az intelligencia és a tudatosság fogalmainak felülvizsgálatára. Arthur Reber sejtszintű tudatosság elmélete szerint az intelligencia nem tekinthető emberi privilégiumnak. Az intelligencia inkább egy skálázható kvalitás, amely alacsonyabb vagy magasabb komplexitásban, de számos organizmuson megfigyelhető.
Hogyan viszonyul az immunrendszer a rosszindulatú daganatokhoz?
Az immunrendszer a halmozott szomatikus mutációk következtében kialakult rosszindulatú daganatok antigénjeit (TSA) ismeri fel és a transzformálódott sejteket elpusztítja. Az immunrendszer, hálózat jellegénél fogva, egyszerre több, egymást kiegészítő mechanizmussal lép fel a daganatsejtek ellen. A TSA-k mellett, a mutációk következtében, aktiválódhatnak olyan génszekvenciák is, amelyek az adott életkorban már szerepet nem játszó szöveti hormonokat, növekedési és differenciálódási faktorokat kódolnak. Ezeket, az adott daganatszövetre jellegzetes biomolekulákat nevezzük tumorasszociált antigéneknek (TAA) vagy a klinikai gyakorlatban tumormarkereknek. A TAA-k meghatározása segíti a differenciáldiagnózist, illetve a terápiás hatékonyság monitorozását, de nem alkalmas tömeges szűrővizsgálatokra, mert nem minden daganat expresszál TAA-kat és nemcsak a daganatos elváltozásokban, hanem például gyulladásos állapotokban is termelődhetnek. Általában egy hosszabb ideig tartó egyensúlyi állapotot követően, amikor az immunrendszer már nem tudja az összes daganatsejtet elpusztítani – a fokozott mutációk következtében –, a daganatsejtek megszökhetnek a felügyelet alól és kialakul a klinikai tüneteket okozó rosszindulatú daganat. Az immunterápiák célja az immunválasz mechanizmusainak felhasználásával ismét érzékennyé tenni a rosszindulatú daganat sejtjeit a támadó effektor immunfunkciókra.
Hálózati inverz fertőzési modellek a járványterjedés vizsgálatában
Az egyre növekvő COVID-19 világjárvány közben a világ számos tudósa és kutatócsoportja fáradozik a vírus terjedésének minél pontosabb megértésén, hogy hatékonyabb beavatkozási módszereket dolgozzanak ki a legfőbb döntéshozók számára a terjedés enyhítésében, illetve megállításában. A legfontosabb kutatási területek a fertőzésterjedés modellezése, a fertőzöttség gyors és pontos kimutatása, lehetséges védőoltások és gyógykezelések kifejlesztése, illetve a járvány társadalmi- és gazdasági hatásainak vizsgálata.
A kezelések sorrendje áttétes colorectalis rákban
Az áttétes colorectalis rák (mCRC) a legtöbb esetben gyógyíthatatlan állapot, de a beteg élettartama a korszerű kemoterápiás és célzott gyógyszeres kezelésekkel meghosszabbítható. Ugyanakkor nem teljesen tisztázott, hogy ezeket a gyógyszereket a kezelés különböző vonalaiban milyen optimális sorrendben kellene használni. A tanulmányban számba veszik a jelenleg rendelkezésre álló kezeléseket és az optimális kezelési sorrendet az mCRC első, második és harmadik választású ellátása során, de érintik a kezelési sorrendet és a kezelések átértékelését befolyásoló biológiai aspektusokat is. A hatásos első vonalú kezelés kulcsszerepet játszik a betegség végső kimenetelének alakulásában, ezért a különböző klinikai faktorok és biológiai markerek – mint a RAS és a BRAF – ismeretében kell azt megválasztani. A második vonalban alkalmazandó kezelés az első vonalban adott szisztémás kezeléstől függ. A legtöbb betegnél antiangiogén kezelések (például bevacizumab, ramucirumab és afl ibercept) bevezetése is indokolt, míg az epidermalis növekedési faktor receptor (EGFR-) gátlás alkalmazása a második vonalban nem hosszabbítja meg az élettartamot. Harmadik vonalban nagyon fontos a molekuláris profil ismerete, a vad típusú RAS-t mutató daganatos betegeknél EGFR-gátlókat (cetuximab vagy panitumumab) tartalmazó regorafenib és trifl uridin/tipiracil kezelést alkalmaznak. A pembrolizumabbal vagy nivolumabbal ± ipilimumabbal végzett immunkezelést szükséges megfontolni a magas mikroszatellita-instabilitást mutató betegségben. A HER2/neu amplifikációt megcélzó kezelések sikeresek lehetnek az ilyen abnormitást mutató colorectalis tumoros esetekben. A kezelések sorrendjének eldöntését tovább bonyolítják a kezeléseknek a daganatos progresszió eltérő jellege miatt szükségessé vált megszakításai vagy beszűkítései. Jelenleg is vizsgálják mCRC-s betegeken a kezelések optimális sorrendjét és azok optimális ütemezését. A molekuláris profilok megismerésével új targeteket lehet kijelölni, ráadásul egyre jobban kezdjük megérteni a daganatoknak a gyógyszerhatások alatt bekövetkező folyamatait, amelyek végül befolyásolhatják a kezelési sorrendet is.
Szérumhúgysavszint hypertoniában. Hazai tapasztalatok a Magyar Hypertonia Regiszter 2011., 2013., 2015. évi adatai alapján - I. rész Bevezető gondolatok. Betegek és módszer. Alapadatok
Világszerte az általános populációban végzett szűrések alapján észlelik a szérumhúgysavszint átlagának emelkedését mindkét nemben. Ez a növekedési tendencia érvényes a hypertoniabetegségre is. A szerzők a Magyar Hypertonia Regiszter 2011., 2013. és 2015. évi adatainak felhasználásával vizsgálták 47372 hypertoniás betegben (22688 férfi, 24684 nő) a szérumhúgysavszint alakulását és összefüggését az életkorral, kockázati tényezőkkel, antropológiai, metabolikus jellemzőkkel, vérnyomással, a vérnyomáscélértékkel, szervkárosodásokkal, gyógyszeres kezeléssel, valamint a társbetegségekkel. Elemzésük első részében bemutatják az elemzés módszerét és az alapösszefüggéseket. A húgysavszint magasabb férfiaknál, mint nőknél, a kor előrehaladásával értéke emelkedik. A szisztolés és diasztolés vérnyomás emelkedése a szérumhúgysavszint növekedésével jár, amelynek trendje a szisztolés nyomás esetében szignifikánsan nagyobb. A hölgyeknél az emelkedési trend kisebb és mindig alacsonyabbak a húgysavértékek. Azoknál, akik nem érik el a célvérnyomást, a húgysavérték magasabb. A társbetegségek jelenléte szignifikánsan növeli a szérumhúgysavszintet.
A stroma szerepe a rosszindulatú daganatok viselkedésében
A daganatok stromáját hosszú időn át úgy tekintették, mint ártatlan mellékszereplőt, ami nem befolyásolja a tumorok biológiai viselkedését. Ez a nézet az elmúlt 20 évben jelentősen megváltozott. Ismereteink gazdagodásával bebizonyosodott, hogy a stroma minden egyes sejtes eleme és alapállománya is aktív résztvevő a daganat kialakulásában és progressziójában. A kezdetben védőszerepet is játszó stromát a daganatsejtek gyorsan saját szolgálatukba állítják. Gyakorlatilag nincs olyan stromalis komponens, amely ne befolyásolná a rosszindulatú daganatok viselkedését. Ez lehet a daganatsejtek proliferációjának, inváziójának serkentése a stroma merevségének növelésével, energiatermelés a tumorsejtek számára, citokinek, növekedési faktorok előállítása és prezentációja, a daganatok vérellátása. Ez a felismerés vezetett új típusú, a daganatos neostroma komponenseinek gátlását célzó terápiák tervezéséhez. Ezek közül a legsikeresebb az immun- és az angiogenezist gátló terápia, de számos más target gátlására is folyamatos próbálkozások tanúi lehetünk.
1.
2.
3.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről4.
5.
1.
2.
Klinikai Onkológia
A rosszindulatú daganatok fenotípusának plaszticitása és az immunogén mimikri3.
Klinikai Onkológia
A szarkopénia mérése komputertomográfiával és jelentősége az onkológiai betegeknél4.
5.