Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 33
A vesecarcinoma első vonalas kezelésének lehetőségei, korai tapasztalatok az immun-immun kombinációval
Az előrehaladott és áttétes vesedaganatok kezelése az onkológia dinamikusan változó területe. Az első célzott terápiás készítmény törzskönyvezése óta (2005) szinte évente került sor újabb és újabb készítmények regisztrálására. Az immunellenőrzőpont-gátlók kifejlesztése és az ellátási algoritmusokba való illesztése (2015) tovább bővítette a terápiás palettát. Mindezek ellenére a különböző terápiás vonalakban alkalmazott készítmények kiválasztása sokszor kihívás elé állítja a klinikusokat. A cikkben az első vonalbeli kezelések kerültek összefoglalásra.
Út a szívhez a vesén át. A residualis cardiovascularis rizikó csökkentésének újabb távlatai – a mesodermalis eredetű szervek kommunikációs útvonalai és mediátorai
A cardiovascularis betegségek továbbra is magas morbiditási adatai a ”maradék” rizikótényezők feltárását indokolják. Az embrionális fejlődés folyamán a cardiovascularis szervek a mesodermából fejlődnek ki, a sejtvonalak között fennmaradó humorális és mechanikus kommunikáció részben magyarázatot ad a maradék cardiovascularis rizikó jelenségére, részben pedig új terápiás célpontok körvonalazódásához vezet.
Az autoszomális domináns policisztás vesebetegség és a tolvaptankezelés
Az autoszomális domináns policisztás vesebetegség a leggyakoribb öröklődő vesebetegség, amely a végstádiumú vesebetegségek 5-10%-áért tehető felelőssé. Kialakulását elsősorban a policisztint kódoló gének hibája okozza, amely több jelátviteli úton keresztül fokozott folyadéktranszportot, proliferációt, végső soron a ciszták képződését eredményezi. A diagnózis elsődlegesen az ultrahangos képen és családi anamnézisen alapul. Genetikai meghatározásra csak atípusos formákban van szükség. A klinikumra jellemző a hypertonia, haematuria, proteinuria, a progresszíven csökkenő GFR-szint, illetve az extrarenalis manifesztációk – mint a májciszták, agyi aneurysmák, különböző szívbillentyűhibák jelenléte. Nehézséget a differenciáldiagnosztika során elsősorban a többi cisztás vesebetegségtől való elkülönítése jelent. A terápia megtervezése komplex szemléletmódot igényel, amiben alapvető a progresszió sebességének meghatározása. Ebben segítségünkre lehet a Mayo-klasszifikáció, amely a veseméret alapján prognosztizálja a betegséget, illetve a PROPKD-score, amely a klinikumot és a genetikát is figyelembe veszi. A terápiát eddig elsősorban az életmódváltás, a sószegény diéta, a hypertonia kezelése uralta. 2016 óta rendelkezésünkre áll a vazopresszin-2-receptor-gátló tolvaptan, amely különböző vizsgálatokban (TEMPO 3:3; TEMPO 3:4; REPRISE) a veseméret növekedésének, illetve a GFR-vesztés mértékének lassulását okozta. Összefoglaló közleményünkben a patogenezis és klinikum áttekintése mellett a legújabb terápiás ajánlás legfontosabb pontjait ismertetjük. A kutatási eredmények alapján a jövőben egyéb jelátviteli útvonalak befolyásolásával újabb terápiás lehetőségek állhatnak majd rendelkezésünkre, mint a szomatosztatinanalógok, az EGFR-gátlók és az mTOR-gátlók.
Az artériás életkor meghatározásának klinikai jelentősége
Az artériás öregedés, az emberi szervezet idősödésével együtt járó folyamat, egy adott egyén kronológiai életkorához képest az artériás életkora eltérő lehet. Ennek hátterében genetikai tényezők és számos rizikófaktor hatása áll. Annak ellenére, hogy a kockázatbecslési kalkulátorok nélkülözhetetlenek a prevenciós stratégiák megvalósításában, különbségeket tapasztalhatunk az előre jelzett és a valóban bekövetkező események számában.
Az emberi agy feltáratlan GnRH-neuronrendszere
A szaporodás agyi szabályozásáért felelős gonadotropin-releasing hormont (GnRH) a legtöbb emlős fajban mindössze ~2000 idegsejt termeli és választja el neuroszekréció útján az agyalapi mirigy portalis keringési rendszerébe. Míg laboratóriumi rágcsálókban GnRH-idegsejtek kizárólag a preoptikus agyterületen helyezkednek el, post mortem emberi agyon végzett immunhisztokémiai megfigyeléseink GnRH-termelő neuronok bőséges előfordulását mutatták hypothalamuson kívüli agyterületeken is. Munkánk célja az extrahypothalamicus GnRH-idegsejtek karakterizálása volt.
A pajzsmirigyhormon-háztartás idegrendszeri szabályozása hypothyreosis T4-monoterápiája során
A pajzsmirigyhormonok a sejtműködés alapvető fontosságú szabályozói, hatásuk szinte minden szervrendszerben tetten érhető. Az idegrendszer fejlődése és működése is nagymértékben függ a pajzsmirigyhomon-jelátvitel megfelelő szintjétől. A pajzsmirigyhomon-háztartás egyik fő szabályozó köre a hypothalamus-hypophysis-pajzsmirigy tengely, ami elsősorban a vér keringő pajzsmirigyhomon szintjére képes hatni. Az egyes szövetek pajzsmirigyormon elérhetőségeit viszont egy sejttípus-specifikus, összetett szabályozórendszer állítja be az adott sejt/szövet adott pillanatban szükséges igényeinek megfelelően.
A célzott kezelések „célzott” mellékhatásai
A célzott gyógyszerek nem elég célzottak, gyakran a normális gének termékeire is hatnak, vagy nem elég szelektívek a mutáns változatokra, így egyáltalán nem elhanyagolható és sajátos mellékhatásaik vannak, aminek patomechanizmusát érdemes ismerni, mert általa a mellékhatások megelőzése vagy „célzott” kezelése lehetséges. Miután a célzott kezelések molekuláris mechanizmusai igen eltérők, ezen mellékhatások spektruma is széles és nagyon eltérő a hagyományos kemoterápiás szerekhez hasonlítva. Az angiogenezisgátlók mellékhatásai a VEGF-mediált folyamatok zavarai (vérzés, sebgyógyulás, vérnyomás-szabályozás), a csontáttét kezelésében használt szerek csontregenerációs zavarokhoz vezetnek az osteoclastfunkció blokkolásával, a HER-2-gátlók szelektív szívizom-károsítók lehetnek, mert ez a receptor kulcsfontosságú az izomregenerációban. Mivel az EGFR a felszíni hám folyamatos megújulásának fő szabályozója, az anti-EGFR-szerek bőrmellékhatásai csaknem természetesek. A multikináz-inhibitorok két fontos célpontja a csontvelő (a KIT kulcsszerepe miatt), illetve a melanocita (hasonló okokból). Az új TRK-inhibitorok esetében idegrendszeri mellékhatások léptek fel, miután az idegsejtek fontos szabályozója az NTRK. A mutáns BRAF-inhibitorok, sajnos, csak szelektívek, és alkalmazásuk során másodlagos, elsősorban RAS-mutáns daganatok keletkezése várható a RAS-RAF-MEK jelpálya sajátos visszacsatolási reakciói eredményeként. A lipidkináz-jelpálya különböző inhibitorai (PI3K, AKT vagy mTOR) megint csak jellegzetes mellékhatásokkal járnak, mint a hyperglykaemia vagy a hyperlipidaemia. Végül az immunellenőrzőpont-gátlók a daganatellenes immunválasz felszabadítása mellett, eddig kontroll alatt levő autoimmun mechanizmusokat is aktiválnak, amelyek adott esetben súlyosak is lehetnek vagy eddig még nem ismert formában manifesztálódnak (hypophysitis).
Terápiás megközelítés és új evidenciák a neuromyelitis optica spektrum kezelésében
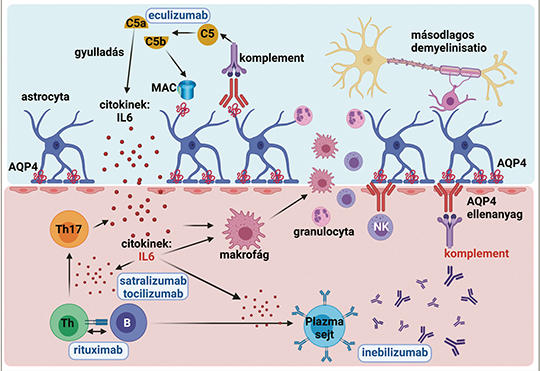
A neuromyelitis optica spektrum betegség (NMOSD) az esetek körülbelül 80%-ában AQP4-ellenanyaggal társul. A szeronegatív betegek körülbelül negyedében a központi idegrendszeri myelin oligodendrocyta glikoprotein (MOG) ellen mutatható ki ellenanyag, és ez a kórkép a MOG-ellenanyag-asszociált betegség (MOGAD) elnevezést kapta. Jelen közlemény áttekinti az off-label azathioprin és mycophenolat mofetil, valamint az evidenciákon alapuló B- és plazmasejt-depletio, az IL-6-jelátvitel és a komplement útvonal antagonizálás klinikai aspektusait NMOSD-ben. Az összefoglaló tárgyalja az NMOSD-terápia terhességi vonatkozásait, és a MOGAD – NMOSD-től eltérő – kezelési megközelítését. Az NMOSD kezelése kapcsán az utóbbi két évben több, III. fázisú klinikai tanulmányon alapuló I. osztályú evidencia jelent meg. A monoklonális ellenanyagokkal végzett vizsgálatok a rituximab (anti-CD20), az inebilizumab (anti-CD19), a tocilizumab (anti-IL6R), a satralizumab (anti-IL6R) és az eculizumab (anti-C5) hatékonyságát és biztonságosságát jelzik egyéb immunterápiákkal kombinálva vagy monoterápiában. A MOGAD kezelését bonyolítja, hogy az esetek körülbelül fele monofázisos, és a MOG ellenanyag a betegség lefolyása során spontán vagy kezelés hatására eltűnhet. A tartós immunszuppresszió igényét MOGAD-ban a relapsusterápiát követő, leépített orális szteroidkezelés után célszerű eldönteni. NMOSD-ben a fenntartó terápia folytatása javasolt terhesség és szoptatás alatt is, és ezt az optimális kezelés kiválasztásánál fertilis nőbetegeknél figyelembe kell venni. Az új evidenciák terápiarezisztens NMOSD-ben is több lehetőséget kínálnak, és a MOGAD kezelési stratégiája is körvonalazódik.
A prolaktin a CGRP interakciója migrénben
Régóta ismert tény, hogy a migrén gyakoribb nőkben, mint férfiakban. Noha a jelenség pontos háttere nem ismert, egyre több adat utal arra, hogy a nem specifikus hormonszintek fontos szereplői lehetnek a történetnek. Például az agyalapi mirigy által kiválasztott prolaktin, melynek szintjét a gonadalis hormonok szabályozzák, a calcitonin gene-related peptide-del (CGRP-vel) interakcióba lépve fokozza annak migrént kiváltó hatását, állítja Avona és munkatársainak az Annals of Neurology-ben megjelent cikke.
1.
2.
3.
4.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről5.
1.
2.
Klinikai Onkológia
A rosszindulatú daganatok fenotípusának plaszticitása és az immunogén mimikri3.
Klinikai Onkológia
A szarkopénia mérése komputertomográfiával és jelentősége az onkológiai betegeknél4.
5.