Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 192
„Aki erre a pályára jön, elhivatottnak kell lennie”. Életútinterjú Farsang Csaba professzor úrral
Farsang Csaba professzor úrral a Szent Imre Kórház-beli dolgozószobájában beszélgettünk szakmai és privát életútjáról egy különleges főszerkesztői találkozón, amelyen a LAM jelenlegi aktív főszerkesztői, Kapócs Gábor és Benczúr Béla kérdezték a nagy elődöt, a LAM professor emeritusát.
Ökológia
2022. SZEPTEMBER 07.
A környezet, az emberi mikrobióta és az immunrendszer
Nem kérdés, hogy a baktériumok – és más mikroorganizmusok – rendkívül fontosak az emberi egészség szempontjából. Az azonban, hogy a természeti környezettel és annak egyes elemeivel való érintkezés pontosan hogyan befolyásolja a mikrobiótánkat és ezzel az egészségünket, kevéssé ismert. A Science of the Total Environment című szaklapban megjelent tanulmány, az Interplay between natural environment, human microbiota and immune system: A scoping review of interventions and future perspectives towards allergy prevention szerzői felkutatták és áttekintették azokat a tudományos publikációkat, amelyek ezzel kapcsolatban különféle kísérleti beavatkozások hatásait vizsgálták.
Idegtudományok
2022. JÚLIUS 23.
Új eredmények a neuroimmunológia területéről
Bár még gyerekcipőben jár az ideg- és az immunrendszer közötti kapcsolatok feltárása, a neuroimmunológia az elmúlt pár évben nemcsak a mikroglia-, T- és makrofágsejtek agyi szerepét, valamint az agy saját limfatikus rendszerét kezdi megismerni, de azokról az útvonalakról is kezd lehullani a lepel, amelyek révén a pozitív érzelmek lassítják a tumornövekedést vagy a negatív érzelmek pszichoszomatikus betegségeket okoznak.
Agresszív lefolyású akut sclerosis multiplexes beteg sikeres kombinált (plazmaferézis és alemtuzumab) kezelése
A sclerosis multiplex (SM) diagnosztikus és terápiás protokollja az utóbbi 3-4 évben jelentősen megváltozott. Az ECTRIMS 2020-ban közölt ajánlása meghatározta a magas betegségaktivitású SM -enotípus nomenklatúráját, diagnosztikus és terápiás protokollját. Ezt a fenotípust az ECTRIMS 2020 „agresszív SM”-ként definiálja, mely kórformát gyakori, súlyos relapszusok, rapid progresszió, magas gyulladásos és neurodegeneratív aktivitás jellemez.
HHV-6-asszociált rhombencephalitis. Egy ritka herpeses encephalitiseset sikeres kezelése
A humán herpesvírus-6 (HHV-6) egy elterjedt neurotropikus vírus. A primér fertőzés általában gyerekkorban következik be, tünetmentesen vagy enyhe tünetekkel. A vírus látens formában a mononuclearis sejtekben, részben az agyszövetben perzisztál. A HHV-6 reaktiválódása ritka, amit főként immunszuppresszió esetén, általában haemopoeticus őssejt-transzplantációt követően figyeltek meg. A vírus reaktiválódása encephalitist okozhat, ami súlyos, általában jelentős maradványtünetekkel gyógyuló kórkép.
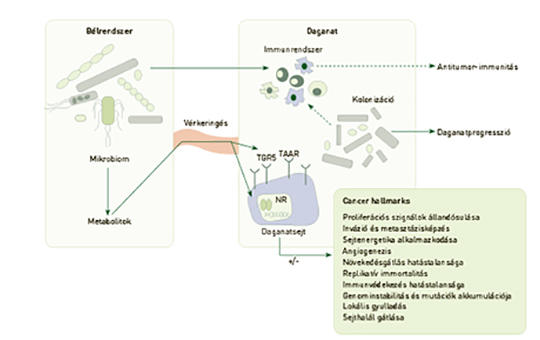
A mikrobiom és a rák
Az emberi szervezet legtöbb szerve és kompartmentje nem steril, ezekben új generációs szekvenálási eljárásokkal bakteriális DNS vagy RNS mutatható ki. Az egy adott kompartmentben kimutatható baktérium örökítőanyag összességét metagenomnak, a transzkriptek összességét metatranszkriptomnak, a baktériumok összességét pedig mikrobiomnak nevezzük. A mikrobiom összetétele megváltozik neoplasztikus betegségekben, amit onkobiózisnak nevezünk, az így kialakult fajösszetételt pedig onkobiomnak. A daganatok jelentős része kolonizálódik, és a daganatokban található baktériumok elősegítik a daganat növekedését, illetve fejlődését. A daganattól távoli kompartmentek (például bél) is áteshetnek onkobiotikus transzformáción. A bélmikrobiom onkobiotikus transzformációja során csökken a bélmikrobiom metabolikus kapacitása és több citosztatikus bakteriális metabolit szintézise lecsökken, ami a daganatsejtek proliferációjához és a metasztázisok képződéséhez vezet. A bélmikrobiom immunológiai tulajdonságai alapvetően meghatározzák azt, hogy az immunrendszer mennyiben tolerogén a daganatsejtekkel szemben, így elsődleges a daganatimmunitás szempontjából. Az onkobiózis önmagában nem indukál daganatokat, azonban elősegítheti növekedésüket és metasztázisképző képességüket. A baktériumoknak fontos szerepe van az antineoplasztikus terápia sikerességében, illetve a mellékhatások kialakításában.
Idegtudományok
2021. NOVEMBER 11.
Klinikai döntéshozatal MOG antitest-asszociált betegségben
A szenzitív és specifikus sejtalapú esszék kifejlesztésével a humán myelin-oligodendrocyta glikoprotein (MOG) ellenes IgG-antitestek kimutatása lehetővé tette az anti-MOG antitest-asszociált betegség (anti-MOG antibody-associated disease, MOGAD) és az egyéb demyelinisatiós betegségek elkülönítését. A MOGAD, az aquaporin-4-asszociált neuromyelitis optica spektrum betegség (AQP4-NMOSD) és a sclerosis multiplex (SM) megkülönböztetését a betegségek különböző kórélettani háttere, klinikuma, terápiás és prognosztikus következményei egyaránt indokolják.
Neuropszichiátriai lupus (NPSLE) bemutatása egy fiatal nő esete kapcsán
Bevezetés: Szisztémás lupus erythematosusban (SLE) az esetek 60%-ában észlelhetők idegrendszeri tünetek, melyek akár megelőzhetik, illetve kísérhetik vagy követhetik is a betegség diagnózisának felállítását. Az SLE-ben egyidejűleg jelentkező centrális és perifériás idegrendszeri tünetek differenciáldiagnosztikai kihívást jelenthetnek. Egy 23 éves nőbeteg kórtörténetén keresztül szeretnénk ismertetni a betegségben megjelenő neuropszichiátriai szövődményeket (NPSLE). Esetismertetés: Betegünk több hónapja fennálló, időnként jelentkező, 2-3 napig tartó fejfájás és enyhe kognitív zavar miatt jelentkezett neurológiai szakrendelésünkön. Felvételét megelőzően körülbelül 1 hónappal belgyógyászati osztályon kezelték mélyvénás thrombosis miatt, ekkor orális antikoaguláns terápia került beállításra. Az akutan elvégzett koponya-CT-vizsgálat (venográfia) panaszait magyarázó eltérést nem igazolt. Kezdetben migrénre gyanakodtunk, azonban a koponya-MRI-n látott elváltozások (microangiopathia, kisérvasculitisre utaló jelek) szisztémás autoimmun betegség lehetőségét vetették fel, ezért a beteget immunológiai centrumba utaltuk. Az ott elvégzett vizsgálatok – az érvényben lévő kritériumrendszer alapján – egyértelműen igazolták az SLE-t. A hetente 4 alkalommal alkalmazott chloroquinkezelés mellett a beteg állapota stabilizálódott, fejfájása, kognitív zavara megszűnt. Következtetés: Az általunk ismertetett – az ARC-kritériumok alapján is definitíven igazolt –, lupusban szen- vedő betegünk esete jól szemlélteti az SLE-ben elsőként megjelenő neuropszichiátriai tüneteket, és jó példa arra, hogy egy szisztémás autoimmun betegség szervi manifesztációjának tünetei akár meg is előzhetik a betegség diagnózisának felállítását.
Immun-neuropathiák útvesztői a gyakorlatban: a krónikus gyulladásos demyelinisatiós neuropathiától (CIDP) az anti-MAG neuropathiáig
Immunológiai ismereteink bővülésével és az új antitestek felfedezésével a neuroimmunológiai kórképek száma nő. Nem kivétel ez alól a perifériás neuropathiák csoportja sem, diagnosztikai és terápiás kihívás elé állítva a betegcsoporttal foglalkozó kollégákat. Esetbemutatásunk révén, anti-MAG neuropathiás betegünkkel kapcsolatos diagnosztikus és terápiás nehézségeink, valamint a társuló, egyelőre cryptogen strokeesemények okozta kihívások ismertetésén keresztül szeretnénk rávilágítani a perifériás gyulladásos neuropathiás megbetegedések komplexitására. A pár hónapja fennálló, alsó végtagi distalis paraesthesiákkal jelentkező fiatal férfi neurofiziológiai vizsgálata során alsó végtagi szenzomotoros demyelinisatiós neuropathiára utaló képet láttunk. Az ismert antitestek vizsgálata nem hozott pozitív eredményt, a rutin liquorvizsgálat emelkedett összfehérjét mutatott. Az időablak és a progresszív klinikum miatt CIDP-t feltételezve kezdettől intravénás immunglobulin-kezelést alkalmaztunk. Az ezt következő klinikai romlás miatt terápia-eszkalációként szteroidot adjuváltunk. Átmeneti stacioner állapotot követően klinikai és neurofiziológiai romlást észleltük, emiatt másodvonalbeli kezelési lehetőségek irányában immunológiai konzultáció történt. Az előbbi elbíráláshoz szükséges további kivizsgálás új etiológiai aspektusokat nem hozott, a diagnózisrevízió részeként megismételt antitest-meghatározások során azonban anti- MAG-pozitivitást találtunk. A választott rituximabkezelés érdemi eredményt nem hozott. Az ekkor már súlyosan mozgáskorlátozott beteg „salvage” terápiájaként 1 ciklus plazmaferézist alkalmaztunk, sikertelenül. Végül ismételt „expert opinion” konzultációk során biológiaiterápia-váltás helyett a rituximabciklusok folytatása mellett döntöttünk. Ezt követően az összképet komplikálandó, recidív ischaemiás stroke eseményt diagnosztizáltunk betegünknél. Széles körű etiológiai kivizsgálás során az immuneredetű vascularis történéseket is vizsgáltuk, emellett az esetleges nem kívánt terápiás következményeket sem hanyagoltuk el, tumorkutatás is indult, azonban eddig kórokot megállapítani nem tudtunk, így a terápiaválasztás is bizonytalan maradt. Esetünk a holisztikus, rendszerszintű és interdiszciplináris gondolkodás jelentőségét hangsúlyozza. Feltételezzük, hogy a beteg tünetei, melyeket az anti-MAGpozitivitás önmagában nem magyaráz, immunológiai eredetűek. A társuló vascularis események is a kóroki tényezők komplexitására utalnak. Megoldáshoz a neuroimmunológia interdiszciplináris munkamódszerekkel történő fejlesztése vezethet.
Epilepsziával járó autoimmun encephalitis miatt kezelt betegek klinikai összegzése epilepsziacentrumban
Az autoimmun encephalitisek a kóros, gyakran epilepsziát okozó immunológiai folyamatok széles körét ölelik föl, melyekben számos esetben kimutathatók neuronalis intracelluláris vagy sejtfelszíni antigének ellen termelődő antitestek. A betegség prevalenciáját napjainkban is alábecsülik, a diagnosztikus lépések és a pontos kezelési metodika nem teljesen tisztázott. Célunk az Országos Klinikai Idegtudományi Intézet Epilepszia Részlegén autoimmun encephalitis miatt gondozott betegek egyes alcsoportjai közötti klinikai, radiológiai, pszichopatológiai és elektrofiziológiai különbségek összegzése. Összesen 40 beteget választottunk be vizsgálatunkba; a betegeket a detektált antitestek, a klinikai, radiológiai, elektrofiziológiai szempontok alapján 9 különböző csoportba soroltuk. A legtöbb (n=11) beteg esetében GAD elleni antitestet találtunk, GABA-B receptor elleni antitest a legkevesebb, 1 beteg esetében volt. A legalacsonyabb átlagéletkorral (16,7 év) a posztinfekciós encephalitisszel (FIRES) diagnosztizált betegek, a legmagasabbal (50,4 év) a paraneoplasiás antitesteket termelő betegek rendelkeztek. A társbetegségeket megfigyelve az anti-GAD antitesttel rendelkezők több mint felének autoimmun pajzsmirigybetegsége volt. A vizsgált vasculitisszel diagnosztizált, anti-GABA-B antitesttel rendelkező és Rasmussen-kórban szenvedő betegeknél a koponya-MRI-vizsgálaton a betegségükkel összefüggő eltérés látszott, míg akiknél paraneoplasiás vagy anti-NMDA antitestet detektáltunk, a betegséggel összefüggésben lévő MRI-eltérés nem igazolódott. Az egy csoportba sorolt betegek antiepileptikus, illetve immunszuppresszáns kezelésre adott válasza is hasonló volt. A felszíni antigének ellen termelődött antitesttel bíró betegek esetén jobb volt a terápiás válasz, a leginkább terápiarefrakter betegek a Rasmussen- és a FIRES-csoportba tartoztak. Az autoimmun encephalitis egyes alcsoportjainak fenotípusa hasonló, de a klinikai megnyilvánulás, az EEGés az MR-vizsgálatok átfogó értékelése segíthet egy jól meghatározott rendellenesség diagnosztizálásában. Néhány példát említve, a pajzsimigybetegséggel társuló, MRI-negatív epilepszia hátterében anti-GAD-pozitív encephalitis is állhat. Memóriazavarral, TGA-val járó rosszullétek esetén későbbi életkorban paraneoplasiás mechanizmust is feltételezhetünk, ez segíthet malignus folyamat felfedezésében. Az autoimmun encephalitisben szenvedő betegekre csoportspecifikusan más-más klinikai minták igazak, és egy-egy csoportra különböző terápiás szükséglet, illetve különböző terápiás válasz jellemző. A jövő kihívása többek között a betegség korai felismerése, az encephalitis hátterében álló immunpatológiai folyamatok pontosabb megértése, és a megfelelő időben történő célzott kezelés kidolgozása, melyhez további vizsgálatok szükségesek.
1.
2.
3.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről4.
5.
1.
2.
Klinikai Onkológia
Hasnyálmirigyrák: az ESMO klinikai gyakorlati irányelve a diagnózishoz, kezeléshez, követéshez*3.
Klinikai Onkológia
Gyógyszerbiztonsági szemelvények – a múlt tanulságai és a jövő lehetőségei4.
5.