Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 85
Hírvilág
2021. AUGUSZTUS 24.
hirdetés
A TAGRISSO TM ▼ megkapta az Európai Gyógyszerügynökség (EMA) jóváhagyását a korai stádiumú, EGFR-mutációt hordozó, nem kissejtes tüdőrákban szenvedő betegek adjuváns kezelésére
A jóváhagyás a III. fázisú ADAURA vizsgálat eredményei alapján történt, ahol a TAGRISSO-kezelés 80%-kal csökkentette a halálozás, illetve a betegség kiújulásának relatív kockázatát.
Nőgyógyászati hormonterápia és a cardiovascularis rizikó. 1. rész: a hormonális fogamzásgátlás
A nem kívánt terhesség megakadályozása érdekében, valamint számos nőgyógyászati betegség kezelésében használjuk a petefészek által termelt hormonokat: a tüszőhormont és a sárgatesthormont, illetve ezek szintetikus változatait. A hormonálisterápiák között kiemelkedő jelentőséggel bír a kombinált orális hormonális fogamzásgátlás, valamint a menopauzális hormonterápia. Vannak készítmények, amelyek nem járnak a cardiovascularis kockázat növekedésével.
A végjátékot megváltoztató mRNS-oltás. Egy Nobel-díj krónikája
A Nobel Alapítvány bejelentette, hogy sok magyar várakozásának, reményeinek megfelelően Karikó Katalinnak és Drew Weissmannek ítéli az idei orvosi és fiziológiai Nobel-díjat, a Covid-oltásokat megalapozó módosított mRNS-technológia kifejlesztéséért. Duda Ernő virológussal, a Szegedi Tudományegyetem Szent-Györgyi Albert Orvostudományi Kar emeritus professzorával beszélgettünk a díj hátteréről.
Ökológia
2022. AUGUSZTUS 31.
Antibiotikum-rezisztencia a környezetben
Az antibiotikum-rezisztencia globális egészségügyi kihívássá vált. Bár számos akadály nehezíti a baktériumok és gének áramlását, újra és újra megjelennek az adott fajokra korábban nem jellemző rezisztenciagének, ezzel megnehezítve a baktériumokkal összefüggő megbetegedések megelőzését és kezelését. Az Antibiotic resistance in the environment című, a Nature Reviews Microbiology szaklapban megjelent cikkükben a szerzők az antibiotikum-rezisztencia kialakulásának hátteréről, e probléma nyomon követésének és kezelésének lehetőségeiről összegezték a rendelkezésre álló ismereteket.
Négy Niemann–Pick C esetünk, diagnosztikus és terápiás lehetőségek
42 éves nő. Újszülöttként icterus, hepatomegalia, intrahepaticus epeút-hypoplasia, cystoduodenostomia. Húszas évektől szellemi hanyatlás, ataxia, spasticus járás. Később myoclonusok, aluszékonyság, depresszió, akaratlan végtagmozgások, nyelészavar.
Genetika Parkinson-kórban: crescit audacia experimento
Hagyományos értelemben az idiopathiás Parkinson-kór egy sporadikus előfordulású megbetegedés, habár az esetek családi halmozódása régóta ismeretes. A genetikai vizsgálatok előretörésével közel 20 monogénes öröklődésű kórformát, valamint számos rizikófaktorként szerepet játszó genetikai variánst is sikerült igazolni. Habár a monogénes formák ritkák, a genetikai rizikófaktorok gyakrabban fordulnak elő, de a pontos prevalenciájuk nem ismert.
Jövő Unikornisa Díj a rákdiagnosztikát segítő fejlesztésért
A Digital Europe kereskedelmi szövetség ebben az évben a Peták István és Schwab Richárd kutatóorvosok által alapított Oncompass Medicine molekuláris diagnosztikával és precíziós orvoslással foglalkozó céget díjazta a Jövő Unikornisa Díjával. A kitüntetést azon technológiai vállalkozásoknak adományozzák, amelyek jövőbeli értéke meghaladhatja az egymilliárd dollárt. Az Oncompass Medicine-t 17 európai ország legkülönfélébb területeken működő vállalkozásai közül választották ki. Az elismerést Mariya Gabriel az EU innovációért felelős biztosa adta át virtuálisan a magyar biotechnológiai cégnek 2021. február 4-én, a rák világnapján. A Jövő Unikornisa Díjat a kutatóorvosok a daganatos betegek célzott terápiájának segítésére fejlesztett orvosi szoftverrel érdemelték ki. A Real-Time Oncology Treatment Calculator (TM) elnevezésű informatikai eszköz példátlanul sok, 405 ráktípusban, 52 ezer mutáció esetén, 26 838 orvosbiológiai szabály alapján, 1417 gyógyszerhatóanyag közül képes rangsorolni az adott beteg betegségéhez és genetikai profiljához kijelölhető, legjobb reményekkel kecsegtető terápiákat. Mindehhez pedig 0,02 másodpercre van szüksége. Peták István évtizedek óta foglalkozik molekuláris rákdiagnosztikával, személyre szabott precíziós onkológiával, célzott gyógyszerfejlesztéssel. A kutató a díj alkalmából adott interjút folyóiratunknak.
[Új patogén mutáció következtében kialakuló karnitin-palmitoil-transzferáz II-hiánnyal magyarázható ismétlődő rhabdomyolysis]
[A karnitin-palmitoil-transzferáz II- (CPT II-) hiány egy autoszomálisan öröklődő anyagcsere-rendellenesség, amelyben a hosszú láncú zsírsavak β-oxidációja hiányos. A klinikai megjelenés különféle formában lehetséges; súlyos formájában jelentkezik újszülöttkorban és infantilis időszakban, míg iskolás- és serdülőkorban a kevésbé súlyos myopathiás formában jelentkezik. Bár a rhabdomyolysisrohamok súlyossága változó, a klinikai lefolyást esetenként akut veseelégtelenség komplikálhatja. Az acilkarnitin-elemzés segíthet a CPT II diagnosztizálásában, de az eredmény normalitása nem jelzi a betegség hiányát. Erős gyanú esetén genetikai elemzést kell végezni. Ebben a tanulmányban egy 15 éves fiú beteg esetét mutatjuk be, akinek két, fertőzés, illetve éhezés által kiváltott rhabdomyolysisrohama volt. Az acilkarnitin-elemzés eredménye normális volt, a kórtörténet értékelésénél figyelembe vettük a CPT II-hiányt, és kimutattuk a CPT II gén c.137A> G (p.Gln46Arg) új patogén homozigóta mutációját. A CPT II-hiány a metabolikus rhabdomyolysis egyik leggyakoribb oka az ismétlődő rhabdomyolysisepizódoktól szenvedő betegek esetén.]
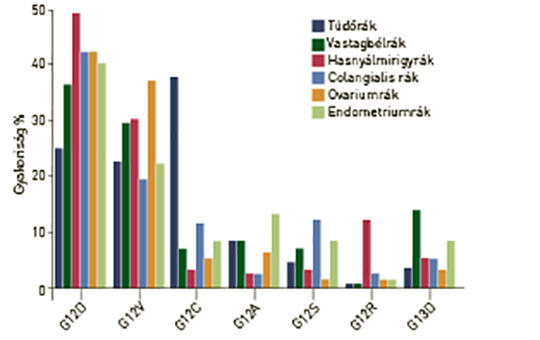
A (K)RAS-mutáció molekuláris epidemiológiája emberi daganatokban
A RAS onkogén mutációja a leggyakoribb génhiba emberi daganatokban, és a három családtag közül a K-RAS-é a leggyakoribb, amit az N-RAS követ. A tipikus K-RAS-mutáns daganatok a hasnyálmirigyrák, vastagbélrák és tüdő-adenocarcinoma, amelyekben a mutáns variáns allélok gyakorisága igen heterogén, aminek hátterében eltérő karcinogenezis áll. A RAS-mutáns daganatok genetikai sokszínűségét tovább fokozza, hogy a mutáns allél homo- vagy heterozigóta formában van-e jelen. A sokszínűség egy másik forrása az, hogy a különféle daganatokban a K-RAS-mutánsok esetében sajátos kísérő mutációs mintázatú altípusok lehetnek. Mindezeknek az a következménye, hogy a K-RAS-mutáns daganatok biológiai viselkedése és nagy valószínűséggel terápiás érzékenysége is nagyon heterogén lehet. A K-RAS-inhibitorok klinikai debütálásával ezeknek a kérdéseknek egyre nagyobb jelentősége lesz.
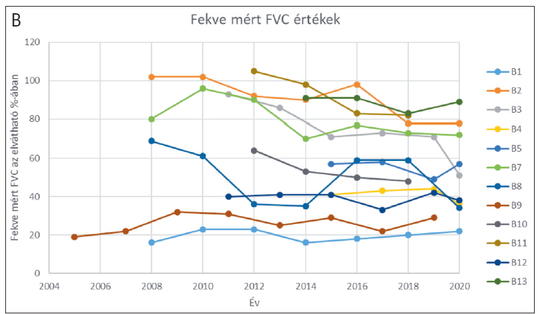
A késői kezdetű Pompe-kórban szenvedők enzimpótló kezelésének hosszú távú követése
A Pompe-kór (PD) egy ritka lizoszomális tárolási betegség, amit a GAA gén mutációja következtében kialakuló α-glükozidáz (GAA) enzim elégtelen működése okoz. Az enzimdeficientia a glikogén lizoszomális felszaporodásához vezet. A betegségnek két klinikai formája ismert, az újszülöttkori, valamint a késői forma. Jelenleg a betegség hátterében a GAA génnek közel 600 mutációja ismert. A kaukázusi populációban a késői forma hátterében a c.-32-13T>G mutáció a leggyakoribb, az allélfrekvencia közel 70%. A Pompe-kórt enzimpótló terápiával (ERT) tudjuk kezelni, kéthetente Myozyme infúzió adásával. Közleményünkben 13, több mint öt éve kezelt, késői kezdetű formában szenvedő beteg hosszú távú követését mutatjuk be. A leghosszabb követési idő 15 év volt. A kezelés eredményességének megítélésére évente mértük a 6 perces járótávolságot és a légzésfunkciót. Az adatok alapján a 6 perces járótávolság az enzimpótló kezelés indítása után körülbelül 3-4 évig javult, ezt követően az esetek többségében a megtett távolság csökkent. A több mint 10 éves követés után a kezdeti 6 perces járótávolsághoz képest romlást tapasztaltunk az esetek 77%-ában, javulást az esetek 23%-ában. A követés ideje alatt mindössze egyetlen beteg került kerekesszékbe. A légzésfunkció, különösen fekvő helyzetben hasonlóan alakult. A betegek terápiára adott válaszában nagy variabilitást figyeltünk meg, ami csak részben mutatott összefüggést a terápiás fehérje ellen termelődő antitestszinttel. Az ERT eredményessége jelentősen függött a betegséget okozó mutáció típusától, a betegség státuszától a kezelés kezdetekor, a beteg fizikai aktivitásától és táplálkozási szokásaitól. Az innovatív orphan gyógyszerekkel kezelt betegek hosszú távú követése kiemelkedően fontos ahhoz, hogy megismerjük a kezelés valós hasznát és a betegek igényeit.
1.
2.
3.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről4.
5.
1.
2.
Klinikai Onkológia
A rosszindulatú daganatok fenotípusának plaszticitása és az immunogén mimikri3.
Klinikai Onkológia
A szarkopénia mérése komputertomográfiával és jelentősége az onkológiai betegeknél4.
5.