Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 173
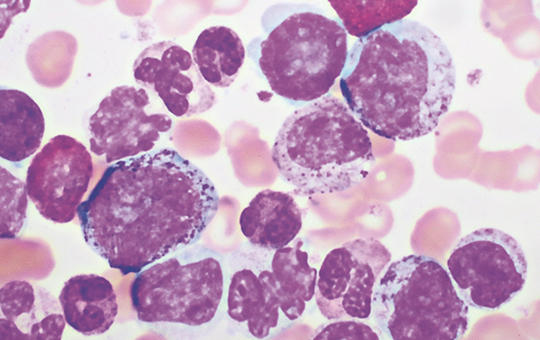
A krónikus myeloid leukaemia kezelésének aktualitásai
A krónikus myeloid leukaemia a tirozinkináz-gátló kezelések megjelenése óta halálos betegségből jól kezelhető, krónikus kórképpé vált. A betegség alapját a Philadelphia-kromoszóma kialakulása és a konstitutívan aktív BCR-ABL1 tirozinkináz keletkezése okozza. A tirozinkináz-gátlók alkalmazása mellett a krónikus fázisú CML-es betegek életkilátásai ma már megközelítik a normálpopulációét.
Poszttranszplantációs hypertonia rizikófaktora és hatása az allograft funkciójára
Bevezetés: A vesetranszplantációt követő halálozások csaknem 40%-a valamilyen cardiovascularis betegség miatt történik, amelynek egyik főbb rizikófaktora a transzplantáció utáni magas vérnyomás (PTHT), ami gyakran nem kerül felismerésre és kezelésre. Beteg és módszerek: Kutatásunk során a PTHT előfordulási gyakoriságát és kockázati tényezőit vizsgáltuk, valamint a PTHT hatását az allograft működésére. Eredmények: Vizsgálatunkban a PTHT előfordulásának gyakorisága 42% volt. A rizikófaktorokat vizsgálva BMI, életkor, nemek arányában szignifikáns különbséget nem találtunk. A PTHT szignifikánsan nagyobb arányban fordult elő a ciklosporint szedők körében (p=0,021), mint a takrolimuszt szedőknél. A vese funkcióját vizsgálva a szérumkreatinin- (p=0,024), urea- (p=0,005) és eGFR- (p=0,036) értékek szignifikánsan különböztek a PTHT és a normális vérnyomású betegek között. Megbeszélés: A transzplantáció után újonnan kialakult hypertonia allograftra gyakorolt hatása már korán megmutatkozik a vesefunkcionális értékek romlásában. Ezért elengedhetetlennek tartjuk a vérnyomás rendszeres ellenőrzését, szükség esetén a vérnyomáscsökkentő terápia megkezdését.
Vélemény a TIME vizsgálatról. Vérnyomáscsökkentő reggel és/vagy este? A kronofarmakoterápia jelentősége
A Hypertonia és Nephrologia legutóbbi számában (2022;26(5):244-245.) megjelent TIME tanulmány (Hypertoniás felnőttek cardiovascularis eseményeinek gyakorisága a szokványosan alkalmazott antihipertenzív szerek esti, illetve reggeli adáskor az Egyesült Királyságban végzett prospektív, véletlenszerű betegbeválasztásos, nyílt elrendezésű, vak végpontú klinikai vizsgálat) ismertetése kapcsán írom véleményemet.
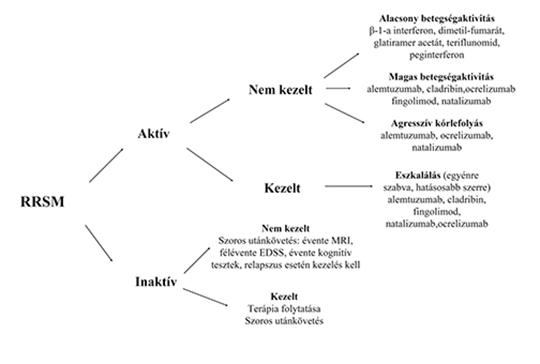
Alemtuzumabterápiával kezelt sclerosis multiplexes betegek követéses vizsgálata a szegedi Sclerosis Multiplex Centrumban
A relapszus-remisszió kórformájú sclerosis multiplex kezelési stratégiája az elmúlt évtizedben jelentősen megváltozott. Míg korábban az eszkalációs terápia volt az elfogadott terápiás módszer, napjainkban magas betegségaktivitás esetén lehetőségünk van indukciós kezelés indítására is.
EEG-alapú agyi funkcionális konnektivitásvizsgálat epilepsziákban
A krónikus fájdalomszindrómák több mint 80 millió embert érintenek Európában. A gyógyszeres kezelésre nem reagáló deafferentációs fájdalmak csökkentésére már 1954-ben publikálta Heath a mély agyi stimulációs módszert.
A krónikus stressz szerepe az essentialis hypertonia kialakulásában. A rilmenidin helye a stressz által kiváltott hypertonia kezelésében
A hypertonia a cardiovascularis betegségek egyik önálló rizikótényezője. Kialakulásában számos tényező játszik szerepet. Ezek közül a krónikus stressz a szimpatikus aktivitás fokozásán keresztül eredményezheti a magasvérnyomás-betegség kialakulását. A szimpatikus idegrendszeri aktivitás emelkedésének jeleit elsősorban a hypertonia kezdeti – perctérfogat-fokozódással járó – szakaszában észlelhetjük. A szimpatikus aktivitás fokozódása a hemodinamikai következményeken (perctérfogat-emelkedés, tachycardia, coronariavasoconstrictio, proarrhythmia) túl számos kedvezőtlen következménnyel járhat. A metabolikus (inzulinrezisztencia, dyslipidaemia), strukturális és trofikus hatásokon túl (endotheldiszfunkció, vascularis hypertrophia, myocardium-hypertrophia), thromboticus és humorális (prokoaguláció, thrombocytaaggregáció-fokozódás, nátriumretenció, renin-angiotenzin-aldoszteron tengely aktivációja) folyamatok indulhatnak el, amelyek több támadásponton károsíthatják a szervezet működését. A fokozott szimpatikus aktivitás kedvező befolyásolására számos antihypertensiv gyógyszercsoport áll rendelkezésünkre. Idetartoznak a perifériásan ható alfa- és béta-blokkolók, továbbá a centrálisan ható vegyületek. Ez utóbbiak első generációját (például clonidin, guanfacin, alfa-metildopa) – jelentős mellékhatásprofiljuk miatt – jelenleg ritkán, egyáltalán nem vagy csak szűk indikációs körben alkalmazzuk. A második generációs, centrálisan ható vegyületek közül a rilmenidin, az imidazolin-I1-receptorok stimulációjának útján fejti ki kedvező hatásait, amelyeket kihasználhatunk a szimpatikus idegrendszer fokozott aktivitásával járó enyhe vagy mérsékelt hypertoniában.
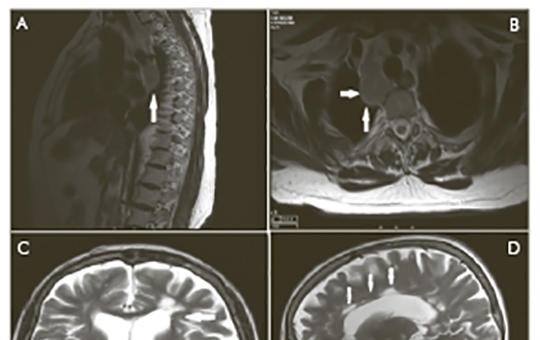
[Esetbemutatás: Sclerosis multiplexben szenvedő betegben immunmoduláns kezelés során kialakult lymphopenia és tuberculosus lymphadenitis ]
[Az interferon-β- (IFN-β) 1a és a glatiramer-acetát (GA) a sclerosis multiplex (SM) első vonalbeli kezelésében használatos immunmoduláns szerek. Egy olyan SM-beteg esetét mutatjuk be, akinél ezen immunmoduláns szerek alkalmazása során lymphopenia és tuberculous lymphadenitis alakult ki. Az SM-ambulanciánkon kezelt, jelenleg 65 éves nőbeteg korábban 20 mg/nap subcutan GA-, majd heti háromszor 44 µg subcutan IFN-β 1a-terápiában részesült. Immunmoduláns kezelése során enyhe-súlyos lymphopenia alakult ki nála. Utánkövetése során (800/µl lymphocytaszámnál) thoracalis gerinc-MR-felvételén a posterior mediastinumban számos megnagyobbodott nyirokcsomó ábrázolódott. A további vizsgálat tuberculosus lymphadenitist igazolt. Ezt követően kilenc hónapig tuberculosis (tbc) elleni kezelésben részesült, és tbc-fertőzése megszűnt. Habár az immunmoduláns kezelést az opportunisztikus fertőzések kialakulása szempontjából biztonságosnak tartják, és az immunmoduláns kezelés során kialakuló lymphopenia általában enyhe és tünetmentes, a bemutatott esetben nem ez történt. További vizsgálatokra van szükség annak kiderítése érdekében, hogyan kell a lymphopeniás betegeket kezelni, és milyen mértékű a tbc kialakulásának kockázata immunmoduláns kezelés során.]
Idegtudományok
2022. MÁRCIUS 08.
Mi történik az agyunkban, amikor meghalunk?
Először rögzítették EEG-vel egy haldokló ember agyhullámait. Az agy az átmenet során és 30 másodpercig a halál után is aktív és koordinált maradt. Az átmenet során az álmodásra, a memória-előhívásra és a meditálásra jellemző EEG-hullámok jelentek meg.
Az inzulin: alfa és ómega
Az 1-es típusú cukorbetegséget az inzulint termelő β-sejtek autoimmun pusztulása okozza. A folyamat hátterében az elsődleges antigén (ha az elsődleges antigén teóriája helytálló) nagy valószínűséggel maga az inzulin vagy a proinzulin. Ugyanakkor az 1-es típusú cukorbetegség kezelése gyakorlatilag egyet jelent az inzulinkezeléssel. Minél korábban ismerjük fel és kezdjük kezelni az 1-es típusú cukorbetegséget, és minél jobb glykaemiás eredményeket érünk el, annál nagyobb a valószínűsége annak, hogy a β-sejt-állomány tovább marad működőképes. Az inzulin az 1-es típusú cukorbetegség kialakulásának immunpatogenezisében és kezelésében is alapvető szerepet játszik, tehát az alfa és ómega ebben a betegségben.
Magas aktivitású sclerosis multiplex hatásos kezelése gyermekkorban
A sclerosis multiplex (SM) jellemzően a fiatal felnőttek betegsége. Gyermekkori sclerosis multiplexről 18 éves kor alatt kezdődő megbetegedés esetén beszélhetünk, bár egyes szerzők 16 éves kor alatt szabják meg a határt. Korábban „early onset multiple sclerosis”, illetve „juvenilis sclerosis multiplex” néven vált ismertté. A gyermekkori SM előfordulási gyakorisága az összes SM 3–5%-a. Napjainkban, köszönhetően az egyre jobb diagnosztikai eszközöknek és a jól követhető, szigorúan meghatározott diagnosztikus kritériumoknak, a gyermekkori SM incidenciája világszerte növekszik (0,05–2,85/100 000). Az SM-et térben és időben elkülöníthető, ismétlődő központi idegrendszeri demyelinisatióval jellemezhető epizódok jellemzik. Gyermekkorban csaknem kizárólag a relapszáló-remittáló (RR) forma fordul elő. A felnőtteknél szerzett tapasztalatokra építve a gyermekpopulációban szintén a korai diagnózis, az adekvát betegségmódosító terápia (DMT) mielőbbi indítása, a tünetmentesség és a jó életminőség elérése a cél. A felnőtt populációban végzett hatékonysági és biztonságossági vizsgálatok alapján a gyermekkori SM kezelésében az FDA és az EMA először az interferon β-1a-t és a glatiramer acetátot engedélyezte. A gyermekkori SM-re jellemző magas relapsusráta és az első DMT-re közel 45%-ban adott kedvezőtlen terápiás válasz szükségessé tette a hatékonyabb és második vonalbeli szerek vizsgálatát a 18 év alatti populációban is (PARADIGMS, CONNECT). A nemzetközi közlemények szerint a natalizumab hatékony és jól tolerálható az aktív RR gyermekkori SM-ben, de kontrollált tanulmány hiányában az esetismertetésünkben szereplő betegeinknél evidencia még nem állt rendelkezésre. Közleményünkben haárom aktív RR-SM-ben szenvedő betegünk indikáción túli, egyedileg engedélyeztetett natalizumabbal végzett sikeres kezeléséről számolunk be.
1.
2.
3.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről4.
5.
1.
2.
Klinikai Onkológia
A rosszindulatú daganatok fenotípusának plaszticitása és az immunogén mimikri3.
Klinikai Onkológia
A szarkopénia mérése komputertomográfiával és jelentősége az onkológiai betegeknél4.
5.