Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 255
[Lehetséges genotípus-fenotípus korrelációk C típusú Niemann–Pick-kórban és a betegek miglustatkezelése]
[A C típusú Niemann–Pick-kór károsodott intracelluláris koleszterintranszport miatt kialakuló, ritka lizoszomális tárolási betegség. Az autoszomális recesszív betegséget az NPC1 vagy NPC2 gén mutációi okozzák. Értékeltük kora újszülöttkori, C típusú Niemann–Pick-kórral diagnosztizált betegeink klinikai és laboratóriumi tüneteit, a genotípusuk és a fenotípusuk közötti korrelációt és a miglustatkezelésre adott válaszukat. Tanulmányunkban bemutatjuk négy, C típusú Niemann–Pick-kórral kora újszülöttkorban diagnosztizált beteg esetét. Betegeink közös tünete volt a hepato- és splenomegalia, a cholestasis és a mozgásfejlődés visszamaradása. Az 1-es és a 2-es beteg (ikrek) az NPC1 gén c.2776G>A p.(Ala926Thr) homozigóta mutációjával és súlyos fokú tüdőérintettséggel bírt. A tüdőérintettség, ami a szakirodalom szerint általában az NPC2 gén mutációjával jár együtt, betegeinkben olyan súlyos fokú volt, ami korai halálukat eredményezte. A 3-as és 4-es beteg az NPC1 gén c.2972del p.(Gln991Argfs*6) mutációjával és az NPC2 gén homozigóta c.133C>T p.(Gln45*) mutációjával bír. Ennél a két betegnél miglustatkezelés hatására a neurológiai tünetek javulását figyeltük meg. Ikerpár betegeinknél súlyos fokú tüdőérintettséget figyeltünk meg. A négy közül kettő, kora újszülöttkori, C típusú Niemann–Pick-kórral diagnosztizált betegünk neurológiai tünetei a miglustatkezelés hatására javultak.]
A méhnyakrák korszerű onkológiai kezelése
Világszerte évente több mint félmillió nőnél igazolódik méhnyakrák, és körülbelül 300 000 halálesetet okoz a betegség. A nyugati társadalmakban a cervixcarcinoma incidenciája és mortalitása csökken a humán papilloma vírus (HPV) elleni vakcinációnak és a populációs szintű szűrésnek köszönhetően. A fejlődő világ országaiban azonban továbbra is emelkedő a tendencia. A rákmegelőző állapotok és a korai méhnyakrák definitív onkológiai ellátása a stádiumfüggő kiterjesztéssel végzett műtétek révén lehetséges. A posztoperatív sugárkezelés vagy kemoradioterápia szükségessége a patológiai rizikófaktorok alapján határozható meg. Előrehaladott méhnyakrákban a definitív kemoradioterápia vagy a szisztémás kezelés a terápiás alternatívák. A fiatal betegek részéről gyakran felmerülő kívánság a fertilitásmegtartás, amely az onkológiai elvekkel csak jól definiált határok között egyeztethető össze, alapos felvilágosítást követően. A terhesség alatt felismert méhnyakrák becsült incidenciája 1,4-4,6 eset/100 000 szülés, amelynek ellátása során, az onkológiai szempontokon túl, a magzat biztonságát is szem előtt kell tartanunk az anya preferenciái alapján. A klasszikus kemoterápia mellett a biológiai szerek is megjelentek a közelmúltban a méhnyakrák szisztémás kezelési lehetőségei között: első vonalban bevacizumabbal egészíthető ki a ciszplatin-paclitaxel kombináció közel négy hónapos túlélési előnyt nyújtva a betegek számára; míg másodvonalban pembrolizumab adható mikroszatellita-instabil vagy PDL-1-et expresszáló (combined positive score [CPS] ≥1), illetve magas tumormutációs terheltséget (TMB ≥10) mutató daganatok esetén. A jelen munka egy rövid összefoglalót szolgáltat a méhnyakrák megelőzéséről, kivizsgálásáról és onkológiai ellátásáról.
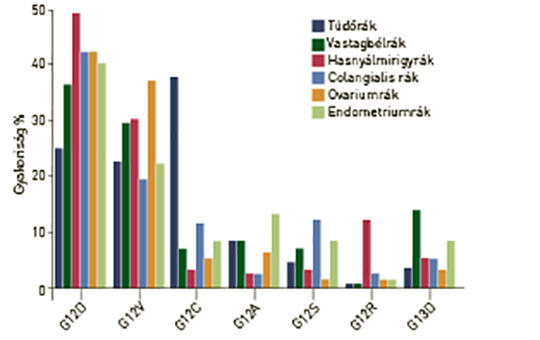
A (K)RAS-mutáció molekuláris epidemiológiája emberi daganatokban
A RAS onkogén mutációja a leggyakoribb génhiba emberi daganatokban, és a három családtag közül a K-RAS-é a leggyakoribb, amit az N-RAS követ. A tipikus K-RAS-mutáns daganatok a hasnyálmirigyrák, vastagbélrák és tüdő-adenocarcinoma, amelyekben a mutáns variáns allélok gyakorisága igen heterogén, aminek hátterében eltérő karcinogenezis áll. A RAS-mutáns daganatok genetikai sokszínűségét tovább fokozza, hogy a mutáns allél homo- vagy heterozigóta formában van-e jelen. A sokszínűség egy másik forrása az, hogy a különféle daganatokban a K-RAS-mutánsok esetében sajátos kísérő mutációs mintázatú altípusok lehetnek. Mindezeknek az a következménye, hogy a K-RAS-mutáns daganatok biológiai viselkedése és nagy valószínűséggel terápiás érzékenysége is nagyon heterogén lehet. A K-RAS-inhibitorok klinikai debütálásával ezeknek a kérdéseknek egyre nagyobb jelentősége lesz.
SARS-CoV-2-immunitás és kapcsolata az oltásokkal
A The Lancet tanulmánya összefoglalja jelenlegi tudásunkat a SARS-CoV-2-fertőzésre adott humorális és celluláris immunválasszal kapcsolatban, és összehasonlítja a természetes, valamint a befogadott, illetve III-as fázisú vizsgálatban lévő vakcinákra adott immunválaszokat.
Heterogenitás és a daganatok
A sejtek alapvető feladata, hogy fenntartsák az egyensúlyt a proliferáció és a programozott sejthalál között, amely lehetőséget ad a sejt számára, hogy specifikus feladatát végrehajtsa. Ez a folyamat szorosan összekapcsolódik a szomszédos sejtekkel, továbbá a sejtek közötti állománnyal is. Mindezek szabályozásában hibák keletkezhetnek, persze leggyakrabban mutációk. Ezek némelyike a sejt életében zavarokat okozhat, azonban a mutációk többsége nem játszik fontos szerepet. Jól ismert a benignitás és a malignitás elkülönítése, amelyből a daganatsejtek metasztatizálása az igazi veszély. (Tulajdonképpen klinikailag akkor lehet malignusnak tekinteni egy daganatot, ha képes a metasztatizálásra.) Ez az említett hiba lehet veleszületett és szerzett, amellyel a normális klonális jelenlétet fokozatosan uniklonálissá változtatja (inkább a hematológiai tumorokban, mintsem a szolidokban), és ez a poliklonalitás összezavarja a sejt funkcionális képességét. Érthető tehát, hogy ezt a két jelenséget, a metasztatizálást és a szelekciót tekinthetjük a terápia első számú célpontjának. A heterogenitás fontos szerepet játszik a sejtek életében.
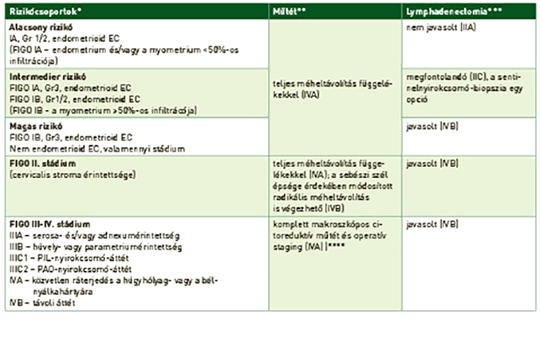
A méh rosszindulatú daganatainak korszerű onkológiai kezelése
Világviszonylatban évente közel 400 000 nőnél igazolódik méhtestrák, amely 2018-ban körülbelül 90 000 nő halálát okozta. Az esetek túlnyomó részét a méhnyálkahártya hormonérzékeny hámjából kiinduló endometriumcarcinomák (EC) alkotják. A sarcomák a méhtestrákok alig 3%-át adják. Az EC-k 80-85%-a jó prognózisú, mivel alacsony gradusú és korai stádiumban kerül felismerésre, amikor a műtét és az esetleges posztoperatív kezelés révén a gyógyulás reális terápiás cél. Az előrehaladott stádiumban diagnosztizált EC és a nem endometrioid altípusok esetén a prognózis lényegesen rosszabb. A magas rizikójú EC optimális adjuváns kezelésére irányuló vizsgálatok egy része még folyamatban van, illetve a bővülő molekuláris ismeretek újabb vizsgálatokat generálnak. A méhtestsarcomák esetében is a sebészi eltávolítás jelenthet kuratív megoldást, az adjuváns kezelésre vonatkozó evidenciák bizonytalanok, egyéni mérlegelést igényelnek. A modern onkoterápia érájában már nemcsak a betegségmentes élet meghosszabbítására, hanem az élet minőségének minél teljesebb megőrzésére is törekszünk. A nőgyógyászati onkológiában ezt jelenti a fertilitás vagy a funkcionáló ováriumok lehetőség szerinti megőrzése; a magas morbiditással járó szisztémás lymphadenectomia indikációs körének szűkítése; a kedvezőbb mellékhatásprofilú brachytherapia alkalmazása a teljes kismedencei besugárzás helyett. A modern onkoterápia az úgynevezett biológiai kezelések által az előrehaladott betegségek ellátásának is a részévé vált: kemoterápia mellett/után progrediáló esetekben a pembrolizumab az EC és a sarcomák esetén is alkalmazható mikroszatellita-instabilitás vagy magas tumormutációs terheltség esetén, míg az NTRK fúziós gén jelenlétében larotrectinib vagy entrectinib mint célzott tirozinkináz-gátlók javasolhatók. Az EC-k 70-80%-át kitevő mikroszatellita-stabil esetekben (nem endometrioid altípusokban is!) a pembrolizumab lenvatinibbel kombinációban adható a kemoterápia után. Az EC területén gyarapodnak továbbá az egyéb célzott terápiás szerekkel szerzett tapasztalatok is (anti-HER2 serosus carcinomában, mTOR-gátló kezelés, endokrin terápia, más immun checkpoint inhibitorok, tirozinkináz-gátlók, PARP-gátlók és kombinációs kezelések). A jelen munka a méhtestrákok onkoterápiájáról kíván rövid összefoglalást nyújtani az aktuális szakmai ajánlások és a folyamatban lévő vizsgálatok bemutatásával.
Agnosztikus terápia onkológiai alkalmazása
A tumoragnosztikus terápia az onkológiai kezelés ígéretes lehetősége, azonban a potenciális célpontok klasszifikálása, validálása, azok egységes módszerek szerinti kimutatása elengedhetetlen. A tumoragnosztikus kezelések engedélyezése új típusú, biomarker-vezérelt klinikai vizsgálatok bevezetését tette szükségessé. Jelenleg három tumoragnosztikus molekuláris célpont ismert: a daganatok magas fokú mikroszatellita-instabilitása (MSI-H), a neurotrop-tirozinkináz-receptor (NTKR) gének fúziója, valamint a daganatok magas tumormutációs terhelése (TMB-H). A pembrolizumab (anti-PD-1 antitest) az első tumoragnosztikus indikációban is törzskönyvezett gyógyszer, amelyet először MSI-H daganatok kezelésére engedélyeztek, majd később a magas TMB is bekerült az indikációk közé. Az NTKR-fúziót hordozó daganatok kezelésére a larotrectinib és az entrectinib került engedélyezésre.
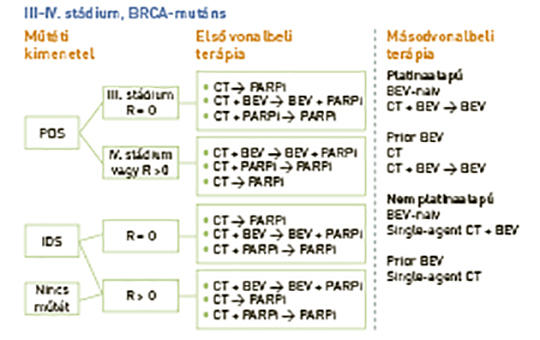
A petefészekrák kezelésének frontvonalában: a PARP-gátlók szerepének megújítása
Kiújult petefészekrákban a poli(ADP-ribóz)polimeráz- (PARP-) gátlókkal történő kezelések megváltoztatták a platinaérzékeny daganatok kezelését. Az új adatok szerint a PARP-gátlókat a kezelési algoritmus korábbi szakaszában kell alkalmazni. A kutatók számba veszik azokat a fázis III vizsgálatokat, amelyekben a PARP-gátlók hatását értékelték újonnan diagnosztizált petefészekrákok primer, illetve fenntartó kezelésében. Megvitatják a gyógyszerek hatásosságát és biztonságosságát az összes daganat, illetve a biomarkerek szerint válogatott daganatok klinikai vizsgálataiban, és összevetik a különböző vizsgálatok előnyeit és korlátait. Fontolóra veszik a jövő kutatásainak prioritásait – különös tekintettel a betegek kiválasztására és a jövőben alkalmazandó, egyelőre hiányzó gyógyszeres regimenek megalkotására. Négy fázis III vizsgálatban (SOLO-1, PAOLA-1/ENGOT-OV25, PRIMA/ENGOT-OV26 és VELIA/GOG-3005) PARP-gátlók használatával (olaparib, niraparib vagy veliparib) a progressziómentes túlélés jelentős javulását figyelték meg petefészekrákos betegekben. A vizsgálatok eltérő kialakítása (kezelés vagy fenntartó kezelés, egy gyógyszeres vagy kombinációs kezelés, bevacizumabbal vagy bevacizumab nélkül), a betegek kiválasztása (műtéti eredmény, biomarkerek elérhetősége, prognózis szerint), a résztvevők eredeti megválasztása (intention-to-treat, BRCA-mutációs vagy homológ rekombinációdeficites pozitív) befolyásolták a vizsgálatokból levonható következtetéseket. A teljes túlélési adatok még függőben vannak, hosszú távú biztonságossági adatok is csak korlátozottan állnak rendelkezésre. A PARP-gátlók sarkalatos szerepet játszanak az újonnan kimutatott petefészekrák-ellátásban, és befolyásolják a további kezeléseket. Ki kell választani azokat a betegeket és gyógyszereket, akiknél az eddigi alkalmazott kezelések a PARP-gátlóknál kevesebb haszonnal járnának.
Mammográfiás szűrésre várják október 30-án a beutalóval rendelkező hölgyeket az SZTE Radiológiai Klinikán
A mellrák a hölgyek körében a leggyakrabban előforduló daganattípus, amely világszerte a nők 10-12 százalékát érinti, és évente mintegy 2200 életet követel Magyarországon! Ennek oka, hogy a többségüknél már csak előrehaladott klinikai stádiumban ismerik fel a betegséget, miközben az időben felfedezett és diagnosztizált emlődaganat sokkal hatékonyabban gyógyítható! Mivel a betegség kezdeti stádiumában tünet- és panaszmentes, ezért nem lehet elégszer hangsúlyozni a szűrővizsgálatok és a helyesen végzett, rendszeres önvizsgálat fontosságát! A legközelebbi mammográfiás szűrőnapon, október 30-án, pénteken 15 órától 20 óráig várják az SZTE Radiológiai Klinika Női Diagnosztikai Osztályán a beutalóval rendelkező hölgyeket szűrővizsgálatra.
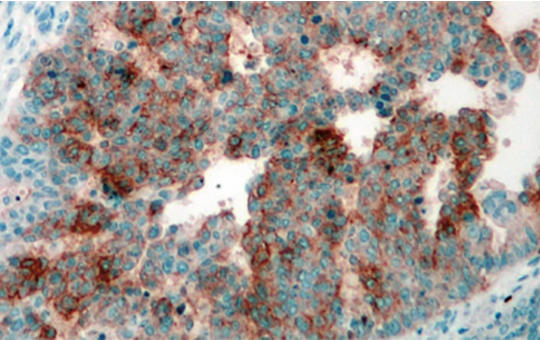
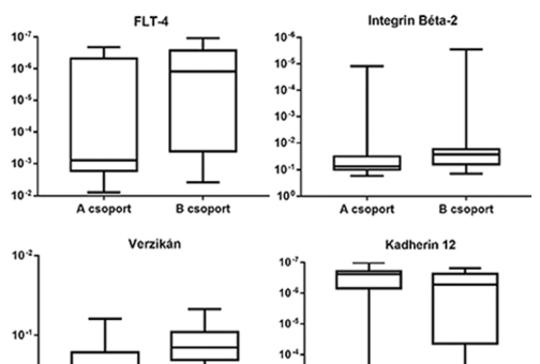
Az inváziós spektrum prognosztikai jelentősége glioblastomában
A glioblastoma a leggyakoribb központi idegrendszeri rosszindulatú daganat; sebészi kezelése a daganatok invazív jellegénél fogva nem lehetséges, onkoterápiája pedig csupán szerény eredményeket hoz – a betegek átlagos teljes túlélése (OS) 16–24 hónap. A betegek egy része alig reagál az alkalmazott kezelésre; a klinikumban jelenleg nincs olyan prognosztikai vagy prediktív marker, ami segítené a betegek túlélésében tapasztalható jelentős szórás érdemi feltérképezését és a kezelési algoritmus optimalizálását. Jelen kutatásban az invázióban szerepet játszó extracelluláris mátrix (ECM-) molekulák expressziójának prognosztikai jelentőségét kívántuk meghatározni. Eltérő prognózisú betegcsoportokat létrehozva (A csoport OS < 16 hónap, B csoport OS > 16 hónap) vizsgáltuk meg glioblastomás betegek gyorsfagyasztott tumormintáiban a szakirodalom által jelenleg elismert markerek (IDH1 mutációs és MGMT metilációs státusz) jelenlétét, továbbá 46 inváziós ECM-molekula mRNS-szintjét. A DE KK Idegsebészeti Klinikán operált és az Onkológiai Klinikán utókezelt betegek klinikai adatai nem mutattak jelentős különbségeket a túlélési adatokat (progressziómentes és teljes túlélés) és a reoperációs arányt leszámítva. Minden minta IDH vad típusú volt. Jelentős különbség volt a jobb és a rosszabb túlélésű betegek között az MGMT promoter hipermetiláció arányában (28,6% vs. 68,8%). Az inváziós ECM-molekulák expressziós mintázata, az inváziós spektrum szintén jelentős különbséget mutatott; szignifikáns különbség mutatkozott az integrin β2, kadherin-12, FLT4/VEGFR-3, verzikán molekulák expressziójában. Az inváziós spektrum megbízhatóságát statisztikai osztályozóval tesztelve a módszer a minták 83,3%-át sorolta a megfelelő prognosztikai csoportba (PPÉ: 0,93). A különböző túlélésű betegcsoportok összehasonlítása során a reoperációs arányban megfigyelhető különbség az irodalmi adatokkal összevágó tény. Az MGMT promoter metiláltságának vizsgálata hazai újdonság, az eredmény az eddigi ismereteket megerősítve sürgeti a vizsgálat rutinszerű bevezetését. Az inváziós spektrum vizsgálata többletinformációt ad a tumorról, prognosztikai markerként segíthet felismerni az agresszívabb tumorokat, továbbá felhívja a figyelmet az antiinvazív ágensek jövőbeni használatának szükségességére a GBM terápiájában.
1.
2.
3.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről4.
5.
1.
2.
Klinikai Onkológia
A rosszindulatú daganatok fenotípusának plaszticitása és az immunogén mimikri3.
Klinikai Onkológia
A szarkopénia mérése komputertomográfiával és jelentősége az onkológiai betegeknél4.
5.