Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 97
Hyperinflammatio és modulációja kritikus állapotú Covid-betegekben
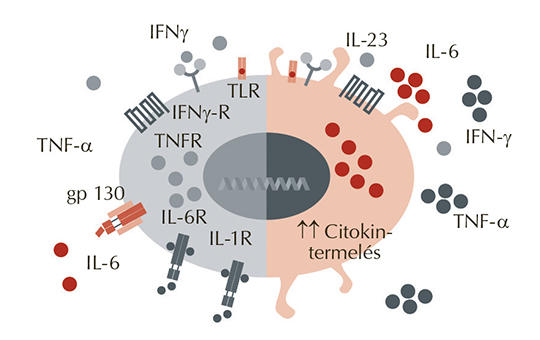
A Covid-19-járvány 2020-ban világszerte milliók életét követelte. Fatális kimenetelének hátterében legtöbbször súlyos légzési vagy többszervi elégtelenség áll. A folyamat patomechanizmusában valószínűleg fontos szerepet játszik a szervezet diszregulált immunválasza, csakúgy, mint szepszis esetében. Elsősorban a proinflammatorikus citokinek szérumkoncentrációja emelkedik meg a betegség során, ami felveti, hogy a monoklonális antitestekkel történő gyógyszeres kezelés, illetve a keringő citokinek extrakorporális, nem szelektív, adszorpciós eljárással történő megkötése kedvezően befolyásolhatja-e a betegség lefolyását és kimenetelét. A közlemény célja a citokinek Covid-19-ben betöltött szerepének, illetve az immunválasz modulációjáról szóló ismereteinknek rövid összefoglalása.
Ellentmondások a neurológiában: A sclerosis multiplex diagnózisának, követésének és terápiájának aktuális kérdései a patomechanizmus megközelítésével
A sclerosis multiplex relapszáló-remittáló és progresszív formái közötti határvonal sokszor nehezen megállapítható. A kórkép különböző klinikai megjelenései (fenotípusai) ellenére nincs egyértelmű biológiai oka az egyes formák elkülönítésének. Mind a primer progresszív, mind pedig a szekunder eseteknél ugyanis hasonló patológiai eltérések észlelhetők a gyulladásos infiltráció, az axonalis károsodás és a corticalis demyelinisatio vonatkozásában. Felmerül a kérdés, hogy a primer progresszív sclerosis multiplexet megelőzheti egy aszimptomatikus (fel nem ismert) relapszáló-remittáló fázis. A szekunder progresszív sclerosis multiplex meghatározásához a betegnek 4-es EDSS-értéke kell, hogy legyen. Következésképpen a klinikai progresszió a korai fázisban kevéssé követett a betegeknél. Ismert továbbá a relapszusoktól függetlenül előrehaladó progresszió, ami észlelhető a betegség relapszáló-remittáló fázisában. A háttérben zajló lappangó, parázsló celluláris/molekuláris folyamatok meghatározzák a klinikai történést, amik a gyógyszeres terápia fontos célpontjai lehetnek. Ugyanakkor a proinflammatorikus citokinek összefüggésbe hozhatók a rosszabbodó kognícióval. Ez a gyulladásos környezet igen komolyan közrejátszhat a relapszus alatt megfigyelt mentális állapot kialakulásában. A betegeknél a motoros (fizikai) rosszabbodást jóval megelőzően rejtett kognitív teljesítménycsökkenés észlelhető. A relapszáló-remittáló fázisban észlelt silent progression pedig kapcsolatban lehet az agyi atrophia előrehaladásával. Levonható tehát az a következetés, hogy a szekunder progresszív fázisban észlelt folyamat jóval előbb elkezdődhet. Ezek az adatok a sclerosis multiplex egységes szemléletét erősítik, és felvetik a lehetőséget, hogy a betegség valójában egy primer progresszív kórkép, amire relapszusok rakódnak.
Statinok hatása a Covid-19 kimenetelére
A SARS-hoz és a MERS-hez hasonlóan, a Covid-19 megbetegedésre is jellemző a gyulladásos reakció és az immunválasz szabályozási zavara. Súlyos lefolyású esetekben megemelkedik a gyulladásos citokinek koncentrációja, a neutrophil granulocyták száma, és lymphopenia alakul ki. A súlyos Covid-19 többek között hyperinflammatoricus állapottal, cardiovascularis zavarokkal és a vénás thromboembolisatio fokozott kockázatával jellemezhető.
A humán immunrendszer rendszerelvű megközelítése
A nukleotidpolimorfizmusok kutatása révén kiderült, hogy az autoimmun betegségek kialakulásában nagyon kis hatáserősséggel nagyon sok genetikai lokusz közreműködik, és itt is kiderült, hogy egy-egy kórkép molekuláris heterogenitása – pl. SLE esetén – milyen óriási. E betegségek kezelését forradalmasította a biologikumok rendszerimmunológiának köszönhető bevezetése.
A citokinek fájdalomkeltő szerepe a központi idegrendszerben – az anticitokin-terápia közvetlen analgetikus hatása
A krónikus fájdalom érzékelésében, továbbításában, feldolgozásában és az agyi fájdalomkép megformálásában nociceptiv, neuropathiás és centrális mechanizmusok vesznek részt. A kórokozó jelenlétét vagy a szövetkárosodást jelző és a védekezést riadóztató molekulák, az alarminok kóros folyamatok sorát indítják el, amelyek gyulladásos fájdalomingert váltanak ki. A gyulladáskeltő citokineknek a fájdalom idegrendszeri szinten való megjelenítésében van döntő szerepe. A folyamatos gyulladásos ingerek az idegsejtek perifériás és központi érzékenyítésével aktiválják a fájdalomérzéssel kapcsolatos agyi területeket és kialakítják az összetett fájdalomképet, a fájdalommátrixot. Az agyi funkcionális kapcsolatok hálózatokban működnek és funkcionális MRI-vel képezhetők le. A citokinek a neuronokat közvetlenül, vagy más neuromediátorok révén közvetve aktiválják. A citokinreceptorok megjelennek a nociceptorokon és a magasabb rendű neuronokon is, valamint a különféle nem neuralis sejteken, mint a microglia vagy az astrocyták. Az idegrendszerben szinte mindenütt fellelhető citokinek a tumornekrózis-faktor és az interleukin 6. Jeladási útvonalaik a nukleáris faktor κB és a Janus-kináz enzimrendszere. Ezért a gyulladáskeltő citokinek és a Janus-kináz elsőrendű terápiás célpontok. Az anticitokin biologikumok és a kismolekulájú kinázgátlók rheumatoid arthritisben csökkentik a fájdalmat és javítják a működőképességet. A fájdalomcsökkenés nagyobb, mint ami csak a gyulladás klinikai biomarkereinek csökkenésétől várható lenne. A célzott biológiai és kémiai-biológiai válaszmódosítók korai és gyors fájdalomcsökkentő hatását az agyban kifejtett közvetlen analgetikus hatásnak tulajdonítják.
Táplálkozási ajánlások a CoVID-19 miatti karantén idején
A karanténhoz társuló stressz alvászavarokat is okozhat, ami tovább fokozhatja a stresszt és ezáltal a táplálékbevitelt, ami egy ördögi kör kialakulásához vezethet. Fontos, hogy vacsorára olyan ételeket fogyasszunk, amelyek szerotonint vagy melatonint tartalmaznak vagy elősegítik ezeknek a szintézisét.
Az urogenitalis tractus folyamatos ellenőrzése COVID-19-ben
A Wuhan városában kirobbant COVID-19 vírusbetegségben 2020 áprilisára világszerte több mint 1,2 millióan fertőződtek meg, a járvány halálos áldozatainak száma pedig több, mint 64000-re nőtt. Bár a betegség klasszikusan légúti tünetekkel jelentkezik, az egyre növekvő tapasztalatok azt mutatják, hogy a fertőzés az urogenitalis tractus működésére is jelentős hatással lehet. Számos fertőzött betegnél akut vese-elégtelenség lépett fel, és ezeket a betegeket folyamatos dialízis kezelésben kellett részesíteni, de drámai változásokat véltek felfedezni a férfi nemi szervek működésében is.
COVID-19: Gondoljunk a citokinvihar-szindrómára és az immunszupresszióra
A 2020 március 12.-i adatok alapján a COVID-19 által okozott betegségnek 3,7 % a mortalitása, míg az influenzáé az előző évek adatai alapján kevesebb, mint 1 %. A rendelkezésre álló, gyarapodó adatok azt mutatják, hogy a súlyos betegek egy részében citokinvihar-szindróma jelentkezhet.
Veszélyeztetettek-e a magzatok a SARS-COV-2 fertőzéssel szemben?
Az Amerikai Orvosi Szövetség Folyóiratában (Journal of the American Medical Association) két cikk is megjelent a témában, egymástól független kínai kutatócsoportok (Dong és mtsai ill. Zeng és mtsai) által, amelyek felvetik 3 újszülött anyaméhben való koronavírus fertőződését.
A gyulladás szerepe a daganatok kialakulásában
A krónikus gyulladás (például pancreatitis, colitis, bronchitis) számos daganatféleség esetében a karcinogenezis fontos előmozdítója és a keletkező genetikai hibák egyik okozója is, az ismert karcinogének mellett. Az érintett szövetek hámjának folyamatos regenerációja mellett a krónikus gyulladás olyan intra- és extracelluláris környezetet teremt, amely kedvez a malignus transzformációnak és blokkolja az esetleges immunválasz kialakulását is. Legújabb ismereteink szerint a szolid daganatok maguk is intenzív krónikus gyulladást generálnak teljesen függetlenül attól, hogy magának a daganatnak a kialakulásában ez a folyamat szerepet játszott-e. Ennek kiváltó okai a daganatos necrosis és a daganatszövet által termelt gyulladásos citokinek. A daganatindukált gyulladásos reakció blokkolja a daganat elleni hatékony immunválaszt, és egyes elemeinek monitorozása a daganatos progresszió klinikai markere lehet.
1.
2.
3.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről4.
5.
1.
2.
Klinikai Onkológia
Hasnyálmirigyrák: az ESMO klinikai gyakorlati irányelve a diagnózishoz, kezeléshez, követéshez*3.
Klinikai Onkológia
Gyógyszerbiztonsági szemelvények – a múlt tanulságai és a jövő lehetőségei4.
5.