Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 218
Mikor érdemes bevenni a vérnyomáscsökkentőt? Reggel és/vagy este?
A vérnyomás cirkadián (24 órás) variabilitását állandó és változó (külső és belső) tényezők befolyásolják. Ezeknek és 24 órás ambuláns vérnyomás- monitorozással (ABPM) meghatározott hypertonia-fenotípusnak az ismeretében lehet az individuális kronofarmakológiai szempontú kezelést (a magas vérnyomás kronofarmakoterápiáját) megtervezni. Jelentős különbségek vannak a különböző időpontokban adagolt antihipertenzív gyógyszerek kronokinetikájában. Terápiás tartományuk, hatékonyságuk jelentősen függ a cirkadián időpontbeli adagolásuktól. Bár a legtöbb korszerű antihipertenzívum 24 órás hatású, de mégsem képesek minden időpontban a vérnyomást azonos mértékben csökkenteni. Az ACE-gátlók, az ARB-k és az alfa-receptor-blokkolók reggeli bevétele elsősorban a délutáni, kora esti emelkedést befolyásolják, az esti bevétel az éjjeli, hajnali emelkedéseket csökkenti. A kalciumcsatorna-blokkolók, a béta-receptor-blokkolók (kivéve karvedilol és labetolol) nem hatnak a cirkadián vérnyomásprofilra. Ezért nondipper hypertoniában, illetve hajnali emelkedéseknél a kétszeri: reggeli és esti adás hatékonyabb a reggeli egyszeri adásnál (általában este kisebb dózis elegendő). Az éjszakai vagy hajnali vérnyomás-emelkedések megfelelő kontrollját az este bevett gyógyszerrel lehet elérni. Releváns tanulmányok szerint jelenleg nincsenek egyértelmű evidenciák arra vonatkozóan, hogy az esti bevétel révén megelőzhetők a szervkárosodások vagy csökkenthetők a cardiovascularis események, ezért nem ajánlható a kizárólagos esti bevétel. Ez különösen igaz idős pácienseknél, mert olyan mértékű lehet az éjszakai vérnyomásesés, amely növelheti a néma cerebralis infarctusnak a kockázatát és coronariabetegeknél a myocardiumischaemia rizikóját.
Kinek a kezébe valók az SGLT-2-gátlók?
A sodium-glucose cotransporter 2-inhibitorok (SGLT-2-gátlók) használata számos cardiovascularis (CV) kórképben (szívelégtelenségben, koszorúér-betegségben, szívinfarktus és stroke után) bizonyítottan előnyös, emiatt 2-es típusú diabetes mellitusban (T2DM) évek óta részei az ajánlásoknak. A közelmúltban két klinikai vizsgálat is rávilágított arra, hogy az SGLT-2-gátlók mennyire jótékonyak a csökkent balkamra-funkcióval járó szívelégtelenségben (HFrEF) szenvedő betegekben, jelentősen csökkentve a szívelégtelenség miatti kórházi felvétel és a szív- és érrendszeri (CV) halálozás kockázatát, függetlenül attól, hogy a beteg diabeteses vagy nem. Ezáltal napjaink egyik legforrongóbb és legizgalmasabb kérdése tehető fel: Kinek a kezébe valók az SGLT-2-gátlók?
Az SGLT-2-gátlók haszna: túl a glykaemiás hatáson
Az utóbbi években a nemzetközi és hazai ajánlásokban az életmód-terápia kiegészítéseként a metformin a 2-es típusú cukorbetegek első vonalbeli gyógyszeres kezelésének preferált készítményeként szerepel, ellenjavallat hiányában. A nátrium-glükóz-kotranszporter-2-gátlók igazoltan lassítják a krónikus vesebetegség progresszióját, csökkentik a veseelégtelenség kialakulását, egyúttal csökkentik a pangásos szívelégtelenség miatti kórházi felvételi igényt és a szív- és érrendszeri halálozást a 2-es típusú cukorbetegekben, ez utóbbit főleg szekunder prevencióban. Jelenleg úgy tűnik, hogy a nagy cardiovascularis eseményeket és a renoprotektív hatást illetően a nátrium-glükóz-kotranszporter-2-gátlók nem egységesek. Ezzel szemben a szívelégtelenség miatti hospitalizációs igényre gyakorolt kedvező hatás csoporthatásnak tekinthető. Az összefoglaló közleményben a szerzők áttekintik a nátrium-glükóz-kotranszporter-2-gátlókkal kapcsolatos újabb adatokat, és ezen készítmények lehetséges szerepét a közeljövőben.
A ketontestek terápiás potenciálja cardiovascularis betegségben
A ketontestek cardiovascularis hatásai túlmutatnak az energetikán: vasodilatatorok, gyulladásgátló, vérnyomás- és testsúlycsökkentő hatással bírnak.
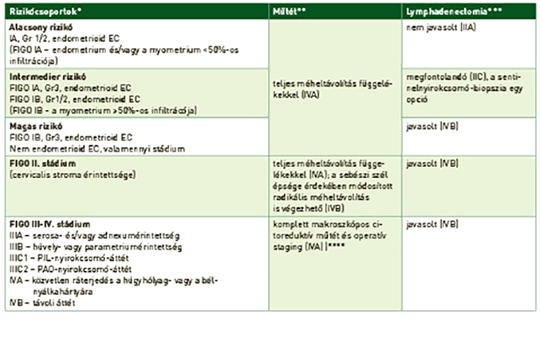
A méh rosszindulatú daganatainak korszerű onkológiai kezelése
Világviszonylatban évente közel 400 000 nőnél igazolódik méhtestrák, amely 2018-ban körülbelül 90 000 nő halálát okozta. Az esetek túlnyomó részét a méhnyálkahártya hormonérzékeny hámjából kiinduló endometriumcarcinomák (EC) alkotják. A sarcomák a méhtestrákok alig 3%-át adják. Az EC-k 80-85%-a jó prognózisú, mivel alacsony gradusú és korai stádiumban kerül felismerésre, amikor a műtét és az esetleges posztoperatív kezelés révén a gyógyulás reális terápiás cél. Az előrehaladott stádiumban diagnosztizált EC és a nem endometrioid altípusok esetén a prognózis lényegesen rosszabb. A magas rizikójú EC optimális adjuváns kezelésére irányuló vizsgálatok egy része még folyamatban van, illetve a bővülő molekuláris ismeretek újabb vizsgálatokat generálnak. A méhtestsarcomák esetében is a sebészi eltávolítás jelenthet kuratív megoldást, az adjuváns kezelésre vonatkozó evidenciák bizonytalanok, egyéni mérlegelést igényelnek. A modern onkoterápia érájában már nemcsak a betegségmentes élet meghosszabbítására, hanem az élet minőségének minél teljesebb megőrzésére is törekszünk. A nőgyógyászati onkológiában ezt jelenti a fertilitás vagy a funkcionáló ováriumok lehetőség szerinti megőrzése; a magas morbiditással járó szisztémás lymphadenectomia indikációs körének szűkítése; a kedvezőbb mellékhatásprofilú brachytherapia alkalmazása a teljes kismedencei besugárzás helyett. A modern onkoterápia az úgynevezett biológiai kezelések által az előrehaladott betegségek ellátásának is a részévé vált: kemoterápia mellett/után progrediáló esetekben a pembrolizumab az EC és a sarcomák esetén is alkalmazható mikroszatellita-instabilitás vagy magas tumormutációs terheltség esetén, míg az NTRK fúziós gén jelenlétében larotrectinib vagy entrectinib mint célzott tirozinkináz-gátlók javasolhatók. Az EC-k 70-80%-át kitevő mikroszatellita-stabil esetekben (nem endometrioid altípusokban is!) a pembrolizumab lenvatinibbel kombinációban adható a kemoterápia után. Az EC területén gyarapodnak továbbá az egyéb célzott terápiás szerekkel szerzett tapasztalatok is (anti-HER2 serosus carcinomában, mTOR-gátló kezelés, endokrin terápia, más immun checkpoint inhibitorok, tirozinkináz-gátlók, PARP-gátlók és kombinációs kezelések). A jelen munka a méhtestrákok onkoterápiájáról kíván rövid összefoglalást nyújtani az aktuális szakmai ajánlások és a folyamatban lévő vizsgálatok bemutatásával.
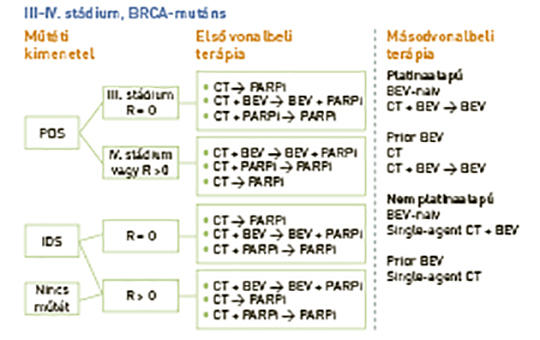
A petefészekrák kezelésének frontvonalában: a PARP-gátlók szerepének megújítása
Kiújult petefészekrákban a poli(ADP-ribóz)polimeráz- (PARP-) gátlókkal történő kezelések megváltoztatták a platinaérzékeny daganatok kezelését. Az új adatok szerint a PARP-gátlókat a kezelési algoritmus korábbi szakaszában kell alkalmazni. A kutatók számba veszik azokat a fázis III vizsgálatokat, amelyekben a PARP-gátlók hatását értékelték újonnan diagnosztizált petefészekrákok primer, illetve fenntartó kezelésében. Megvitatják a gyógyszerek hatásosságát és biztonságosságát az összes daganat, illetve a biomarkerek szerint válogatott daganatok klinikai vizsgálataiban, és összevetik a különböző vizsgálatok előnyeit és korlátait. Fontolóra veszik a jövő kutatásainak prioritásait – különös tekintettel a betegek kiválasztására és a jövőben alkalmazandó, egyelőre hiányzó gyógyszeres regimenek megalkotására. Négy fázis III vizsgálatban (SOLO-1, PAOLA-1/ENGOT-OV25, PRIMA/ENGOT-OV26 és VELIA/GOG-3005) PARP-gátlók használatával (olaparib, niraparib vagy veliparib) a progressziómentes túlélés jelentős javulását figyelték meg petefészekrákos betegekben. A vizsgálatok eltérő kialakítása (kezelés vagy fenntartó kezelés, egy gyógyszeres vagy kombinációs kezelés, bevacizumabbal vagy bevacizumab nélkül), a betegek kiválasztása (műtéti eredmény, biomarkerek elérhetősége, prognózis szerint), a résztvevők eredeti megválasztása (intention-to-treat, BRCA-mutációs vagy homológ rekombinációdeficites pozitív) befolyásolták a vizsgálatokból levonható következtetéseket. A teljes túlélési adatok még függőben vannak, hosszú távú biztonságossági adatok is csak korlátozottan állnak rendelkezésre. A PARP-gátlók sarkalatos szerepet játszanak az újonnan kimutatott petefészekrák-ellátásban, és befolyásolják a további kezeléseket. Ki kell választani azokat a betegeket és gyógyszereket, akiknél az eddigi alkalmazott kezelések a PARP-gátlóknál kevesebb haszonnal járnának.
A humán immunrendszer rendszerelvű megközelítése
A nukleotidpolimorfizmusok kutatása révén kiderült, hogy az autoimmun betegségek kialakulásában nagyon kis hatáserősséggel nagyon sok genetikai lokusz közreműködik, és itt is kiderült, hogy egy-egy kórkép molekuláris heterogenitása – pl. SLE esetén – milyen óriási. E betegségek kezelését forradalmasította a biologikumok rendszerimmunológiának köszönhető bevezetése.
A RAAS-gátlók pozitív hatása COVID-19-betegek körében
A metaanalízis célja annak megállapítása volt, hogy milyen hatással bírnak a hipertenzív, illetve bármely egyéb okból RAAS-gátlót szedő COVID-19-betegek morbiditására és mortalitására a SARS-CoV-2 vírus sejtbe lépését esetlegesen befolyásoló szerek.
Van-e hatásosságbeli különbség a PD-1, illetve PD-L1 gátlók között szolid tumorok esetén?
Az immunterápia, ezen belül különösen az immunellenőrzőpont-gátlók (ICI), amelyek a programozott sejthalál receptor-1 (PD- 1) és PD-ligand 1-et (PD-L1) célozzák meg, számos daganatféleségben a rákterápiának az egyik legfontosabb áttörését jelentik. A klinikai vizsgálatok növekvő számával egyre több összefoglaló érhető el az anti-PD-1 és az anti-PD-L1 kezelések eltérő klinikai hatásosságát illetően.
Az immunellenőrzőpont-gátlók alkalmazása Covid-19-fertőzés során
Már 2020. március első felében látszott, hogy a daganatos betegek Covid-19-fertőzése esetén jóval nagyobb a súlyos szövődmények kockázata, mint a nem daganatos fertőzötteknél (39% vs. 8%, p = 0,0003). Ha a betegek éppen kemoterápiát kaptak, vagy éppen műtéten estek át, még magasabb volt a kockázat. Ezért a kutatók rendszerint a kemoterápia és a műtét pár napos/hetes elhalasztását javasolták például Olaszországban is, főleg a hematológiai toxicitás és az immunszuppresszió miatt.
1.
2.
3.
4.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről5.
1.
2.
Klinikai Onkológia
A rosszindulatú daganatok fenotípusának plaszticitása és az immunogén mimikri3.
Klinikai Onkológia
A szarkopénia mérése komputertomográfiával és jelentősége az onkológiai betegeknél4.
5.