Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 218
Két dihidroorotát-dehidrogenáz (DHODH) gátló, a leflunomid és a teriflunomid hatásossága és biztonságossága Covid-19 esetén: narratív összefoglaló
A Covid-19-világjárványt okozó SARS-CoV-2 vírus és a gazdaszervezet interakciója egyre pontosabb részleteiben válik ismertté. Ezek alapján a preventív módon működő vakcinák fejlesztése mellett különféle támadáspontokon ható terápiás szerek előállítása és klinikai vizsgálata is folyamatban van. Egy ilyen gyógyszercsoportot jelentenek a dihidroorotát-dehidrogenáz (DHODH) gátlók, amelyek képviselői a leflunomid, illetve ennek aktív metabolitja, a teriflunomid. Kaur és munkatársai a Europen Journal of Pharmacology-ban megjelent cikkükben a DHODH-gátlók antivirális hatásmechanizmusát, biztonságosságuk és hatásosságuk bizonyítékait és lehetséges szerepüket a Covid-19 kezelésében mutatják be.
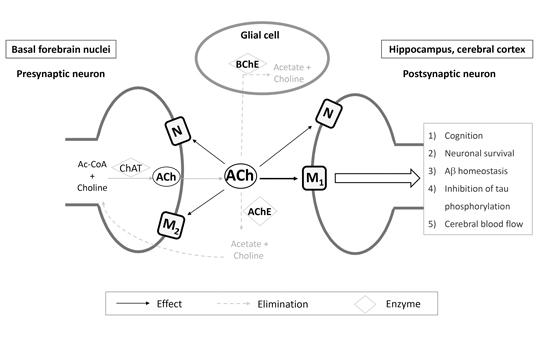
[A kolinészteráz-gátlók és a memantin használata Alzheimer- és nem Alzheimer eredetű dementiákban]
[Az öregedő társadalmakban a dementia morbiditása és mortalitása jelentős ütemben növekszik, kifejezett terhet róva így az egészségügyre, a gazdaságra és a társadalom egészére egyaránt. A betegek és gondozóik életminőségét és életkilátásait a mihamarabbi diagnózis és az elérhető kezelések megkezdése nagymértékben meghatározza. A rendelkezésre álló kolinészteráz-gátlók és a memantin megközelítőleg két évtizede az Alzheimer-kór terápiájának alappillérei, de az évek során egyre több tapasztalat gyűlt össze a nem Alzheimer-kór okozta egyéb dementiát okozó kórképekben való alkalmazásról is. Munkánk célja, hogy átfogó összefoglalót adjunk a kolinészteráz-gátlók és a memantin használatáról, jellemzőiről és hatásairól Alzheimer- és nem Alzheimer eredetű dementiákban.]
Koronavírus-betegség reumatológiai betegek körében – a megfertőződés, a súlyos lefolyás és a hatásos vakcináció esélyei
A gyulladásos és reumatológiai betegségekben szenvedők koronavírus-fertőzöttségének gyakorisága nem tér el jelentősen a helyi népesség fertőzöttségi arányaitól. A nagyobb adagú kortikoszteroiddal kezeltek, elsősorban a súlyosabb szisztémás autoimmun betegek megfertőződésének nagyobb a valószínűsége. A hospitalizáció, illetve a mortalitás esélye sem tér el lényegesen a népességi Covid-fertőzöttekétől. E tekintetben is kivételnek számítanak a nagyobb mennyiségű kortikoszteroidokkal és citosztatikumokkal kezeltek. A Covid-prognózist illetően az általában kockázatot jelentő társuló betegségek (a Covid előtti reumatológiai felmérések szerint) ugyanazok a gyulladásos és a nem gyulladásos reumatológiai betegek körében. Ezért nem a reumatológiai betegség miatt súlyos a Covid-kimenetel kockázata, hanem az időskor és az ebben az életkori csoportban egyaránt fellelhető cardiopulmonalis és anyagcsere-betegségek következtében. A gyulladásos reumatológiai/autoimmun betegek kezelésének fegyvertárából hipotetikus alapon a súlyos Covid kezelésére kiválasztott készítmények közül a dexamethason hatásossága bizonyított egyértelműen. Speciális betegcsoportokban kedvező hatása lehet az interleukin-6-antagonistáknak és a JAK-gátlóknak. A reumatológiai és az autoimmun betegségek kezelésére alkalmazott betegségmódosító gyógyszerek, köztük az antimetabolitok, az anticitokin immunológiai készítmények és a JAK-gátlók nem jelentenek Covid-kockázatot, adásukat nem kell megszakítani. Kivétel ez alól a korai B-sejteket közvetlenül elpusztító rituximabkészítmény, amely a súlyos kimenetel esélyét növeli a kezeltekben, feltehetően aktív betegségük és a gátolt humorális immunvédekezés miatt. A Covid-vakcináció szintúgy nem jelent speciális akut kockázatot reumatológiai és autoimmun betegek számára. Hosszabb távon még vizsgálandó, hogy az immunválasz erősségét és tartósságát reumatológiai betegekben a vakcináció speciálisan befolyásolja-e.
RAAS-gátló kezelés – Covid-pandémia
A SARS-CoV-2 okozta különböző méretű és lefolyású akut légzési szindróma ma az egészségügyi rendszerek legnagyobb kihívása világszerte. A Covid-19 klinikai képének kialakulásában döntő szerepe van a renin-angiotenzin-aldoszteron, valamint a kinin-kallikrein rendszernek, illetve ezen rendszereken belül két endopeptidáznak, az ACE és ACE-2 enzimeknek. Az ACE által stimulált Ang II/AT1R tengely káros hatásait (oxidáns, gyulladáskeltő hatás, vasoconstrictio) az ACE-2 által indukált AT2R- és MasR-aktivitás (antioxidáns, gyulladáscsökkentő hatás, vasodilatatio) ellensúlyozza. A SARS-CoV-2 azért okoz ilyen súlyos tüdő- és szisztémás gyulladást, mert az ACE-2-t, mint a tüdő fontos védelmi tényezőjét, károsítja a SARS-CoV-2 fehérjetüskéje az ACE-2-höz kötődéssel, ami az ACE-2-szint csökkenéséhez vezet. Ezzel párhuzamosan fokozott a bradikinintermelődés, amely a BKB1- és BKB2-receptorok révén ugyancsak erősíti a SARS-CoV-2 gerjesztette citokinvihart. Mivel a RAAS-gátló szerek (ACEI, ARB) különböző támadási helyeken és különböző mértékben befolyásolják a két említett szabályozó rendszert és enzimeket, sürgős volt szerepük tisztázása a Covid-fertőzés során, hiszen alkalmazásuk igen kiterjedt és nélkülözhetetlen pillére számos népbetegségnek (hypertonia, cardiorenalis anyagcsere-betegségek). A patofiziológiai és kísérletes adatok alapján jogosan feltételezhető, hogy Covid-fertőzésben a társbetegségekkel járó esetekben – kifejezetten az idős egyéneknél – a csökkent ACE-2-expressziót a RAAS-gátlók helyreállíthatják, és újra érvényesülni tud az elmaradt, vagy csökkent védőhatás. Ez a védőhatás mindkét RAAS-gátlóra érvényes. A klinikai vizsgálatok egyértelműen alátámasztják a különböző nemzetközi társaságok deklarált véleményét, miszerint a RAAS-gátlók alkalmazása nem növeli a Covid-19-előfordulást, illetve a súlyos, kritikus Covid-betegek megjelenésének kockázatát. Ennek értelmében az elindított RAAS-gátló kezelést folytatni lehet és szükséges a Covid-19 betegség kialakulása folyamán.
HFpEF-ben szenvedő hypertoniás betegek kezelése. A mineralokortikoidreceptor-antagonista (MRA), az angiotenzinreceptor-gátló neprilizininhibitor (ARNI) és a nátrium-glükóz kotranszporter-2 gátlók (SGLT-2-inhibitorok) szerepe
A megtartott szisztolés szíverejű szívelégtelenség (HFpEF) tünetes formájának prevalenciája gyakran okoz terápiás gondot a klinikusok számára. Számos társbetegség között a hypertonia az egyik leggyakoribb kísérő állapota, így annak kezelése, gondozása szintén megkülönböztetett figyelmet érdemel. A magas vérnyomás és a HFpEF egyidejű kezelésében felmerülő új gyógyszeres terápiás lehetőségeket tekintjük át az erre a célra tervezett vizsgálatok eredményeinek tükrében.
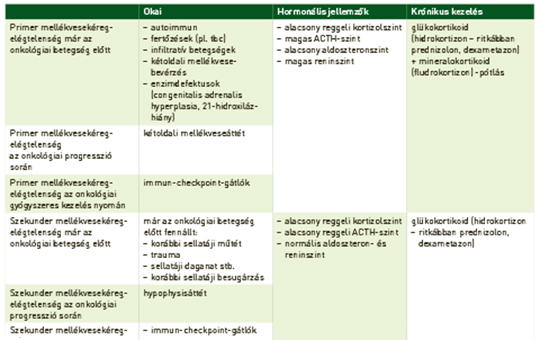
A mellékvesekéreg-elégtelenség jelentősége az onkológiai betegellátásban
A mellékvesekéreg-elégtelenség jelentősége összetett az onkológiai ellátásban. Egyrészt mellékvesekéreg-elégtelenségben szenvedő betegekben kialakulhat rosszindulatú daganat, ami kezelést igényel, másrészről rosszindulatú daganat következtében, illetve annak kezelése nyomán is kialakulhat mellékvesekéreg-elégtelenség. Az onkológiai betegség progressziója során a mellékvese kétoldali áttétje vagy, nagyon ritkán, a hypophysis áttéte vezethet mellékvesekéreg-elégtelenséghez. Az onkológiai kezelés során alkalmazott új immun-checkpoint-gátlók, opioidok és a tartós glükokortikoidkezelés is mellékvesekéreg-elégtelenséget okozhatnak. A mellékvesekéreg-elégtelenség felismerése, illetve kezelésének ismerete fontos, hiszen a kezelés elmaradása súlyos, akár fatális következményekkel is járhat. Ezen összefoglaló cikkben e klinikailag fontos területeket mutatom be.
Angiogenezis-gátlók és immunjelátviteli pontokra ható szerek kombinációja egymás hatásának potencírozására
A daganatok nem sebészi kezelésében mind az angiogenezis gátlásának, mind az immunfolyamatok befolyásolásának jelentős és egyre növekvő szerepe van. A tumoros neo-angiogenezis kedvezőtlenül befolyásolja az immunrendszer működését, ezért gátlása serkenti a kulcsfontosságú T-lymphocyták és azok működését támogató egyéb tényezők hatását, kedvezően befolyásolja a daganat mikrokörnyezetét, miközben az immunjelátviteli pontokra ható kezelés segít az érrendszer normalizálásában. A két támadáspont együttes befolyásolása ezért kedvező hatású lehet. A szerzők vesesejtes rákban, melanoma malignumban, nem kissejtes tüdőrákban, vastag- és végbél-, valamint hepatocellularis és emlőrákban mutatják be a két hatásmechanizmusú csoportba tartozó szerek alkalmazását és kombinálását, megállapítva, hogy sikerrel zárult fázis III vizsgálatok döntően a világos sejtes (vagy világos sejtes komponenst is tartalmazó) vesesejtes rákokban történtek. Hangsúlyozzák, hogy az immunterápiához általában szükséges az érzékenységet előrevetítő paraméterek (megfelelő PD-L1, MSI-H, dMMR, TMB-H) kimutatása, és a tumoragnosztikus kezelés terápiás filozófiája mellett is figyelembe kell venni a törzskönyvezett javallatokat.
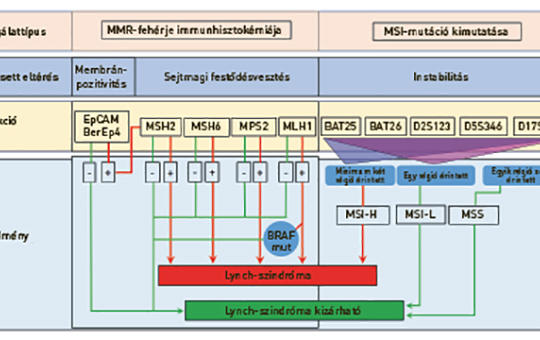
Mikroszatelliták mint a genom „szeizmográfjai”
A genetikai állomány fehérjét nem kódoló, monotonon ismétlődő, 1–6 nukleotidot tartalmazó szakaszain, a mikroszatellitákon a DNS-kettőződésért felelős polimerázok könnyen hibáznak. Így azok rövidülnek vagy hosszabbak lesznek. Ha az ilyen típusú DNS-hibákat javító enzimek működőképesek, a mutációk kijavítódnak. Ha nem, akkor különböző hosszúságú szakaszokként, instabil formában adódnak át az utódsejtekbe. Nemcsak korán jelzik a fokozott mutációs hajlamot, hanem önmagukban is, keretleolvasási problémát okozva, továbbiakat generálnak. Következésképpen a mikroszatellita-instabil (MSI) daganatok nagyobb arányban fejeznek ki idegen antigéneket, mint ezen eltérést nem mutatók, ami a tumorellenes immunválasz fokozott hatékonyságát valószínűsíti. Az MSI tehát nemcsak a genetikai instabilitásra, hanem az immunellenőrzőpont-gátló szerek hatásosságára is utal. Jelenlétét lehet közvetlenül, nukleotidfelbontási szintű PCR-alapú eljárással vagy közvetve, a hibajavító fehérjék kimutatásával, immunhisztokémiával vizsgálni, de ma már új generációs szekvenálási adatokból és mesterséges intelligencia képi elemzésből is kinyerhetők ilyen információk. Az MSI-meghatározás módszertanát és klinikai jelentőségét foglaljuk össze.
Telmizartán a vesevédelemben és az antihypertensiv kezelésben
A vese védelme különösen fontos terület, hiszen a hypertonia és a vesekárosodás fokozott cardiovascularis kockázattal jár együtt, ami végül végstádiumú veseelégtelenséghez vezet, és nagyobb mértékű mortalitást eredményez. A diabeteses és nem diabeteses eredetű, elsősorban hypertensiv nephropathiás vesekárosodás esetén a vérnyomáscsökkentő szerek közül a proteinuriát is mérséklő ACE-gátlók és az ARB-k a leghatásosabb vesevédelmet biztosítják. A telmizartánnal végzett nagyszámú nemzetközi és hazai vizsgálat elegendő bizonyítékot adott a szer antihypertensiv, renoprotektív hatását illetően. A betegek a célvérnyomásértéket és a morbiditási eredményeket kedvező mellékhatásprofil mellett érték el. A NEAK adatainak elemzéséből egyértelmű, hogy az orvosok gyógyszerválasztásában és gyógyszerfelírási szokásaiban jól megfigyelhető a nemzetközi és hazai társaságok ajánlásaiban megfogalmazottak elfogadása.
Hypertonia, COPD és Covid-19. Fókuszban az antihipertenzív terápia
A hypertonia gyakori társbetegsége a krónikus obstruktív tüdőbetegség, ami gyakran elkerüli a kezelőorvosok figyelmét. A kezelés kiválasztásakor ismerni kell mindkét kórkép patomechanizmusában részt vevő tényezőket. Kiemelendő a hypoxia, a szimpatikus idegrendszer tónusának fokozódása és a renin-angiotenzin-aldoszteron rendszer aktivációja. Mindkét betegségben nagy szerepe van az érfalak károsodásának, az endotheldiszfunkciónak. A terápia célja a kockázati tényezők megszüntetése, a vérnyomás normalizálása, továbbá a cardiocerebrovascularis, renalis és pulmonalis károsodások megelőzése, következésképpen a betegek élettartamának meghosszabbítása és életminőségük javítása. A Covid-19-ben szenvedő betegek állapotát jelentősen rontja a hypertonia és a COPD is, mert fokozzák a betegség súlyosságát, és növelik a hospitalizált betegek arányát, valamint a mortalitást is. A hypertonia kezelésében COPD és Covid-19 fennállása esetén is kiemelendőek a renin-angiotenzin-aldoszteron rendszert gátló gyógyszerek, így az angiotenzinkonvertáló-enzimet gátlók vagy az angiotenzin-II-AT1-receptorantagonisták. Különös figyelem fordult a mineralokortikoidreceptor-antagonista spironolakton kedvező hatására is. Szükség esetén a többi vérnyomáscsökkentő szer (kalciumantagonisták, tiazid típusú diuretikum, nagy szelektivitású β1-receptor-antagonisták) is kiegészítheti a kezelést. A COPD terápiájában alkalmazott hosszú hatású β2-receptor-agonisták, a muszkarinreceptor- antagonisták és az inhalációs kortikoszteroidok, illetve ezek kettős, esetenként hármas kombinációi alkalmazhatók hypertonia és COPD esetén is. Fontos megjegyezni, hogy a statinkezelés és a D3-vitamin is javíthatja a Covid-19-ben szenvedő betegek állapotát.
1.
2.
3.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről4.
5.
1.
2.
Klinikai Onkológia
Hasnyálmirigyrák: az ESMO klinikai gyakorlati irányelve a diagnózishoz, kezeléshez, követéshez*3.
Klinikai Onkológia
Gyógyszerbiztonsági szemelvények – a múlt tanulságai és a jövő lehetőségei4.
5.