Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 138
Az onkológiai gyógyszerész táguló szerepköre
A technológiai haladás felszabadította a gyógyszerészeket, akiknek ma már nem kell a gyógyszerkiadás biztonsági ellenőrzésére fókuszálniuk, és egyre több betegágy melletti feladatot is vállalhatnak, részt vehetnek akár az őssejttranszplantáció kivitelezésében vagy a farmakogenomikai eredmények értelmezésében is.
Az immunellenőrzőpont-gátlók alkalmazása Covid-19-fertőzés során
Már 2020. március első felében látszott, hogy a daganatos betegek Covid-19-fertőzése esetén jóval nagyobb a súlyos szövődmények kockázata, mint a nem daganatos fertőzötteknél (39% vs. 8%, p = 0,0003). Ha a betegek éppen kemoterápiát kaptak, vagy éppen műtéten estek át, még magasabb volt a kockázat. Ezért a kutatók rendszerint a kemoterápia és a műtét pár napos/hetes elhalasztását javasolták például Olaszországban is, főleg a hematológiai toxicitás és az immunszuppresszió miatt.
[Longitudinális extenzív transzverzális myelitisként jelentkező idegrendszeri lymphoma]
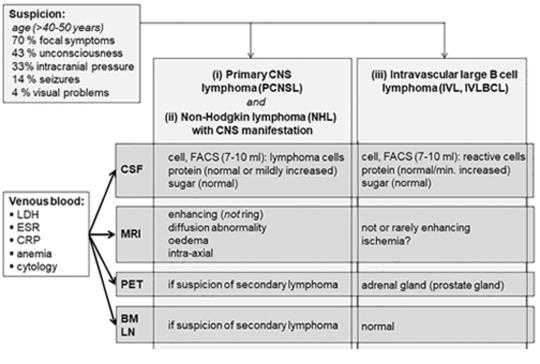
[Célkitűzés – Két, kifejezetten ritka, longitudinális extenzív transzverzális myelitisként (LETM) jelentkező, szubakut lefolyású, post mortem kórismézett, intravascularis, nagy B-sejtes, valamint szekunder T-sejtes idegrendszeri lymphoma bemutatása. A diagnosztikus problémák, a meg - tévesztő radiológiai és szövettani vizsgálatok okainak keresése, és a tennivalóink megfogalmazása ezekben a nehezen diagnosztizálható betegségekben, eseteink és másutt közölt esetek alapján. Módszer, esetismertetések – Neurológiai osztályra való felvételekor a 48 éves nő parapareticus volt, az MR-vizsgálat LETM-re utalt, de a kezelés hatástalan maradt. Pneumonia és befolyásolhatatlan polyserositis miatt ápolásának negyedik hetében meghalt. A patológiai vizsgálat intravascularis diffúz nagy B-sejtes lymphomát (IVL) derített fel. Második esetünkben, egy 61 éves férfinél fejfájás és paraparesis miatt végzett MR-vizsgálat gyulladás látszatát keltő, bitemporalis elváltozást és LETM-et állapított meg. A vizsgálatok eredménytelenek maradtak, az IVL gyanúja miatt végzett áramlásos citometria és az izombiopszia is. Mellkasi, hasi CT-vizsgálat a bal tüdőben, kis területen, gyulladásos gócos elváltozást, a jobb mellékvesében adenomát talált. Az érintett temporalis területből neuronavigációval vett minta T-sejt mediálta meningoencephalitisre utalt, diffúz nagy B-sejtes lymphoma lehetőségét kizárta. A beteg állapota fokozatosan romlott, a kórházi felvételt követő hatodik héten meghalt. A patológiai vizsgálat során a mellékvesével összefüggő, adeno - má nak vélt daganat, valamint a pancreasfarokban és a tüdőben talált elváltozás perifériás T-sejtes lymphomának bizonyult, ugyanúgy, mint az agyban és a gerincvelőben talált elváltozások. A lymphoma megtévesztően gyulladás látszatát keltette a szövettani mintákban, ugyanúgy, mint az MR-vizsgálatoknál. Következtetések – Lymphoma manifesztálódhat LETMként. Etiológiailag bizonytalan, atípusos LETM esetén, 40 évesnél idősebbeknél, eseteinkre és előzőleg közölt ese - tekre is hivatkozva, a rutinkivizsgálás részeként, hangsú - lyozottan minél hamarabb random bőrbiopszia javasolt (sub cutan zsírszövettel együtt), a comb és a has bőréből. A lelet, kiderítve az intravascularis lymphomát, megteremti az agresszív kemoterápia feltételeit. Ezzel egyidejűleg a liquoráramlási citometriás vizsgálata is javasolt. A bőrbiopszia negativitása esetén, ha lymphoma gyanúja továbbra is fennáll, mintavétel javasolt esetleges szisz té - más primer gócból (csontvelőből, nyirokcsomóból vagy mellékveséből), ha ez eredménytelen, a spinalis elváltozással rendszerint egyidejű cerebralis gócok egyikéből, az IVL, a diffúz nagy B-sejtes lymphoma, de a ritka Tsejtes lymphoma kizárására is, vagy bizonyítására.]
Egy biosimilar gyógyszer kifejlesztése és tízéves története a binocrit® példáján keresztül
A szabadalmak lejárata számos biológiai termék esetén alternatív változatok kifejlesztésére sarkallta a gyógyszergyárakat. Ezeket a változatokat „biosimilar” termékeknek nevezzük, amelyek minősége, biztonságossága, hatásossága a már engedélyezett (licenccel rendelkező) gyógyszerekéhez hasonló (amely utóbbiakat referenciagyógyszereknek is szokás nevezni). Az onkológiában megjelent első biosimilar gyógyszerek az alapkezelések mellé társuló szupportív kezelések gyógyszerei voltak, mint például a filgrasztim vagy az epoetin. A Binocrit® (HX575) az epoetin-alfa biosimilar változata, amelyet az onkológiában a kemoterápia által indukált anaemia (CIA) kezelésére használnak. A Binocrit® biosimilarként való kifejlesztésének és engedélyeztetésének folyamata során először kiterjedt analitikai összehasonlításokat végeztek a referencia epoetin-alfával. Ezután következett a klinikai fejlesztés: a fázis I farmakokinetikai/farmakodinamikai vizsgálatok során igazolták az új szer és a referencia-gyógyszer közötti bioekvivalenciát, majd egy fázis III vizsgálatban bizonyították a CIA-ban való terápiás hatásosságot is. Törzskönyvezése óta a Binokrit® ma már kiterjedten használatos a mindennapi klinikai gyakorlatban. Már sok-sok adattal igazolható, hogy a Binocrit® segítségével a daganatos betegek kezelése során kialakuló CIA hatásos és jól tolerálható lehet.
A kemoterápia daganatkeltő hatása
Kemoterápia nélkül a felfedezett daganatos betegségek ötéves túlélési rátája – daganatfüggően – 0–15% között lenne, a jelenlegi terápia alkalmazásával 17-85%. Ugyanakkor számos figyelmeztetés hívja fel a figyelmet a kemoterápia által indukált nemkívánatos mellékhatások, legfőképpen a lehetséges tumorindukciós képesség veszélyeire, ami az öt éven túl gyógyult betegek 5-10%-át is érintheti. A szisztémás kemoterápiában használt egyes gyógyszerek (alkilálószerek, etopozid, arzén-trioxid) képesek a szervezet egészséges sejtjeiben mutációt okozni, amivel megnő a valószínűsége annak, hogy a mutációt szenvedett sejtek egy későbbi (szekunder) daganatképződést indítsanak el. A mutagén hatások mellett egyes kemoterapeutikumok a szervezet normális myeloid és epithelialis sejtjeire fejtenek ki olyan hatásokat, amelyek a szöveti mikrokörnyezet átalakításával megteremtik a malignus transzformáció lehetőségét. Ebben a folyamatban igen fontos szereplők a tumorokkal asszociáló makrofágok (TAM), amelyek a daganatsejt által szekretált faktorok és mikroszómák hatására megváltoztathatják génexpressziós mintázatukat, és prokarcinogén szignálokkal segítik a tumorsejtek megmaradását, invazivitását, csökkentik a citotoxikus T-sejtek aktivitását. Mindezen okok miatt kiemelten fontos az, hogy a daganatkeltő mutagénekkel dolgozó orvosok, gyógyszerészek, technikusok és nővérek ne kerüljenek közvetlen érintkezésbe ezekkel a veszélyes anyagokkal, hanem használjanak megfelelő védőfelszerelést.
Hematológiai betegek kezelése a COV-19 járvány idején
A British Journal of Haematology levelezési rovatában megjelent közlemény a SARS-CoV-2 koronavírus által okozott COVID-19-fertőzés miatt a különösen veszélyeztetett betegcsoportok közül a hematológiai betegek járvány idején való kezelésére, a folyamatos gondozás alatt álló betegek esetében pedig elsősorban a kockázatokat csökkentő lehetőségekre összpontosít.
Petefészekrákban szenvedő betegek nem sebészi kezelése
A petefészekrákban szenvedő betegek kezelésében alapvető a kellően radikális műtét, amely az egyéb módszerek eredményességét is meghatározza. Az ezt követően, egy ülésben végzett hyperthermiás intraperitonealis kemoterápia 40,5–42,5 Celsius-fokos citosztatikus oldat perfúziójával történik. A szisztémás kezelések megválasztásában a hat hónapos progressziómentesség a mérföldkő, ezentúl platinaszenzitív, ezen belül -refrakter vagy -rezisztens betegségről van szó. A citosztatikus kezelés fejlődése az alkilálószerektől a platinaszármazékokon át a paklitaxel alkalmazásáig terjed, különféle kombinációkkal, egyre jobb eredményekkel és mind kevesebb mellékhatással. A célzott terápiában az érújdonképződés-gátlók (főleg a bevacizumab) és a DNS-hibák javítását megakadályozó, PARP-gátlók a legjelentősebbek; ez utóbbiak esetében általában a platinaérzékenység feltétel, míg a BRCA-mutáció már nem mindig követelmény. Az utóbbi időben az immunterápiával kapcsolatban is ígéretes vizsgálatok folynak. A hormonkezelés fő előnye a jó tolerálhatóság. A gyógyszerek alkalmazásának sikerei mellett visszaszorulni látszik a sugárterápia, pedig a teljes peritonealis felszín ellátása – különösen a korszerű besugárzási technikák alkalmazása mellett – a kemoterápia alternatívája lehet, a palliatív irradiáció pedig a tünetek csökkentése mellett a gyógyszermentes időszakot is megnyújthatja, s a kombinálás lehetőségei további távlatokat nyitnak meg.
Húgyhólyagdaganat neoadjuváns és palliatív gyógyszeres ellátása
Az izominvazív, lokális hólyagtumoros betegek túlélése kedvezőbb, ha a cystectomiát neoadjuváns vagy adjuváns platinatartalmú kemoterápia egészíti ki. A neoadjuváns ciszplatinbázisú kemoterápia hatására, metaanalízisek alapján, 5-16%-os ötéves túlélési benefit érhető el. A neoadjuváns kemoterápiára jól reagáló betegeknél (patológiai komplett remisszió aránya 12-50%) még kedvezőbb a kimenetel. A cystectomia három hónapon túli késlekedésének nincs kedvezőtlen hatása a túlélésre, ha a műtét előtt kemoterápia történik. Az adjuváns fázis III vizsgálatok és metaanalízisek eredményei kevésbé egyértelműek, de összességükben kedvező trend észlelhető a kemoterápia hatására a túlélésben, különösen pT 3/4 és/ vagy N+ (valamint high grade vagy margin pozitív) esetekben. A platinabázisú kemoterápiás kezelés utáni progresszió esetén másod- és többed-, valamint ciszplatinra alkalmatlan betegeknél PD-L1-expresszió esetén első vonalban is alkalmazható immunterápia hatására a betegek túlélésének és a tumorválasz időtartamának eredményei igen biztatóak, hatékonyabbnak látszanak az adott stádiumokban eddig alkalmazott kemoterápiás szerek publikált adatainál. A legújabb irányokban az immunterápia neoadjuváns, adjuváns, valamint kemoterápiával kombinált alkalmazása is klinikai vizsgálatok értékelése alatt áll, amelyek korai adatai kiemelkedően perspektivikusnak tűnnek.
Milyen újdonságokat hozott a 2019-es ESMO-kongresszus a tüdődaganat kezelésében?
Az elmúlt években jelentős áttörést jelentett a tüdődaganat kezelésében az immunterápiák és az új célzott terápiák hódítása. Több lehetőségünk van arra, hogy a beteget célzott terápiával, immunterápiával, kemoterápia és immunterápia kombinációjával, sőt immunterápia és immunterápia kombinációjával kezeljük. Meg kell találnunk, hogy melyik betegnek melyik a leghatékonyabb kezelés. Ezzel a betegeknek jó életminőségben további éveket adhatunk. A 2019-es ESMO-kongresszus újabb lehetőségeket adott számunkra a kezelést illetően.
Immunonkológia
2017. MÁRCIUS 01.
Hosszú távú túlélés előrehaladott nem kissejtes tüdődaganatban
A sebészi reszekció, a platinabázisú kombinált kemoterápia, a sugárkezelés és napjaink-ban az újabb terápiás lehetőségek, a célzott biológiai terápiák javítottak ugyan a tüdőrák túlélési eredményein, a betegségnek mégis igen magas a letalitási indexe. A tüdőrák ötéves túlélése mindössze 14%, Magyarországon ez az átlag rosszabb, csupán 8-10%. Retrospektív vizsgálatok történtek, hogy feltárják az előrehaladott stádiumú (III-IV. stá-diumú) nem kissejtes tüdőrák ötéves túlélőinek jellemzőit, de egyértelmű prognosztikai paramétereket nem találtak. Jelen összefoglalóban a nem kissejtes tüdőrákban immun-terápiával szerzett hosszú távú túlélési eredményeket ismertetjük, amely új, ígéretes perspektívát jelent a daganatos betegek ellátásában.
1.
2.
3.
4.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről5.
1.
2.
Klinikai Onkológia
A rosszindulatú daganatok fenotípusának plaszticitása és az immunogén mimikri3.
Klinikai Onkológia
A szarkopénia mérése komputertomográfiával és jelentősége az onkológiai betegeknél4.
5.