Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 116
A vérnyomáscélérték-tartományok elérésének vizsgálata telmizartán és amlodipin fix dózisú kombinációs készítmény alkalmazása során a háziorvosi gyakorlatban
Előzmények: A hypertonia ellátásáról szóló aktuális európai és hazai irányelvek egyszerű és jól alkalmazható kezelési stratégiát javasolnak a kezelés hatékonyságának növelése érdekében. Ennek fontos eleme a kezdő lépésként alkalmazott RAS-blokkoló és kalciumantagonista vagy diuretikum fix dózisú, egytablettás kombináció alkalmazása. Elsődleges célkitűzés: A 2018-as ESC/ESH, az artériás hypertonia kezelésére vonatkozó szakmai irányelveknek megfelelő vérnyomáscélérték-tartományt elérők arányának meghatározása a telmizartán és amlodipin fix kombinációs terápia indítását követő 12 hetes kezelési periódus végén, a rendelőben mért vérnyomásértékek alapján, háziorvosi praxisban kezelt betegek körében. Betegek és módszerek: A többcentrumos, beavatkozással nem járó, prospektív adatgyűjtés során 63 háziorvos 729 beteget vont be a vizsgálatba. 717 beteg részesült a vizsgálati készítménnyel kezelésben (intention-to-treat [ITT] populáció) és 690 beteg esetében volt az elsődleges vizsgálati végpont meghatározható (per protocol [PP] populáció). A vizsgálat során két vizit volt, vérnyomásmérésre minden beteg esetében a beválasztáskor, illetve a második, egyben záró vizit alkalmával került sor. Eredmények: Az ITT-populációt 357 férfi és 360 nő alkotta, átlagéletkoruk 62±12 év volt, a betegek több mint 55%-a 65 évesnél fiatalabb volt. A rendelői vérnyomás átlaga az első viziten 150±17/88±10 Hgmm volt, míg a második vizitre (12. hét) a vérnyomásértékek 130±8,1/78±6,1 Hgmm-re csökkentek (p <0,05, minden esetben). A pulzusszámértékek is csökkenést mutattak a kezelés során (80±9,8/min értékről 75±6,3/min értékre). A 2018-as irányelvek szerinti optimális szisztolés célértéket az első viziten a betegek 10,1%-a , míg a második viziten a betegek 51,6%-a érte el. Az optimális diasztolés célértéket elérők aránya az első vizit alkalmával 15,8%-nak, míg a második viziten 54,1%-nak bizonyult. Az első viziten mindössze a betegek 5,5%-a érte el egyidejűleg az irányelvek szerinti szisztolés és diasztolés célvérnyomást. Ezzel szemben a második viziten a betegek 33%-a érte el egyidejűleg a számára kitűzött irányelvek szerinti optimális szisztolés és diasztolés célvérnyomásértékeket. Szintén nőtt a vizsgálat során azok aránya, akik a jelenlegi ESC/ESH irányelvek szerinti elsődleges célvérnyomásértéket (<140/90 Hgmm) érték el. Kiinduláskor a betegek 19,2%-ának volt a vérnyomása 140/90 Hgmm alatt, ami a vizsgálat végére 87,1%-ra emelkedett. A betegek jól tolerálták a telmizartán/amlodipin fix kombinációt, 95%-uk a vizsgálat befejezését követően is tovább szedte a készítményt. Konklúzió: Ez a való életet tükröző vizsgálat is azt bizonyítja, hogy az irányelvek szerint alkalmazott fix kombinációs telmizartán/amlodipin kezeléssel a betegek jelentős hányadánál már 12 hetes kezelés során el lehet érni a célvérnyomás-tartományt, de a betegek többségénél további dózisemelés vagy kombinációs kiegészítés szükséges a megfelelő vérnyomáskontroll elérése érdekében.
Jövő Unikornisa Díj a rákdiagnosztikát segítő fejlesztésért
A Digital Europe kereskedelmi szövetség ebben az évben a Peták István és Schwab Richárd kutatóorvosok által alapított Oncompass Medicine molekuláris diagnosztikával és precíziós orvoslással foglalkozó céget díjazta a Jövő Unikornisa Díjával. A kitüntetést azon technológiai vállalkozásoknak adományozzák, amelyek jövőbeli értéke meghaladhatja az egymilliárd dollárt. Az Oncompass Medicine-t 17 európai ország legkülönfélébb területeken működő vállalkozásai közül választották ki. Az elismerést Mariya Gabriel az EU innovációért felelős biztosa adta át virtuálisan a magyar biotechnológiai cégnek 2021. február 4-én, a rák világnapján. A Jövő Unikornisa Díjat a kutatóorvosok a daganatos betegek célzott terápiájának segítésére fejlesztett orvosi szoftverrel érdemelték ki. A Real-Time Oncology Treatment Calculator (TM) elnevezésű informatikai eszköz példátlanul sok, 405 ráktípusban, 52 ezer mutáció esetén, 26 838 orvosbiológiai szabály alapján, 1417 gyógyszerhatóanyag közül képes rangsorolni az adott beteg betegségéhez és genetikai profiljához kijelölhető, legjobb reményekkel kecsegtető terápiákat. Mindehhez pedig 0,02 másodpercre van szüksége. Peták István évtizedek óta foglalkozik molekuláris rákdiagnosztikával, személyre szabott precíziós onkológiával, célzott gyógyszerfejlesztéssel. A kutató a díj alkalmából adott interjút folyóiratunknak.
[Új patogén mutáció következtében kialakuló karnitin-palmitoil-transzferáz II-hiánnyal magyarázható ismétlődő rhabdomyolysis]
[A karnitin-palmitoil-transzferáz II- (CPT II-) hiány egy autoszomálisan öröklődő anyagcsere-rendellenesség, amelyben a hosszú láncú zsírsavak β-oxidációja hiányos. A klinikai megjelenés különféle formában lehetséges; súlyos formájában jelentkezik újszülöttkorban és infantilis időszakban, míg iskolás- és serdülőkorban a kevésbé súlyos myopathiás formában jelentkezik. Bár a rhabdomyolysisrohamok súlyossága változó, a klinikai lefolyást esetenként akut veseelégtelenség komplikálhatja. Az acilkarnitin-elemzés segíthet a CPT II diagnosztizálásában, de az eredmény normalitása nem jelzi a betegség hiányát. Erős gyanú esetén genetikai elemzést kell végezni. Ebben a tanulmányban egy 15 éves fiú beteg esetét mutatjuk be, akinek két, fertőzés, illetve éhezés által kiváltott rhabdomyolysisrohama volt. Az acilkarnitin-elemzés eredménye normális volt, a kórtörténet értékelésénél figyelembe vettük a CPT II-hiányt, és kimutattuk a CPT II gén c.137A> G (p.Gln46Arg) új patogén homozigóta mutációját. A CPT II-hiány a metabolikus rhabdomyolysis egyik leggyakoribb oka az ismétlődő rhabdomyolysisepizódoktól szenvedő betegek esetén.]
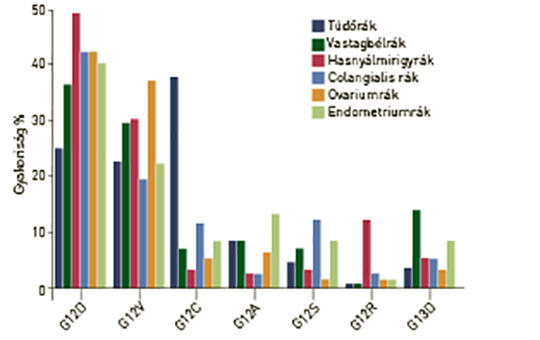
A (K)RAS-mutáció molekuláris epidemiológiája emberi daganatokban
A RAS onkogén mutációja a leggyakoribb génhiba emberi daganatokban, és a három családtag közül a K-RAS-é a leggyakoribb, amit az N-RAS követ. A tipikus K-RAS-mutáns daganatok a hasnyálmirigyrák, vastagbélrák és tüdő-adenocarcinoma, amelyekben a mutáns variáns allélok gyakorisága igen heterogén, aminek hátterében eltérő karcinogenezis áll. A RAS-mutáns daganatok genetikai sokszínűségét tovább fokozza, hogy a mutáns allél homo- vagy heterozigóta formában van-e jelen. A sokszínűség egy másik forrása az, hogy a különféle daganatokban a K-RAS-mutánsok esetében sajátos kísérő mutációs mintázatú altípusok lehetnek. Mindezeknek az a következménye, hogy a K-RAS-mutáns daganatok biológiai viselkedése és nagy valószínűséggel terápiás érzékenysége is nagyon heterogén lehet. A K-RAS-inhibitorok klinikai debütálásával ezeknek a kérdéseknek egyre nagyobb jelentősége lesz.
Hypertonia és Nephrologia
2020. NOVEMBER 04.
Hypertonia és Covid-19 – II. rész
A szerzők áttekintik azokat a komponenseket és mechanizmusokat a keringésszabályozásban alapvető jelentőségű két nagy regulációs rendszerben, amelyek belső egyensúlya és kapcsolatai a SARS-CoV-2 fertőzés során kórosan változnak, és ezáltal fokozzák a súlyos klinikai állapotba torkollással fenyegető tüdő- és szisztémás gyulladás állapotot. Megvizsgálják azt a kérdést, hogy a fertőző ágens szervezeti celluláris behatolásának potenciális elősegítésén túl, az áldozatok között kiugróan magas arányszámú idős hypertoniás betegek RAS-gátló gyógyszerelése hogyan befolyásolja ezeket a változásokat, feltételezhető-e különbség az ACEi és ARB támadáspontú kezelési rendszer anti-, proinflammatorikus befolyása között a Covid-19-járványban. Az áttekintés a koronavírus-fertőzésre adott közvetlen immunológiai választ jelentősen meghaladó gyulladás patomechanikai hátterére fókuszál: az idős hypertoniás betegeknek alapállapotban is fennálló immunmódosulásainak jelentőségére és a kulcskomponensekre, mint angiotenzin-II, ACE-2, angiotenzin- 1–7, bradikinin, ARB, ACEI. A következtetésben a SARS-CoV-2 fertőzött (idős) hypertoniás betegek RAS-gátló kezelésében a támadáspont optimalizálásának mérlegelése ajánlott.
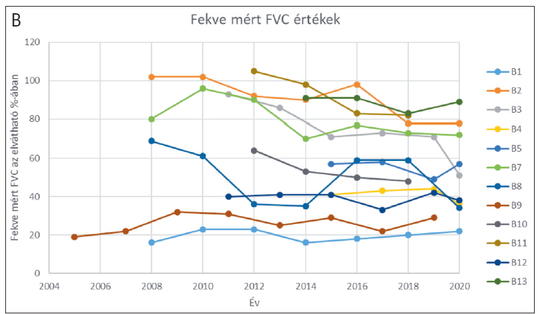
A késői kezdetű Pompe-kórban szenvedők enzimpótló kezelésének hosszú távú követése
A Pompe-kór (PD) egy ritka lizoszomális tárolási betegség, amit a GAA gén mutációja következtében kialakuló α-glükozidáz (GAA) enzim elégtelen működése okoz. Az enzimdeficientia a glikogén lizoszomális felszaporodásához vezet. A betegségnek két klinikai formája ismert, az újszülöttkori, valamint a késői forma. Jelenleg a betegség hátterében a GAA génnek közel 600 mutációja ismert. A kaukázusi populációban a késői forma hátterében a c.-32-13T>G mutáció a leggyakoribb, az allélfrekvencia közel 70%. A Pompe-kórt enzimpótló terápiával (ERT) tudjuk kezelni, kéthetente Myozyme infúzió adásával. Közleményünkben 13, több mint öt éve kezelt, késői kezdetű formában szenvedő beteg hosszú távú követését mutatjuk be. A leghosszabb követési idő 15 év volt. A kezelés eredményességének megítélésére évente mértük a 6 perces járótávolságot és a légzésfunkciót. Az adatok alapján a 6 perces járótávolság az enzimpótló kezelés indítása után körülbelül 3-4 évig javult, ezt követően az esetek többségében a megtett távolság csökkent. A több mint 10 éves követés után a kezdeti 6 perces járótávolsághoz képest romlást tapasztaltunk az esetek 77%-ában, javulást az esetek 23%-ában. A követés ideje alatt mindössze egyetlen beteg került kerekesszékbe. A légzésfunkció, különösen fekvő helyzetben hasonlóan alakult. A betegek terápiára adott válaszában nagy variabilitást figyeltünk meg, ami csak részben mutatott összefüggést a terápiás fehérje ellen termelődő antitestszinttel. Az ERT eredményessége jelentősen függött a betegséget okozó mutáció típusától, a betegség státuszától a kezelés kezdetekor, a beteg fizikai aktivitásától és táplálkozási szokásaitól. Az innovatív orphan gyógyszerekkel kezelt betegek hosszú távú követése kiemelkedően fontos ahhoz, hogy megismerjük a kezelés valós hasznát és a betegek igényeit.
Petefészekrákban szenvedő betegek nem sebészi kezelése
A petefészekrákban szenvedő betegek kezelésében alapvető a kellően radikális műtét, amely az egyéb módszerek eredményességét is meghatározza. Az ezt követően, egy ülésben végzett hyperthermiás intraperitonealis kemoterápia 40,5–42,5 Celsius-fokos citosztatikus oldat perfúziójával történik. A szisztémás kezelések megválasztásában a hat hónapos progressziómentesség a mérföldkő, ezentúl platinaszenzitív, ezen belül -refrakter vagy -rezisztens betegségről van szó. A citosztatikus kezelés fejlődése az alkilálószerektől a platinaszármazékokon át a paklitaxel alkalmazásáig terjed, különféle kombinációkkal, egyre jobb eredményekkel és mind kevesebb mellékhatással. A célzott terápiában az érújdonképződés-gátlók (főleg a bevacizumab) és a DNS-hibák javítását megakadályozó, PARP-gátlók a legjelentősebbek; ez utóbbiak esetében általában a platinaérzékenység feltétel, míg a BRCA-mutáció már nem mindig követelmény. Az utóbbi időben az immunterápiával kapcsolatban is ígéretes vizsgálatok folynak. A hormonkezelés fő előnye a jó tolerálhatóság. A gyógyszerek alkalmazásának sikerei mellett visszaszorulni látszik a sugárterápia, pedig a teljes peritonealis felszín ellátása – különösen a korszerű besugárzási technikák alkalmazása mellett – a kemoterápia alternatívája lehet, a palliatív irradiáció pedig a tünetek csökkentése mellett a gyógyszermentes időszakot is megnyújthatja, s a kombinálás lehetőségei további távlatokat nyitnak meg.
A kezelések sorrendje áttétes colorectalis rákban
Az áttétes colorectalis rák (mCRC) a legtöbb esetben gyógyíthatatlan állapot, de a beteg élettartama a korszerű kemoterápiás és célzott gyógyszeres kezelésekkel meghosszabbítható. Ugyanakkor nem teljesen tisztázott, hogy ezeket a gyógyszereket a kezelés különböző vonalaiban milyen optimális sorrendben kellene használni. A tanulmányban számba veszik a jelenleg rendelkezésre álló kezeléseket és az optimális kezelési sorrendet az mCRC első, második és harmadik választású ellátása során, de érintik a kezelési sorrendet és a kezelések átértékelését befolyásoló biológiai aspektusokat is. A hatásos első vonalú kezelés kulcsszerepet játszik a betegség végső kimenetelének alakulásában, ezért a különböző klinikai faktorok és biológiai markerek – mint a RAS és a BRAF – ismeretében kell azt megválasztani. A második vonalban alkalmazandó kezelés az első vonalban adott szisztémás kezeléstől függ. A legtöbb betegnél antiangiogén kezelések (például bevacizumab, ramucirumab és afl ibercept) bevezetése is indokolt, míg az epidermalis növekedési faktor receptor (EGFR-) gátlás alkalmazása a második vonalban nem hosszabbítja meg az élettartamot. Harmadik vonalban nagyon fontos a molekuláris profil ismerete, a vad típusú RAS-t mutató daganatos betegeknél EGFR-gátlókat (cetuximab vagy panitumumab) tartalmazó regorafenib és trifl uridin/tipiracil kezelést alkalmaznak. A pembrolizumabbal vagy nivolumabbal ± ipilimumabbal végzett immunkezelést szükséges megfontolni a magas mikroszatellita-instabilitást mutató betegségben. A HER2/neu amplifikációt megcélzó kezelések sikeresek lehetnek az ilyen abnormitást mutató colorectalis tumoros esetekben. A kezelések sorrendjének eldöntését tovább bonyolítják a kezeléseknek a daganatos progresszió eltérő jellege miatt szükségessé vált megszakításai vagy beszűkítései. Jelenleg is vizsgálják mCRC-s betegeken a kezelések optimális sorrendjét és azok optimális ütemezését. A molekuláris profilok megismerésével új targeteket lehet kijelölni, ráadásul egyre jobban kezdjük megérteni a daganatoknak a gyógyszerhatások alatt bekövetkező folyamatait, amelyek végül befolyásolhatják a kezelési sorrendet is.
Az olmesartan: egy angiotenzinkonvertálóenzim-gátló hatással rendelkező angiotenzin-II-receptor-blokkoló
Mindenki számára ismert a renin-angiotenzin rendszer (RAS) kóros aktivációjának hypertoniát és cardiovascularis betegségeket okozó hatása. A krónikus RAS-aktiváció hozzájárul az erek, a vesék, illetve a szív progresszív diszfunkciójához.
Célvérnyomás-tartomány és kettős renin-angiotenzinaldoszteron rendszer gátlása krónikus vesebetegségben
Ez a kommentár a Magyar Hypertonia Társaság „A hypertoniabetegség ellátásának irányelvei 11. kiadásának (továbbiakban: Irányelv) a nem albuminuriás krónikus vesebetegek célvérnyomás-tartományára és a hypertoniás betegek renin-angiotenzin-aldoszteron rendszerének (RAS) kombinált gátlására vonatkozó ajánlásaival kapcsolatos észrevételeket tárgyalja.
1.
2.
3.
4.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről5.
1.
2.
Klinikai Onkológia
A rosszindulatú daganatok fenotípusának plaszticitása és az immunogén mimikri3.
Klinikai Onkológia
A szarkopénia mérése komputertomográfiával és jelentősége az onkológiai betegeknél4.
5.