Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 30
A 2023. évi San Antonió-i Emlőrák-Szimpózium összefoglalója
Az emlőrákkal foglalkozó szakemberek minden évben nagy érdeklődéssel várják a San Antonió-i emlőrák-szimpózium legújabb eredményeit. 2023 decemberében is nagy érdeklődés kísérte a szimpóziumot. Sokan várták a nemrég kezdett vizsgálatok elsődleges eredményei mellett a korábban ismertetett klinikai vizsgálatok legújabb adatait is.
Nivolumab+kemoterápia vagy nivolumab+ipilimumab kombináció gastrooesophagealis rákban
A standard első vonalbeli kemoterápia a humán epidermalis növekedési faktor receptor 2 negatív (HER2)-vel nem rendelkező gastrooesophagealis adenocarcinomában szenvedő betegek többségénél egy éven belül a betegség progressziójához és halálhoz vezet. A nivolumab+kemoterápia a 12 hónapos követés során a kemoterápiához képest jobb általános túlélést mutatott.
A CheckMate-649 vizsgálat hároméves utánkövetési eredményei alátámasztják az első vonalbeli nivolumabbal kombinált kemoterápia eredményességét előrehaladott nyelőcső-, gastrooesophagealis junctio és gyomor-adenocarcinoma esetén
A gastrooesophagealis daganatok továbbra is jelentős egészségügyi problémát jelentenek. Az előrehaladott stádiumú rák prognózisa kedvezőtlen, a hagyományos első vonalú kemoterápia alkalmazásával a várható életkilátás HER2-negatív betegség esetén nem éri el az egy évet (1). Az immunterápia megjelenése fontos mérföldkövet jelentett számos rosszindulatú kórkép gyógyszeres kezelésében. A legjelentősebb előrelépést az immunogén tulajdonságú tumortípusok ellátásában sikerült elérni. A gastrooesophagealis daganatok ugyanakkor rendkívül heterogének, nem minden esetben várható az immunterápia hatékonysága. Az immunkezelés szempontjából prediktív értékű biomarkernek tekinthetők a mikroszatellita-instabilitás (MSI) és a programozott sejthalál ligandum 1 (PD-L1) expressziója (2).
Aktualitások az emlőrák kezelésében, kiemelt témák a 45. San Antonió-i Emlőrák Kongresszusról
A SABCS (San Antonió-i Emlőrák-szimpózium) a legrangosabb onkológiai események egyike, amely 2022-ben 45. alkalommal került megrendezésre az Amerikai Egyesült Államokban.
Harmadvonalban alkalmazott terápiával elért hosszú, progressziómentes túlélés metasztatikus gyomorrákban
Hatvannyolc éves, nem dohányzó, jó általános állapotú, de kissé soványabb (BMI: 17) diabeteses, hypertoniás férfi beteg hasi fájdalom, melaena miatt került felvételre a területileg illetékes sürgősségi osztályra. Vérzésforrás lokalizációjának meghatározása céljából akut gasztroszkópiát végeztek nála, melynek során a gyomor kisgörbülete mentén nagy kiterjedésű, makroszkóposan malignusnak imponáló vérző fekélyt találtak. Sikeres endoszkópos vérzéscsillapítás (klipp + noradrenalinos injekció) történt, a laesióból vett minta szövettani vizsgálata magas grádusú intestinalis típusú adenocarcinomát igazolt.
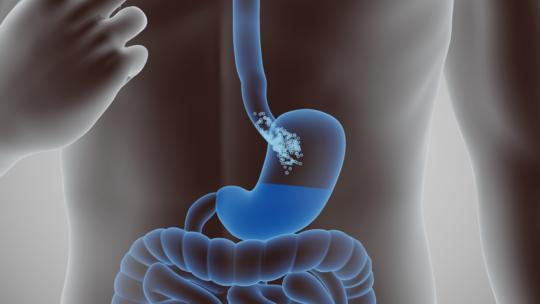
Gondolatok a gyomorrákos betegek nem sebészi kezeléséről
A gyomorrákos betegek oki és tüneti kezelése az oncoteam javaslatán alapuló, interdiszciplináris feladat, amelynek során a beteg állapotára kiemelt figyelmet kell fordítani. Hazánkban a perioperatív (neoadjuváns és adjuváns) kemoterápia, még inkább a radiokemoterápia várható előnyeikhez képest kevésbé elterjedt módszerek. Az áttétes betegség kezelésében legjobb eredmény az első vonalban várható, HER2-pozitív esetben trasztuzumab, HER2-negatív (és PD-L1 pozitív) daganatban a nivolumab és pembrolizumab citosztatikus kezeléshez adásával. A kemoterápia szerei a ciszplatin, kapecitabin, az indikáción túli oxaplatin és a fluoropirimidinek, valamint taxánok különböző kombinációi. Másodvonalban a ramucirumab, harmadvonalban a trifluridin-tipiracil jelentenek újabb lehetőséget. A szerzők hangsúlyozzák a molekuláris célpontalapú terápia, az ezt biztosító (racionális indikációval végzett) új generációs szekvenálás fontosságát, s kitérnek a tumoragnosztikus kezelésre is. Speciális klinikai helyzetek (tumoros vérzés, peritonealis áttétek, idősek, rossz általános állapotúak) ellátására is adnak javaslatot. Hangsúlyozzák, hogy a gondos tüneti terápiát nemcsak terminálisan, hanem a diagnózis felállításától kell szorgalmazni, s hangsúlyozzák, hogy a szomatikus tünetek ellátása mellett a pszichés és szociális tényezők figyelembevétele is szükséges, valamint a beteggel, családdal történő, megfelelő kommunikáció a későbbiekben a különbözőképpen jelentkező elégedetlenség megelőzését is szolgálja.
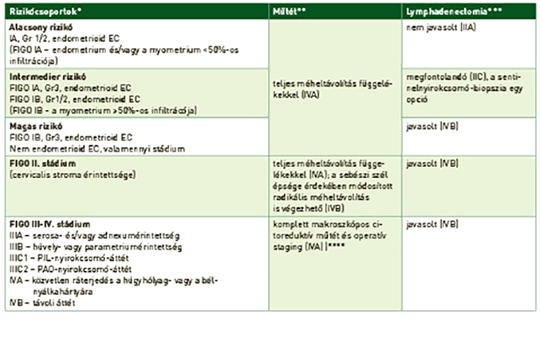
A méh rosszindulatú daganatainak korszerű onkológiai kezelése
Világviszonylatban évente közel 400 000 nőnél igazolódik méhtestrák, amely 2018-ban körülbelül 90 000 nő halálát okozta. Az esetek túlnyomó részét a méhnyálkahártya hormonérzékeny hámjából kiinduló endometriumcarcinomák (EC) alkotják. A sarcomák a méhtestrákok alig 3%-át adják. Az EC-k 80-85%-a jó prognózisú, mivel alacsony gradusú és korai stádiumban kerül felismerésre, amikor a műtét és az esetleges posztoperatív kezelés révén a gyógyulás reális terápiás cél. Az előrehaladott stádiumban diagnosztizált EC és a nem endometrioid altípusok esetén a prognózis lényegesen rosszabb. A magas rizikójú EC optimális adjuváns kezelésére irányuló vizsgálatok egy része még folyamatban van, illetve a bővülő molekuláris ismeretek újabb vizsgálatokat generálnak. A méhtestsarcomák esetében is a sebészi eltávolítás jelenthet kuratív megoldást, az adjuváns kezelésre vonatkozó evidenciák bizonytalanok, egyéni mérlegelést igényelnek. A modern onkoterápia érájában már nemcsak a betegségmentes élet meghosszabbítására, hanem az élet minőségének minél teljesebb megőrzésére is törekszünk. A nőgyógyászati onkológiában ezt jelenti a fertilitás vagy a funkcionáló ováriumok lehetőség szerinti megőrzése; a magas morbiditással járó szisztémás lymphadenectomia indikációs körének szűkítése; a kedvezőbb mellékhatásprofilú brachytherapia alkalmazása a teljes kismedencei besugárzás helyett. A modern onkoterápia az úgynevezett biológiai kezelések által az előrehaladott betegségek ellátásának is a részévé vált: kemoterápia mellett/után progrediáló esetekben a pembrolizumab az EC és a sarcomák esetén is alkalmazható mikroszatellita-instabilitás vagy magas tumormutációs terheltség esetén, míg az NTRK fúziós gén jelenlétében larotrectinib vagy entrectinib mint célzott tirozinkináz-gátlók javasolhatók. Az EC-k 70-80%-át kitevő mikroszatellita-stabil esetekben (nem endometrioid altípusokban is!) a pembrolizumab lenvatinibbel kombinációban adható a kemoterápia után. Az EC területén gyarapodnak továbbá az egyéb célzott terápiás szerekkel szerzett tapasztalatok is (anti-HER2 serosus carcinomában, mTOR-gátló kezelés, endokrin terápia, más immun checkpoint inhibitorok, tirozinkináz-gátlók, PARP-gátlók és kombinációs kezelések). A jelen munka a méhtestrákok onkoterápiájáról kíván rövid összefoglalást nyújtani az aktuális szakmai ajánlások és a folyamatban lévő vizsgálatok bemutatásával.
Az emlőrák hormonkezelése
A fejlett országokban a nők 12%-ának lesz emlőrákja az élete folyamán. Ez az áttekintés az emlőrák szisztémás endokrin kezelésének jelenlegi lehetőségeivel foglalkozik. Az emlőrákokat három nagy alcsoportba lehet osztani a szövettani vizsgálat során értékelt három marker (ER, PR, HER2-receptorok) jelenléte és hiánya alapján. A nem áttétes betegeknél a kezelés célja a lokoregionális és a távoli kiújulás megelőzése. Az adjuváns hormonterápia alkalmazásának időtartama fontos kérdés a mindennapi onkológiai gyakorlatban. Áttétes betegeknél a terápia célja az élet meghosszabbítása, az életminőség megőrzése és a daganatos betegséggel kapcsolatos tünetek palliálása. A HR+ emlőrákos betegek monoterápiában és kombinált kezelések részeként is kaphatnak endokrin ellátást. Az új terápiás megközelítések és a nemzetközi gyógyszerfejlesztési erőfeszítések eredményeként egyre több terápiás lehetőség áll rendelkezésre mind a korai emlőrákos betegek, mind az áttétes betegek számára.
A kezelések sorrendje áttétes colorectalis rákban
Az áttétes colorectalis rák (mCRC) a legtöbb esetben gyógyíthatatlan állapot, de a beteg élettartama a korszerű kemoterápiás és célzott gyógyszeres kezelésekkel meghosszabbítható. Ugyanakkor nem teljesen tisztázott, hogy ezeket a gyógyszereket a kezelés különböző vonalaiban milyen optimális sorrendben kellene használni. A tanulmányban számba veszik a jelenleg rendelkezésre álló kezeléseket és az optimális kezelési sorrendet az mCRC első, második és harmadik választású ellátása során, de érintik a kezelési sorrendet és a kezelések átértékelését befolyásoló biológiai aspektusokat is. A hatásos első vonalú kezelés kulcsszerepet játszik a betegség végső kimenetelének alakulásában, ezért a különböző klinikai faktorok és biológiai markerek – mint a RAS és a BRAF – ismeretében kell azt megválasztani. A második vonalban alkalmazandó kezelés az első vonalban adott szisztémás kezeléstől függ. A legtöbb betegnél antiangiogén kezelések (például bevacizumab, ramucirumab és afl ibercept) bevezetése is indokolt, míg az epidermalis növekedési faktor receptor (EGFR-) gátlás alkalmazása a második vonalban nem hosszabbítja meg az élettartamot. Harmadik vonalban nagyon fontos a molekuláris profil ismerete, a vad típusú RAS-t mutató daganatos betegeknél EGFR-gátlókat (cetuximab vagy panitumumab) tartalmazó regorafenib és trifl uridin/tipiracil kezelést alkalmaznak. A pembrolizumabbal vagy nivolumabbal ± ipilimumabbal végzett immunkezelést szükséges megfontolni a magas mikroszatellita-instabilitást mutató betegségben. A HER2/neu amplifikációt megcélzó kezelések sikeresek lehetnek az ilyen abnormitást mutató colorectalis tumoros esetekben. A kezelések sorrendjének eldöntését tovább bonyolítják a kezeléseknek a daganatos progresszió eltérő jellege miatt szükségessé vált megszakításai vagy beszűkítései. Jelenleg is vizsgálják mCRC-s betegeken a kezelések optimális sorrendjét és azok optimális ütemezését. A molekuláris profilok megismerésével új targeteket lehet kijelölni, ráadásul egyre jobban kezdjük megérteni a daganatoknak a gyógyszerhatások alatt bekövetkező folyamatait, amelyek végül befolyásolhatják a kezelési sorrendet is.
Az áttétes colorectalis rák molekuláris altípusai és a terápiás döntések fejlődése
A colorectalis ráknak (CRC) klinikailag igen jelentős molekuláris heterogenitása van, amely különböző szinteken jelentkezik: a genomikában, az epigenomikában, a transzkripcióban és a mikrokörnyezetben. A karcinogenezis során szerzett genomikus történések hajtják („drive”) áttétes helyzetben a rák progresszióját. Például a KRAS- és az NRAS-mutációk jelzik azokat a daganatsejt-populációkat, amelyek refrakterek az EGFR monoklonális antitestekre, a BRAFV600E-mutációt hordozók viszont rosszabb kimenetelre számíthatnak a standard kezelések és a kombinált célzott kezelések mellett, míg a HER2-amplifi káció arra utal, hogy a daganat különlegesen érzékeny egy kettős HER2-blokáddal szemben. A többszörös, ritka géneltérések által hajtott EGFR monoklonális antitestek elleni rezisztencia jelentős átfedésben van a primer, valamint a szerzett rezisztencia mechanizmusában a klónszelekciós folyamat során. Ebben a tekintetben refrakter esetekben a keringő tumor-DNS szekvenciális vizsgálata vezethet gyógyszerek kifejlesztéséhez. A ritka kinázfúziós események és a DNS-károsodás utáni repair-ben részt vevő gének komplex eltéréseit is leírták, amelyek a célzott kezelések targetjei lehetnek. Másrészt a transzkripció szubtípusai és a jelátviteli utak aktivációs jelei szintén prognosztikai és potenciálisan prediktív értékkel bírnak áttétes colorectalis rákban. Ezek a jelek a stromalis sejtek és az immunkörnyezeti sejtek, valamint a daganatsejtek közötti interakciókat jelzik. Például a mikroszatellita-instabilitást mutató (MSI) vagy a POLE ultramutáns CRC-daganatsejtek különlegesen érzékenyek az immunellenőrzőpont-gátlókra, míg az olyan mesenchymalis fenotípusú daganatok, amelyeket az immunszuppresszív molekulák aktivációja jellemez, jó tárgyai lehetnek egy új immunterápiás kombináció kialakítására. Ebben a cikkben átnézzük az áttétes CRC-ben kimutatott, célzott terápiára alkalmas onkogéneltéréseket és -szignatúrákat, valamint tárgyaljuk az új molekuláris diagnosztikus próbák klinikai alkalmazásának lehetőségeit.
1.
2.
3.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről4.
5.
1.
2.
Klinikai Onkológia
A rosszindulatú daganatok fenotípusának plaszticitása és az immunogén mimikri3.
Klinikai Onkológia
A szarkopénia mérése komputertomográfiával és jelentősége az onkológiai betegeknél4.
5.