Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 23
Az immunterápiák pulmonológiai mellékhatásai
Az immuncheckpoint-gátlók megjelenése átírta az onkológiai kezeléseket a szolid tumorok és a hematológiai malignitások esetében is. Ez az áttörés megérkezett a tüdőtumorok kezelésében is.
Út a szívhez a vesén át. A residualis cardiovascularis rizikó csökkentésének újabb távlatai – a mesodermalis eredetű szervek kommunikációs útvonalai és mediátorai
A cardiovascularis betegségek továbbra is magas morbiditási adatai a ”maradék” rizikótényezők feltárását indokolják. Az embrionális fejlődés folyamán a cardiovascularis szervek a mesodermából fejlődnek ki, a sejtvonalak között fennmaradó humorális és mechanikus kommunikáció részben magyarázatot ad a maradék cardiovascularis rizikó jelenségére, részben pedig új terápiás célpontok körvonalazódásához vezet.
Immunellenőrzőpont-gátló terápiák okozta bőrmellékhatások
Az elmúlt évtizedben az immunellenőrzőpont-gátlók (ICI) megjelenésével az onkológiai betegek ellátása jelentős változáson ment keresztül. Ezen új terápiás szerek megjelenésével új mellékhatásprofilt is meg kellett tanulnunk.
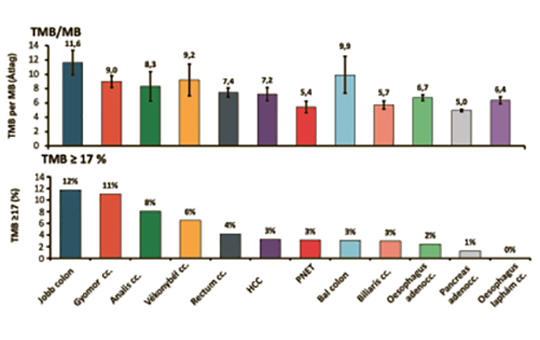
Biomarkerek szerepe a gastrointestinalis daganatok kezelésében
Összefoglaló – A komprehenzív molekuláris profilvizsgálatokon, a bioinformatika fejlődésén alapuló precíziós onkológiai megközelítés, célzott terápia és immunellenőrzőpont-inhibitorok (immune checkpoint inhibitors – ICI) gyökeresen változtatta meg az onkoterápia eredményeit. Az előrehaladott, metasztatikus stádiumú emésztőrendszeri daganatokban szenvedő betegek kedvezőtlen túlélési esélye jelentősen javult az új terápiás lehetőségek alkalmazásától. A sikeres terápia azonban számos molekuláris jellemző ismeretét, meghatározását igényli – PD-L1 expresszió, MSI (mikroszatellita-instabilitás)/dMMR (mismatch repair deficiency), TMB (tumor mutational burden), rezisztenciamutációk, genetikai variánsok jelenléte. Jelen összefoglaló célja áttekintést adni a gastrointestinalis (GI) traktus rosszindulatú daganatainak precíziós onkológiai szemléletű kezelésében alkalmazható prediktív és prognosztikus biomarkerek szerepéről, jelentőségéről.
A RAAS-gátlók pozitív hatása COVID-19-betegek körében
A metaanalízis célja annak megállapítása volt, hogy milyen hatással bírnak a hipertenzív, illetve bármely egyéb okból RAAS-gátlót szedő COVID-19-betegek morbiditására és mortalitására a SARS-CoV-2 vírus sejtbe lépését esetlegesen befolyásoló szerek.
Fókuszban
2020. ÁPRILIS 27.
Van-e hatásosságbeli különbség a PD-1, illetve PD-L1 gátlók között szolid tumorok esetén?
Eredeti közlemény: Duan J, Cui L, Zhao X, et al. Use of immunotherapy With Programmed Cell Death 1 vs Programmed Cell Death Ligand 1 Inhibitors in Patients With Cancer. A Systematic Review and Meta-analysis. JAMA Oncol 2020;6(3):375-84. https://doi.org/10.1001/jamaoncol.2019.5367
A renin-angiotenzin-aldoszteron rendszert gátló gyógyszerek és a Covid-19 kockázata
A közlemény eredményei alapján, az 5 vizsgált, leggyakrabban alkalmazott vérnyomáscsökkentő gyógyszercsoport közül egyik sem növelte jelentősen a pozitív Covid-19 tesztnek a valószínűségét, illetve, hogy a pozitív teszteredményű betegek között súlyosabb lesz a betegség lefolyása.
COVID-19 és az ACE-gátlók/ARB-k szedése
A renin-angiotenzin rendszert gátló gyógyszerek alkalmazásának az összegfüggése a magas vérnyomásban és az új coronavirus okozta betegségben (COVID-19) szenvedő páciensek betegségének a súlyosságával és a halálozási kockázattal. A kínai Wuhani Központi Kórházában végzett vizsgálat eredményei
Előrehaladott NSCLC kezelése immunellenőrzőpontgátlókkal vagy egyidejű kemoterápiával
A tüdődaganat a tumoros halálozás vezető oka. A tüdődaganatok 80-90%-a nem kissejtes típusú (NSCLC), ami az esetek többségében már áttétes formában kerül kimutatásra, ezért az ötéves túlélés csak 0% és 5% között mozog. Az immunellenőrzőpont-gátlók (ICI-k) bevezetésével nőtt az NSCLC-s, melanomás, urothelialis és vesecarcinomás betegek élettartama. Az NSCLC immunkezelésének alapjai az anti-PD-1 monoklonális antitestek (nivolumab, pembrolizumab), valamint az anti-PD-L1 atezolizumab és az anti-CTLA4 ipilimumab, de egyes vizsgálatokban a durvalumab, illetve a tremelimumab is szerepel.
A tüdőrák immunterápiája az újabb eredmények tükrében
Tíz évvel ezelőtt az előrehaladott stádiumú tüdőrák esetén, mind a kissejtes (SCLC), mind pedig a nem kissejtes (NSCLC) csoportban, a várható átlagos túlélés egy év körüli volt. Ez, sajnos, az SCLC esetén lényegileg mára sem változott. Az NSCLC kezelésében igazi forradalmi időszakot élünk át. A patológiai alcsoportokra specifikált kombinált citotoxikus kemoterápia mellett igen hosszú túléléssel kecsegtet a célzott terápia (EGFR-mutáció, ALK, ROS1, BRAF-pozitivitás esetén). Az SCLC vonatkozásában a klinikai gyakorlat tekintetében jelentős előrelépés a gyógyszeres kezelésben az utóbbi harminc évben nem történt. Az újabb terápiás lehetőség NSCLC fennállásakor előrehaladott stádiumban az immunellenőrzőpont-gátló terápia, amely három éve már a klinikumban is a komplex kezelés része, hazánkban is. A PD1, a PDL1 és a CTLA4-gátló vegyületek beépítése a terápiás gyakorlatba igazi, új kihívás. Előrehaladott stádiumú NSCLC fennállásakor, magas PDL1-expresszió esetén, első vonalban új standard a pembrolizumab-monoterápia. Második vonalban mind a pembrolizumab, mind a nivolumab, mind pedig az atezolizumab evidenciaalapon adható. Az NSCLC-betegek mintegy harmadát kitevő lokálisan kiterjedt esetekben a radiokemoterápia után alkalmazott konszolidációs fenntartó durvalumab terápia új hatékony lehetőség. Az eddigi gyógyszeres terápiás nihilizmus az SCLC esetén oldódni látszik. Az antitestgyógyszerkonjugátummal végzett terápia alkalmazásának lehetősége már a közeljövőben a klinikumban is várható. A nivolumab, illetőleg a nivolumab + ipilimumab kombináció szintén ígéretes eredményekkel kecsegtet SCLC másod-, illetőleg többedvonalbeli kezeléseként. A biomarker-szelekción alapuló kezelési terv mind NSCLC, mind pedig SCLC esetén részben gyakorlat, részben kutatási irány (például PDL1-expresszió, szomatikus mutációs arány [TMB], DLL3, cMyc stb.). A különböző gyógyszeres kezelési modalitások egyedi alkalmazása helyett az okos, biomarker-szelekción alapuló komplex terápiás stratégia segíthet e betegség eddigi szerény terápiás eredményeinek javításában, krónikus betegséggé való formálásában.
1.
2.
3.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről4.
5.
1.
2.
Klinikai Onkológia
A rosszindulatú daganatok fenotípusának plaszticitása és az immunogén mimikri3.
Klinikai Onkológia
A szarkopénia mérése komputertomográfiával és jelentősége az onkológiai betegeknél4.
5.