Gastrointestinalis stroma tumorok
2016. JANUÁR 11.
2016. JANUÁR 11.
Szöveg nagyítása:
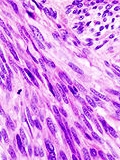
A gastrointestinalis stroma tumorok (GIST) mesenchymalis eredetű solid daganatok. Incidenciájuk 11-14 beteg / 1 millió ember / év. A betegek átlagéletkora a betegség felismerésekor 60 év, a férfiakat és a nőket hasonló arányban érinti. A GIST-ok leggyakrabban a gyomorfalban (60%) és a vékonybelek falában (30%) alakul ki. A tumorok kb. 30%-a malignus daganat, rendszerint intraabdominális terjedéssel és májba történő áttétképződéssel. A nyirookcsomóba történő áttétképzés nem jellemző a GIST-okra. A tumorok kialakulását genetikai eltérés okozza. A patogenetikai háttérben az áll, hogy a bélfal speciális, ún. Cajal-sejteinek sejtfelszíni KIT tirozin-kináz receptoraiban aktiváló mutációk alakulnak ki. Emiatt olyan sejten belüli jelátviteli útvonalak lesznek folyamatosan aktívak, aminek következtében a Cajal-sejtek osztódása, proliferációja és differenciálódása kikerül a normális szabályozás alól. Mindez tumorképződéshez vezet. . A daganatok legfontosabb szövettani jellemzője a CD117 pozitivitás. A CD117 a KIT receptor extracellularis részének epitopja, amihez specifikus antitest kötődhet. A GIST tumorok álatal okozott tünetek többfélék lehetnek: a leggyakoribb általános tünetek közé tartozik a gastrointestinalis vérzés (30-40%-ban) valamint hányinger, hányás, hasi diszkomfort és testsúly csökkenés jelentkezhet. Emellett a lokalizációtól függő specifikusabb eltérések is előfordulhatnak: dysphagia nyelőcső tumor esetén, epeúti obstrukció Vater papilla daganat esetén, vékonybél daganat esetén pedig intussusceptio, ileus alakulhat ki. A GIST felismerésében a kontrasztanyagos CT vizsgálat a legfontosabb eszköz. A tumorok rendszerint heterogén halmozású lágy szövetként ábrázolódnak, amiben nem ritkán necrotikus területek is megfigyelhetőek. A diagnózist segítheti az endoscopos ultrahang vizsgálat, aminek során szövettani mintavételre is lehetőség van vékonytű biopsiás módszerrel. A daganatok és különösen a metastasisok kimutatásában érzékeny módszer a FDG-PET vizsgálat. A 2 cm-nél kisebb GIST-ok kezelésében a komplett sebészi rezekció az elsőnek választandó módszer. Az ajánlott szegment rezekció során a törékeny és lágy tumorszövet nagy gondossággal, tumormentes szélekkel, intakt tokkal távolítandó el. A legújabb ajánlások szerint, a mucosa lamina propriaját el nem érő kis méretű daganat esetén, endoscopos mucosa rezekció is megpróbálható. A 2 cm-nél nagyobb méretű, a bélfali mucosa mélyebb rétegeibe terjedő daganatok esetén szintén műtéti eltávolítás javasolt, azonban ezekben az esetekben preoperativ tirozin-kináz gátló kezelés ajánlott. A kezelés hatására a tumorméret csökkenése érhető el, ami után nagyobb sikerrel végezhető el a sebészi rezekció. A KIT receptor tirozin-kináz hatékony gátlószere az imatinib. Ennek szerkezete hasonló az ATP molekulához, ami a receptor ATP kötőhelyéhez kapcsolódva megakadályozza a valódi ATP megkötését és ezáltal a KIT-jelátviteli útvonal aktiválódását. Az imatinib hatékonysága eltérő a különböző KIT mutációk esetén. A legjobb hatékonyságot azokban a betegekben igazolták, ahol a KIT gén 11-es exonján alakult ki mutáció. Az ajánlott napi dózis 400 mg/nap, ami bizonyos esetekben 800 mg/nap dózisig emelhető. A kezelés sikerességét, azaz a tumorméret csökkenését, kontrasztanyagos CT vizsgálattal ajánlott ellenőrizni. A komplett sebészi rezekció után a betegek 50%-ában daganatkiújulás vagy áttétképződés figyelhető meg. Ezért a legújabb ajánlások szerint az imatinib terápia a műtétet követően is elengedhetetlen minden betegnél minimum 3 éven keresztül. Tumorkiújulás és/vagy áttétek megjelenése esetén szintén imatinib terápia alkalmazandó. Az imatinib mellékhatásainak megjelenése (folyadék retenció, hasmenés, hányinger, fáradtság, izomgörcsök, hasi fájdalom, súlyosabb esetekben májelégtelenség, tüdőkárosodás, cytopeniák) illetve az imatinib hatástalansága esetén (a betegek 10-20%-ában) sunitinib terápia választandó. Tirozin-kináz gátló terápia mellett peritonealis terjedés esetén intraperitonealis kemoterápiát kell alkalmazni (cisplatin és doxorubicin vagy mitoxantron). Májmetasztázisok esetén radiofrekvenciás abláció jöhet szóba. A magas tumorkiújulási és malignizálódási arány miatt a betegek hosszútávú követése elengedhetetlen. Az ajánlások szerint 3-6 havonta kontrasztanyagos CT vizsgálat elvégzése szükséges. Eredeti közlemény: A gist of gastrointestinal stromal tumors: A review Ashwin Rammohan, Jeswanth Sathyanesan, Kamalakannan Rajendran, Anbalagan Pitchaimuthu, Senthil-Kumar Perumal, UP Srinivasan, Ravi Ramasamy, Ravichandran Palaniappan, Manoharan Govindan World J Gastrointest Oncol 2013 June 15; 5(6): 102-112 Szemlézte: dr. Tőke Judit, belgyógyász szakorvos
Az inzulinrezisztencia több betegség, szindróma pathogenezisében részt vesz, ezek közül a legfontosabb a metabolikus szindróma, a 2-es típusú cukorbetegség, a polycystás ovarium szindróma
A rheumatoid arthritis (RA) patomechanizmusának ismert résztvevői az aktivált T-sejtek által stimulált B-sejtek és a monocyta-macrophag rendszer sejtjei, amelyek jelentős mennyiségű gyulladásos citokint termelnek. A citokinek hatásukat a különböző sejteken megjelenő receptorok közvetítésével fejtik ki.
Klinikum
A húgysav keletkezésének vannak endogen (purinszintézis, sejtpusztulás) és exogen (táplálkozás) forrásai. A kezelésnek tehát ennek megfelelően kell, hogy legyen nem csak endogen, hanem exogen útja is, ami magát a táplálkozást (és a helyes életvitelt is) foglalja magába.
Gyulladásos bélbetegség esetén több mint duplájára nő a demencia kockázata; IBD-ben szenvedőknél 7 évvel korábban kezdődik az elbutulás.
Mint az akkor a kutatásszervező Ventavia Research Group alkalmazásában álló regionális igazgató a The BMJ-nek elmondta, a Ventavia adatokat hamisított, nem maszkolt/nem vak módon kezelte a betegeket, nem megfelelően képzett vakcinátorokat alkalmazott, és a III. fázisú vizsgálatok során nem követte megfelelően a betegek által jelentett adverz eseményeket. A cég minőség-ellenőrzéssel foglalkozó munkatársai olyan sok problémát találtak, aminek megoldására képtelenek voltak. Miután a Ventavia vezetését a regionális igazgató, Brook Jackson többször is tájékoztatta a problémákról, az FDA-nak is panaszos e-mailt írt – a Ventavia még aznap kirúgta.
Klinikai vizsgálatok igazolják, hogy az RA-s nőknek kevesebb gyermekük születik, illetve gyakoribb köztük a gyermektelenség, különösen, ha fiatal életkorban (30 éves kor előtt) diagnosztizálják betegségüket, illetve ha a diagnózis felállításakor még nincs gyermekük.
Az American College of Cardiology és az American Heart Association utoljára 2006-ban közölt irányelveket a szívbillentyű-betegség kezelésére. Azóta az infectiv endocarditis (IE) megelőzésével kapcsolatban számos új eredmény született, amelyek szükségessé tették az irányelvek jelen frissítését. Egyes szakembereket meglephetnek majd az irányelvek, amelyek jelentősen eltérnek a korábbiaktól…
Klinikum
A glükózamint több kettős vak, placebokontrollos, hosszú távú vizsgálatban is kedvező hatásúnak találták, jelentősen csökkentette a térdarthrosisban szenvedő betegek fájdalmát, az ízület merevségét, javította a fizikai teljesítményt.
A spondylarthritisek (SpA-k) patogenezisének központi helyszíne a számtalan kisebb-nagyobb enthesis, ahol mechanikai stressz és szisztémás IL23-túltermelődés következtében aktiválódnak az enthesis szövetéhez kötött speciális, Th17 fenotípusú rezidens T-sejtek. A szisztémás IL23 fő forrása a vastagbél, a betegség fő genetikai kóroki tényezője, a HLA-B27 molekula pedig a szintézisének végső lépései során fellépő kóros sejtélettani reakció révén váltja ki macrophagokban az IL23 túltermelődését.
Idegtudományok
Beszámoló az MPT XVII. Vándorgyűléséről
1.
2.
3.
4.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről5.
1.
2.
Klinikai Onkológia
A rosszindulatú daganatok fenotípusának plaszticitása és az immunogén mimikri3.
Klinikai Onkológia
A szarkopénia mérése komputertomográfiával és jelentősége az onkológiai betegeknél4.
5.
HOZZÁSZÓLÁSOK
0 hozzászólás