Az eLitMed.hu orvostudományi portál a böngészés tökéletesítése érdekében cookie-kat használ.
Ha bővebb információkat szeretne kapni a cookie-k használatáról és arról, hogyan módosíthatja a beállításokat, kattintson ide: Tájékoztató az eLitMed.hu Cookie-használatáról.
Részletes keresés
Kérjük, állítsa be a paramétereket!
Találatok száma: 51
Jobb előbb, mint később
A legújabb vizsgálatok szerint a sclerosis multiplex (SM) minél koraibb fázisában érdemes a MAVENCLAD® alkalmazását megkezdeni.
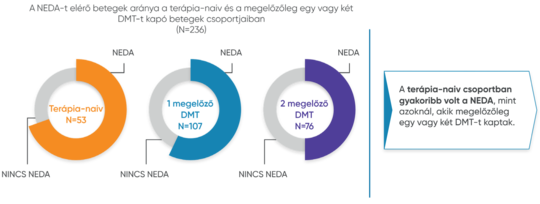
Egy új olasz retrospektív vizsgálatban megállapították, hogy a terápianaiv betegek körében a követési idő végén gyakoribb volt a betegségaktivitást nem mutató NEDA állapot, mint az első, vagy másodvonalbeli terápiáról váltók között.2 Egy finn kutatás is a korai alkalmazás hatékonyságát és jelentőségét bizonyítja:...
A Magyar Neuroimmunológiai Társaság X. Kongresszusa Absztraktfüzet
A Magyar Neuroimmunológiai Társaság X. Kongresszusa Absztraktfüzet Siófok, Magyarország 2023. október 26–28.
A Magyar Neuroimmunológiai Társaság X. Kongresszusa Absztraktfüzet 4.
A Magyar Neuroimmunológiai Társaság X. Kongresszusa Absztraktfüzet Siófok, Magyarország 2023. október 26–28.
Dezmopresszinnel csökkenthető a polyuria a lítium által okozott nephrogen diabetes insipidusban. Rövid irodalmi áttekintés
A lítium, ez az egyszerű ion változatlanul a legjobb, legbiztonságosabb és a legkevésbé költséges kezelések közé tartozik a bipoláris betegség visszatérő epizódjainak megelőzésére. Sok betegben azonban a lítium alkalmazása vesemellékhatásokkal társul. A leggyakoribb mellékhatás a vizeletkoncentráció zavara, amely lítium által okozott permanens nephrogen diabetes insipidushoz vezethet.
A ketamin neocorticalis hatásai
Cichon és munkatársai a Nature Neuroscience-ben megjelent cikkükben mutatják be, hogy egérben a ketaminnal indukálható disszociált állapotot az aktív és kevésbé aktív („csendes”) kérgi piramissejtek aktivitási állapotának megváltozása váltja ki.
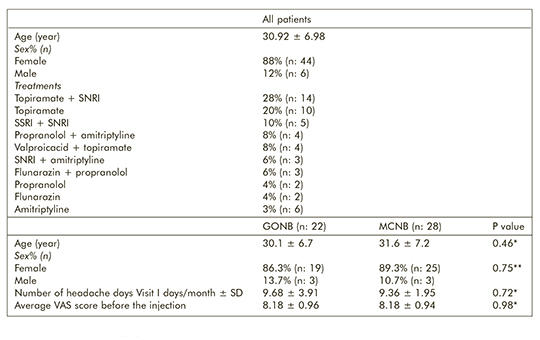
[Hatékonyabb-e az egy ülésben beadott több lidokaininjekció a migrén kezelésében? Három hónapos utánkövetési eredmények]
[Perifériás idegblokád-technikák haszná- latosak mind az akut, mind a profilaktikus migrénkezelés- ben. Vizsgálatunk célja az volt, hogy megállapítsuk: hatékonyabban csökkenthetjük-e a migrénben szenvedők fájdalmát, ha a nagyobb occipitalis ideg (GON) blokád- ján kívül a supraorbitalis ideg (SON) és az infraorbitalis ideg (ION) blokádját is alkalmazzuk.]
Idegtudományok
2022. MÁRCIUS 16.
Agitáció kezelése ketaminnal sürgősségi osztályon
A ketamin egy nem kompetitív NMDA-receptor-antagonista, mely alacsony adagban fájdalomcsillapító hatású, magasabb dózistartományban pedig disszociatív szedációt okoz, ezért procedurális és általános szedatívumként is alkalmazható. Gyors hatásbeállás, kedvező kardiovaszkuláris hatások és a légzési drive megtartása miatt, melyet az alkalmazásához társuló ritka cardiopulmonaris szövődményráta is igazol, a ketamin jó választás lehet gyors, biztonságos, agitált vagy erőszakos betegekben alkalmazható szedatívumként is.
Epilepsziával járó autoimmun encephalitis miatt kezelt betegek klinikai összegzése epilepsziacentrumban
Az autoimmun encephalitisek a kóros, gyakran epilepsziát okozó immunológiai folyamatok széles körét ölelik föl, melyekben számos esetben kimutathatók neuronalis intracelluláris vagy sejtfelszíni antigének ellen termelődő antitestek. A betegség prevalenciáját napjainkban is alábecsülik, a diagnosztikus lépések és a pontos kezelési metodika nem teljesen tisztázott. Célunk az Országos Klinikai Idegtudományi Intézet Epilepszia Részlegén autoimmun encephalitis miatt gondozott betegek egyes alcsoportjai közötti klinikai, radiológiai, pszichopatológiai és elektrofiziológiai különbségek összegzése. Összesen 40 beteget választottunk be vizsgálatunkba; a betegeket a detektált antitestek, a klinikai, radiológiai, elektrofiziológiai szempontok alapján 9 különböző csoportba soroltuk. A legtöbb (n=11) beteg esetében GAD elleni antitestet találtunk, GABA-B receptor elleni antitest a legkevesebb, 1 beteg esetében volt. A legalacsonyabb átlagéletkorral (16,7 év) a posztinfekciós encephalitisszel (FIRES) diagnosztizált betegek, a legmagasabbal (50,4 év) a paraneoplasiás antitesteket termelő betegek rendelkeztek. A társbetegségeket megfigyelve az anti-GAD antitesttel rendelkezők több mint felének autoimmun pajzsmirigybetegsége volt. A vizsgált vasculitisszel diagnosztizált, anti-GABA-B antitesttel rendelkező és Rasmussen-kórban szenvedő betegeknél a koponya-MRI-vizsgálaton a betegségükkel összefüggő eltérés látszott, míg akiknél paraneoplasiás vagy anti-NMDA antitestet detektáltunk, a betegséggel összefüggésben lévő MRI-eltérés nem igazolódott. Az egy csoportba sorolt betegek antiepileptikus, illetve immunszuppresszáns kezelésre adott válasza is hasonló volt. A felszíni antigének ellen termelődött antitesttel bíró betegek esetén jobb volt a terápiás válasz, a leginkább terápiarefrakter betegek a Rasmussen- és a FIRES-csoportba tartoztak. Az autoimmun encephalitis egyes alcsoportjainak fenotípusa hasonló, de a klinikai megnyilvánulás, az EEGés az MR-vizsgálatok átfogó értékelése segíthet egy jól meghatározott rendellenesség diagnosztizálásában. Néhány példát említve, a pajzsimigybetegséggel társuló, MRI-negatív epilepszia hátterében anti-GAD-pozitív encephalitis is állhat. Memóriazavarral, TGA-val járó rosszullétek esetén későbbi életkorban paraneoplasiás mechanizmust is feltételezhetünk, ez segíthet malignus folyamat felfedezésében. Az autoimmun encephalitisben szenvedő betegekre csoportspecifikusan más-más klinikai minták igazak, és egy-egy csoportra különböző terápiás szükséglet, illetve különböző terápiás válasz jellemző. A jövő kihívása többek között a betegség korai felismerése, az encephalitis hátterében álló immunpatológiai folyamatok pontosabb megértése, és a megfelelő időben történő célzott kezelés kidolgozása, melyhez további vizsgálatok szükségesek.
NMDAR-encephalitissel átfedő demyelinisatiós szindróma – diagnosztikai és terápiás kérdések
Az anti-N-metil-D-aszpartát-receptor (NMDAR-) encephalitis az NMDAR GluN1 alegysége elleni IgGantitestekkel társuló autoimmun kórkép. A tünetek súlyossága ellenére csak a betegek 35%-ánál mutatható ki koponya-MRI-vel károsodás, ami leggyakrabban monofázisos formában fordul elő. A legfrissebb adatok alapján azonban az anti-NMDAR encephalitisben szenvedők kis százalékánál további relapszusok jelentkezhetnek, melyek hátterében demyelinisatiós laesiók mutathatók ki. A szakirodalomban egyre több adat lelhető fel, miszerint az NMDAR-encephalitis átfedést mutathat más autoimmum, demyelinisatiós kórképpel, leggyakrabban neuromyelitis optica spektrum betegséggel (főként anti- MOG ellenanyag-pozitív estekben), ritkábban sclerosis multiplexszel. A felmerülő diagnosztikai nehézségeket egy eset kapcsán mutatjuk be. A 24 éves férfi pszichiátriai beutalást követően 2 hónapos tünetkezdetet követően először 2014 májusában került felvételre a Neurológiai Klinikára memóriazavar, bal oldali latens hemiparesis kivizsgálása céljából. Akkor készült koponya-MRI-n disszeminált, gócos agyi folyamat ábrázolódott, gyűrűszerű kontrasztanyag-halmozással, kétoldali hippocampus-érintettséggel. A látott kép leginkább ADEM-nek felelt meg. A liquorban oligoklonális gammopathia látszott. A virális és paraneoplasiás eredetet kizártuk. Intravénás szteroidterápiára átmeneti javulás jelentkezett, azonban a terápia leépítését követően ismételt állapotrosszabbodás következett be. A szteroidterápia ismétlése érdemi változást nem hozott, plazmaferézisben részesült, azathioprinterápiát kapott. A diagnosztikai vizsgálatok során az ellenanyag-vizsgálat alapján anti- NMDAR encephalitis diagnózist állítottuk fel. PET CTvel követtük 3 évig. Állapota stagnált, koponya-MRI-n sem jelent meg új laesio, kifejezett jobb oldali hippocampalis atrophia látszott. Imuran elhagyását követően 2 évvel kettős látása jelentkezett, koponya-MRI-vizsgálaton novum fehérállományi laesiók jelentek meg. A látott radiológiai kép és a korábbi liquorlelet, valamint a klinikum alapján felmerült sclerosis multiplex lehető- sége, intravénás nagy dózisú szteroidterápiát alkalmaztunk. Szérum-aquaporin-4, anti-MOG, anti-NMDAR ellenanyag- vizsgálat a szteroidterápiát követően készült, negatív eredményt adott. A szakirodalmat részletesen áttekintve az anti-MOG ellenanyag-pozitív NMO szövődik leggyakrabban az NMDA-R encephalitisszel átfedő demyelinisatiós szindrómával, a sclerosis multiplex ettől jóval ritkább. A közös hatékony terápiás opció a rituximab, aminek támogatását kérvényeztük.
1.
2.
3.
Ideggyógyászati Szemle Proceedings
Egészségügyi szakmai irányelv az akut ischaemiás stroke diagnosztikájáról és kezeléséről4.
5.
1.
2.
Klinikai Onkológia
A rosszindulatú daganatok fenotípusának plaszticitása és az immunogén mimikri3.
Klinikai Onkológia
A szarkopénia mérése komputertomográfiával és jelentősége az onkológiai betegeknél4.
5.